9-10高一下·河北唐山·期中
名校
解题方法
1 . 在一体积固定的密闭容器中加入反应物A、B,发生如下反应:A+2B=3C。反应经2min后,A的浓度从开始时的1.0mol·L-1降到0.8mol·L-1。已知反应开始时B的浓度是1.2mol·L-1。
(1)2min末B、C的浓度____ 。
(2)用A表示该反应2min内的平均速率____ 。
(1)2min末B、C的浓度
(2)用A表示该反应2min内的平均速率
您最近一年使用:0次
2022-02-10更新
|
755次组卷
|
7卷引用:2009---2010学年唐山二中高一第二学期期中化学试卷
(已下线)2009---2010学年唐山二中高一第二学期期中化学试卷(已下线)2011-2012学年广东省梅州市曾宪梓中学高一5月月考化学试卷陕西省西安中学2019-2020学年高一下学期期中考试(平行班)化学试题江苏省扬州市江都区邵伯高级中学2020-2021学年高一下学期期中考试化学试题(已下线)6.1.1 化学反应速率-2021-2022学年高一化学10分钟课前预习练(苏教版2019必修第二册)苏教2020版化学必修第二册专题6第一单元 化学反应速率与反应限度课后习题福建省福州市福清市虞阳中学2022-2023学年下学期高一年第一次月考化学试卷
2 . 硫粉和S2-反应可以生成多硫离子S ,如:S+S2-→S
,如:S+S2-→S 、2S+S2-→S
、2S+S2-→S 。 在10 mL S2-溶液中加入0.080 g硫粉,控制条件使硫粉完全反应,检测到溶液中最大聚合度的多硫离子是S32-,且离子浓度之比符合等比数列1,10,……10n-1。,若不考虑其他副反应,计算反应后溶液中S2-的浓度c1=
。 在10 mL S2-溶液中加入0.080 g硫粉,控制条件使硫粉完全反应,检测到溶液中最大聚合度的多硫离子是S32-,且离子浓度之比符合等比数列1,10,……10n-1。,若不考虑其他副反应,计算反应后溶液中S2-的浓度c1=_______ ,其起始浓度c0=_______ 。
 ,如:S+S2-→S
,如:S+S2-→S 、2S+S2-→S
、2S+S2-→S 。 在10 mL S2-溶液中加入0.080 g硫粉,控制条件使硫粉完全反应,检测到溶液中最大聚合度的多硫离子是S32-,且离子浓度之比符合等比数列1,10,……10n-1。,若不考虑其他副反应,计算反应后溶液中S2-的浓度c1=
。 在10 mL S2-溶液中加入0.080 g硫粉,控制条件使硫粉完全反应,检测到溶液中最大聚合度的多硫离子是S32-,且离子浓度之比符合等比数列1,10,……10n-1。,若不考虑其他副反应,计算反应后溶液中S2-的浓度c1=
您最近一年使用:0次
2021-07-15更新
|
100次组卷
|
3卷引用:第32届中国化学奥林匹克竞赛(江苏赛区)初赛试题
第32届中国化学奥林匹克竞赛(江苏赛区)初赛试题浙江省丽水市缙云中学等三校2021-2022学年高三12月份联考化学试题(已下线)解密02 物质的量(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)
3 . I.分析某一种不纯的Na2S,已知其中除含有Na2S·9H2O外,还含有Na2S2O3·5H2O,取此试样10.00g配制成500.0mL溶液。
(1)取试样溶液25.00mL于碘量瓶中,加入50.00mL0.05250mol·L-1的I2,用0.1010mol·L-1Na2S2O3溶液滴定多余的I2,用去16.91mL。
(2)取50.00mL试样溶液,用ZnCO3悬浮液沉淀除去其中的Na2S后(忽略体积影响),取滤液的一半,用0.05000mol·L-1I2溶液滴定其中的Na2S2O3,用去5.65mL。
①请写出上述实验涉及的化学方程式_______
②根据以上实验结果,可算出该不纯的硫化钠样品中:Na2S·9H2O的质量分数为_______ ,Na2S2O3·5H2O的质量分数为_______ 。
II.人体正常血液的pH值维持在7.35-7.45间,且数值不会因为少量酸碱性的物质进入血液而发生明显变化,原因是血液中含有缓冲物质,主要由H2CO3/NaHCO3予以调节。人体运动时肌肉收缩产生的乳酸如果过多的进入血液,导致pH<7.3则会造成酸中毒(Acidosis)。计算血液pH与c(H2CO3)/c( )的关系式为:
)的关系式为:_______ ;当血液pH为7.35时,其中的c(H2CO3)/c( )比值为
)比值为_______ 。(已知H2CO3的电离常数pKa1=6.35,pKa2=10.33)
(1)取试样溶液25.00mL于碘量瓶中,加入50.00mL0.05250mol·L-1的I2,用0.1010mol·L-1Na2S2O3溶液滴定多余的I2,用去16.91mL。
(2)取50.00mL试样溶液,用ZnCO3悬浮液沉淀除去其中的Na2S后(忽略体积影响),取滤液的一半,用0.05000mol·L-1I2溶液滴定其中的Na2S2O3,用去5.65mL。
①请写出上述实验涉及的化学方程式
②根据以上实验结果,可算出该不纯的硫化钠样品中:Na2S·9H2O的质量分数为
II.人体正常血液的pH值维持在7.35-7.45间,且数值不会因为少量酸碱性的物质进入血液而发生明显变化,原因是血液中含有缓冲物质,主要由H2CO3/NaHCO3予以调节。人体运动时肌肉收缩产生的乳酸如果过多的进入血液,导致pH<7.3则会造成酸中毒(Acidosis)。计算血液pH与c(H2CO3)/c(
 )的关系式为:
)的关系式为: )比值为
)比值为
您最近一年使用:0次
20-21高一上·江苏镇江·阶段练习
名校
解题方法
4 . 按要求完成下列填空
(1)现有标准状况下CO和CO2混合气体8.96L,其质量为16g,则此混合气体中,CO的体积分数是_______ ,质量之比是_______ 。
(2)40.5g某金属氯化物MCl2中含有0.6 mol Cl-,则金属M的相对原子质量为_______
(3)已知16gA和20gB恰好完全反应生成0.04mol C和31.76g D,则C的摩尔质量为_______
(4)将10.6g Na2CO3溶于水配成1L溶液,向该溶液中加入一定量NaCl固体,使溶液中Na+的物质的量浓度为0.4 mol/L(假设溶液体积不变),需加入NaCl的质量为_______ ;Cl-的物质的量浓度为_______ 。
(5)将4g NaOH溶于_______ g水中,可使溶液中H2O与Na+的物质的量之比等于20:1,若测得该溶液的密度为1.1g/cm-3,溶液中c(Na+)为_______ 。
(1)现有标准状况下CO和CO2混合气体8.96L,其质量为16g,则此混合气体中,CO的体积分数是
(2)40.5g某金属氯化物MCl2中含有0.6 mol Cl-,则金属M的相对原子质量为
(3)已知16gA和20gB恰好完全反应生成0.04mol C和31.76g D,则C的摩尔质量为
(4)将10.6g Na2CO3溶于水配成1L溶液,向该溶液中加入一定量NaCl固体,使溶液中Na+的物质的量浓度为0.4 mol/L(假设溶液体积不变),需加入NaCl的质量为
(5)将4g NaOH溶于
您最近一年使用:0次
名校
5 . 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
(1)如图是 (g)和
(g)和 (g)反应生成1mol
(g)反应生成1mol (g)过程中能量的变化示意图,请写出
(g)过程中能量的变化示意图,请写出 和
和 反应的热化学方程式∶
反应的热化学方程式∶___________
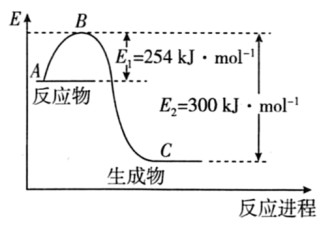
(2)若已知下列数据∶
试根据表中及图中数据计算N-H的键能∶___________ kJ·mol-1
(3)用 催化还原NOx还可以消除氮氧化物的污染。已知:
催化还原NOx还可以消除氮氧化物的污染。已知:
 ①
①
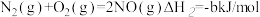 ②
②
若1mol 还原NO至
还原NO至 ,则该反应过程中的反应热△H3
,则该反应过程中的反应热△H3___________ kJ/mol(用含a、b的式子表示)。
(4)捕碳技术(主要指捕获 )在降低温室气体排放中具有重要的作用。目前
)在降低温室气体排放中具有重要的作用。目前 和
和 已经被用作工业捕碳剂,它们与
已经被用作工业捕碳剂,它们与 可发生如下可逆反应:
可发生如下可逆反应:
反应I: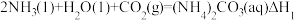
反应II: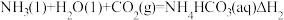
反应Ⅲ: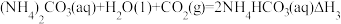
则△H3与△H1、△H2之间的关系是△H3=___________ 。
(1)如图是
 (g)和
(g)和 (g)反应生成1mol
(g)反应生成1mol (g)过程中能量的变化示意图,请写出
(g)过程中能量的变化示意图,请写出 和
和 反应的热化学方程式∶
反应的热化学方程式∶
(2)若已知下列数据∶
| 化学键 | H-H | N=N |
| 键能/kJ·mol-1 | 435 | 943 |
试根据表中及图中数据计算N-H的键能∶
(3)用
 催化还原NOx还可以消除氮氧化物的污染。已知:
催化还原NOx还可以消除氮氧化物的污染。已知: ①
①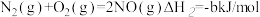 ②
②若1mol
 还原NO至
还原NO至 ,则该反应过程中的反应热△H3
,则该反应过程中的反应热△H3(4)捕碳技术(主要指捕获
 )在降低温室气体排放中具有重要的作用。目前
)在降低温室气体排放中具有重要的作用。目前 和
和 已经被用作工业捕碳剂,它们与
已经被用作工业捕碳剂,它们与 可发生如下可逆反应:
可发生如下可逆反应:反应I:
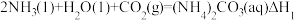
反应II:
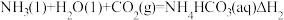
反应Ⅲ:
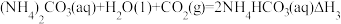
则△H3与△H1、△H2之间的关系是△H3=
您最近一年使用:0次
2021-06-20更新
|
1309次组卷
|
7卷引用:四川省成都市实验外国语学校(西区)2019-2020 学年高二上学期期中考试化学试题
四川省成都市实验外国语学校(西区)2019-2020 学年高二上学期期中考试化学试题江苏省连云港市厉庄高级中学2022-2023学年高三上学期第一次质量检测化学试题江苏省常熟市王淦昌高级中学2022-2023学年高二上学期10月月考化学试卷(已下线)第1章 化学反应与能量(选拔卷)-【单元测试】2021-2022学年高二化学尖子生选拔卷(人教版选修4)四川省攀枝花市成都外国语学校2021-2022学年高二上学期10月月考化学试题(已下线)1.2 反应热的计算(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)新疆维吾尔自治区伊犁哈萨克自治州新源县第二中学2021-2022学年高三上学期第二次月考化学试题
解题方法
6 . 写出下列反应的热化学方程式:
(1)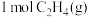 与适量
与适量 反应,生成
反应,生成 和
和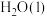 ,放出
,放出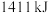 的热。
的热。___________ 。
(2)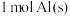 与适量
与适量 发生反应,生成
发生反应,生成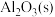 ,放出
,放出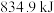 的热。
的热。___________ 。
(1)
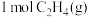 与适量
与适量 反应,生成
反应,生成 和
和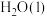 ,放出
,放出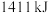 的热。
的热。(2)
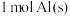 与适量
与适量 发生反应,生成
发生反应,生成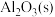 ,放出
,放出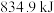 的热。
的热。
您最近一年使用:0次
2021-06-05更新
|
382次组卷
|
3卷引用:(苏教版2019)必修第二册专题6 化学反应与能量变化 第二单元 化学反应中的热 课时1 化学反应中的能量变化
名校
7 . 化学工业中会产生大量含铬废水。需进行无害化处理检测达标后才能排放。
(1)工业常用NaHSO3还原法处理,方法:向酸性废水中加入NaHSO3使Cr2O 还原成为Cr3+,然后加入熟石灰调节废水的pH,使Cr3+完全沉淀。
还原成为Cr3+,然后加入熟石灰调节废水的pH,使Cr3+完全沉淀。
①写出NaHSO3与Cr2O 反应的离子方程式:
反应的离子方程式:___________ 。
②已知25℃时Ksp[Cr(OH)3]=6.4×10-31,若除去废水中Cr3+,使其浓度小于1×10-5mol·L-1,此时溶液中的c(H+)<___________ mol·L-1
(2)废水中铬元素总浓度的测定方法:向一定量含Cr2O 和Cr3+的酸性废水样中加入足量(NH4)2S2O8,溶液将Cr3+氧化成Cr2O
和Cr3+的酸性废水样中加入足量(NH4)2S2O8,溶液将Cr3+氧化成Cr2O ,煮沸除去过量的(NH4)2S2O8;再加入过量的KI溶液,Cr2O
,煮沸除去过量的(NH4)2S2O8;再加入过量的KI溶液,Cr2O 与I-完全反应生成Cr3+和I2后,以淀粉为指示剂,用Na2S2O3标准溶液滴定至终点。测定过程中物质的转化关系为Cr3+
与I-完全反应生成Cr3+和I2后,以淀粉为指示剂,用Na2S2O3标准溶液滴定至终点。测定过程中物质的转化关系为Cr3+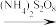 Cr2O
Cr2O
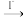 I2
I2 S4O
S4O 。
。
①上述操作过程中,若无煮沸操作,则测定的铬元素总浓度会___________ (填“偏大”、“偏小”或“不变”)。
②准确移取含Cr2O 和Cr3+的酸性废水样100.00mL,按上述方法测定废水样中铬元素总浓度,消耗0.01000mol·L-1Na2S2O3标准溶液13.50mL。计算该废水中铬元素总浓度(以mg·L-1表示)(写出计算过程)。
和Cr3+的酸性废水样100.00mL,按上述方法测定废水样中铬元素总浓度,消耗0.01000mol·L-1Na2S2O3标准溶液13.50mL。计算该废水中铬元素总浓度(以mg·L-1表示)(写出计算过程)。___________
(1)工业常用NaHSO3还原法处理,方法:向酸性废水中加入NaHSO3使Cr2O
 还原成为Cr3+,然后加入熟石灰调节废水的pH,使Cr3+完全沉淀。
还原成为Cr3+,然后加入熟石灰调节废水的pH,使Cr3+完全沉淀。①写出NaHSO3与Cr2O
 反应的离子方程式:
反应的离子方程式:②已知25℃时Ksp[Cr(OH)3]=6.4×10-31,若除去废水中Cr3+,使其浓度小于1×10-5mol·L-1,此时溶液中的c(H+)<
(2)废水中铬元素总浓度的测定方法:向一定量含Cr2O
 和Cr3+的酸性废水样中加入足量(NH4)2S2O8,溶液将Cr3+氧化成Cr2O
和Cr3+的酸性废水样中加入足量(NH4)2S2O8,溶液将Cr3+氧化成Cr2O ,煮沸除去过量的(NH4)2S2O8;再加入过量的KI溶液,Cr2O
,煮沸除去过量的(NH4)2S2O8;再加入过量的KI溶液,Cr2O 与I-完全反应生成Cr3+和I2后,以淀粉为指示剂,用Na2S2O3标准溶液滴定至终点。测定过程中物质的转化关系为Cr3+
与I-完全反应生成Cr3+和I2后,以淀粉为指示剂,用Na2S2O3标准溶液滴定至终点。测定过程中物质的转化关系为Cr3+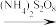 Cr2O
Cr2O
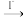 I2
I2 S4O
S4O 。
。①上述操作过程中,若无煮沸操作,则测定的铬元素总浓度会
②准确移取含Cr2O
 和Cr3+的酸性废水样100.00mL,按上述方法测定废水样中铬元素总浓度,消耗0.01000mol·L-1Na2S2O3标准溶液13.50mL。计算该废水中铬元素总浓度(以mg·L-1表示)(写出计算过程)。
和Cr3+的酸性废水样100.00mL,按上述方法测定废水样中铬元素总浓度,消耗0.01000mol·L-1Na2S2O3标准溶液13.50mL。计算该废水中铬元素总浓度(以mg·L-1表示)(写出计算过程)。
您最近一年使用:0次
8 . I.现有以下几种物质①盐酸②醋酸③氢氧化钠④硝酸铵⑤醋酸钠⑥氨水⑦亚硫酸氢钠⑧水。请回答下列问题:
(1)以上物质属于弱电解质的是_______ (填数字序号)。
(2)常温下④的溶液pH<7的原因是_______ (用离子方程式表示)。
(3)常温下⑦的水溶液呈酸性,原因是_______ (用文字叙述)。
(4)常温下,将aLpH=l1的NaOH溶液与bLpH=1的HNO3溶液混合(忽略混合后溶液密度的变化),若所得混合溶液的pH=2,则b:a=_______ 。
(5)已知:
a.常温下:CH3COOH和NH3·H2O的电离平衡常数均为1.74×10-5;
b.CH3COOH+NaHCO3=CH3COONa+CO2↑+H2O;
则NH4HCO3溶液呈_______ 性(填“酸”、“碱”或“中”)。
II.25℃时,向盛有50mLpH=3的HA溶液的绝热容器中加入pH=13的NaOH溶液,加入NaOH溶液的体积(V)与所得混合溶液的温度(T)的关系如图所示。

(6)由图可以推出HA溶液的物质的量浓度为_______ ,25℃时,pH=3的HA溶液的电离度为_______ 。
(7)b点溶液存在质子守恒关系,其关系式是_______ 。
III.(8)已知:Ksp[Al(OH)3]=1×10-33,pH=7.1时Mn(OH)2开始沉淀。室温下,除去MnSO4溶液中的Al3+(使其浓度小于1×10-6mol·L-1),需调节溶液pH范围为_______ 。
(1)以上物质属于弱电解质的是
(2)常温下④的溶液pH<7的原因是
(3)常温下⑦的水溶液呈酸性,原因是
(4)常温下,将aLpH=l1的NaOH溶液与bLpH=1的HNO3溶液混合(忽略混合后溶液密度的变化),若所得混合溶液的pH=2,则b:a=
(5)已知:
a.常温下:CH3COOH和NH3·H2O的电离平衡常数均为1.74×10-5;
b.CH3COOH+NaHCO3=CH3COONa+CO2↑+H2O;
则NH4HCO3溶液呈
II.25℃时,向盛有50mLpH=3的HA溶液的绝热容器中加入pH=13的NaOH溶液,加入NaOH溶液的体积(V)与所得混合溶液的温度(T)的关系如图所示。

(6)由图可以推出HA溶液的物质的量浓度为
(7)b点溶液存在质子守恒关系,其关系式是
III.(8)已知:Ksp[Al(OH)3]=1×10-33,pH=7.1时Mn(OH)2开始沉淀。室温下,除去MnSO4溶液中的Al3+(使其浓度小于1×10-6mol·L-1),需调节溶液pH范围为
您最近一年使用:0次
名校
9 . 一定量的Cu与足量浓硫酸混合加热,充分反应后生成2.24LSO2气体(标准状况下),反应后溶液体积为500mL。试计算:
(1)参加反应的Cu的质量___ 。
(2)反应后溶液中CuSO4的物质的量浓度___ 。
(1)参加反应的Cu的质量
(2)反应后溶液中CuSO4的物质的量浓度
您最近一年使用:0次
2021-05-27更新
|
633次组卷
|
4卷引用:2020年山西省普通高中学业水平考试化学试题
名校
10 . 0.98 g某有机化合物在纯氧中完全燃烧,只生成2.64 gCO2和0.9gH2O。经测定,该有机化合物的相对分子质量是98。
(1)推断该有机物的分子式(写出计算过程)。_______
(2)该化合物的一种同分异构体X同时满足以下条件
①含有两个甲基;
②含有酮羰基(但不含C=C=O);
③不含有环状结构;
④含有手性碳原子。
写出X的结构简式:_______ 。
(1)推断该有机物的分子式(写出计算过程)。
(2)该化合物的一种同分异构体X同时满足以下条件
①含有两个甲基;
②含有酮羰基(但不含C=C=O);
③不含有环状结构;
④含有手性碳原子。
写出X的结构简式:
您最近一年使用:0次



