化学工业中会产生大量含铬废水。需进行无害化处理检测达标后才能排放。
(1)工业常用NaHSO3还原法处理,方法:向酸性废水中加入NaHSO3使Cr2O 还原成为Cr3+,然后加入熟石灰调节废水的pH,使Cr3+完全沉淀。
还原成为Cr3+,然后加入熟石灰调节废水的pH,使Cr3+完全沉淀。
①写出NaHSO3与Cr2O 反应的离子方程式:
反应的离子方程式:___________ 。
②已知25℃时Ksp[Cr(OH)3]=6.4×10-31,若除去废水中Cr3+,使其浓度小于1×10-5mol·L-1,此时溶液中的c(H+)<___________ mol·L-1
(2)废水中铬元素总浓度的测定方法:向一定量含Cr2O 和Cr3+的酸性废水样中加入足量(NH4)2S2O8,溶液将Cr3+氧化成Cr2O
和Cr3+的酸性废水样中加入足量(NH4)2S2O8,溶液将Cr3+氧化成Cr2O ,煮沸除去过量的(NH4)2S2O8;再加入过量的KI溶液,Cr2O
,煮沸除去过量的(NH4)2S2O8;再加入过量的KI溶液,Cr2O 与I-完全反应生成Cr3+和I2后,以淀粉为指示剂,用Na2S2O3标准溶液滴定至终点。测定过程中物质的转化关系为Cr3+
与I-完全反应生成Cr3+和I2后,以淀粉为指示剂,用Na2S2O3标准溶液滴定至终点。测定过程中物质的转化关系为Cr3+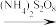 Cr2O
Cr2O
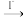 I2
I2 S4O
S4O 。
。
①上述操作过程中,若无煮沸操作,则测定的铬元素总浓度会___________ (填“偏大”、“偏小”或“不变”)。
②准确移取含Cr2O 和Cr3+的酸性废水样100.00mL,按上述方法测定废水样中铬元素总浓度,消耗0.01000mol·L-1Na2S2O3标准溶液13.50mL。计算该废水中铬元素总浓度(以mg·L-1表示)(写出计算过程)。
和Cr3+的酸性废水样100.00mL,按上述方法测定废水样中铬元素总浓度,消耗0.01000mol·L-1Na2S2O3标准溶液13.50mL。计算该废水中铬元素总浓度(以mg·L-1表示)(写出计算过程)。___________
(1)工业常用NaHSO3还原法处理,方法:向酸性废水中加入NaHSO3使Cr2O
 还原成为Cr3+,然后加入熟石灰调节废水的pH,使Cr3+完全沉淀。
还原成为Cr3+,然后加入熟石灰调节废水的pH,使Cr3+完全沉淀。①写出NaHSO3与Cr2O
 反应的离子方程式:
反应的离子方程式:②已知25℃时Ksp[Cr(OH)3]=6.4×10-31,若除去废水中Cr3+,使其浓度小于1×10-5mol·L-1,此时溶液中的c(H+)<
(2)废水中铬元素总浓度的测定方法:向一定量含Cr2O
 和Cr3+的酸性废水样中加入足量(NH4)2S2O8,溶液将Cr3+氧化成Cr2O
和Cr3+的酸性废水样中加入足量(NH4)2S2O8,溶液将Cr3+氧化成Cr2O ,煮沸除去过量的(NH4)2S2O8;再加入过量的KI溶液,Cr2O
,煮沸除去过量的(NH4)2S2O8;再加入过量的KI溶液,Cr2O 与I-完全反应生成Cr3+和I2后,以淀粉为指示剂,用Na2S2O3标准溶液滴定至终点。测定过程中物质的转化关系为Cr3+
与I-完全反应生成Cr3+和I2后,以淀粉为指示剂,用Na2S2O3标准溶液滴定至终点。测定过程中物质的转化关系为Cr3+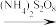 Cr2O
Cr2O
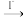 I2
I2 S4O
S4O 。
。①上述操作过程中,若无煮沸操作,则测定的铬元素总浓度会
②准确移取含Cr2O
 和Cr3+的酸性废水样100.00mL,按上述方法测定废水样中铬元素总浓度,消耗0.01000mol·L-1Na2S2O3标准溶液13.50mL。计算该废水中铬元素总浓度(以mg·L-1表示)(写出计算过程)。
和Cr3+的酸性废水样100.00mL,按上述方法测定废水样中铬元素总浓度,消耗0.01000mol·L-1Na2S2O3标准溶液13.50mL。计算该废水中铬元素总浓度(以mg·L-1表示)(写出计算过程)。
更新时间:2021-05-30 10:32:11
|
相似题推荐
计算题
|
较难
(0.4)
【推荐1】为探究化合物A(仅含三种元素,摩尔质量为198g/mol)的组成与性质,设计并完成以下实验:取3.96g化合物A溶于水中,一段时间后全部转化为B(红褐色沉淀)、C(一种碱)和气体单质D(可使带火星的木条复燃),向溶液中加入100mL0.6mol/L稀硫酸,再加入含有0.08mol KOH的溶液,恰好完全反应。过滤,将沉淀洗涤后充分灼烧,得到红棕色固体粉末1.60g;将所得溶液在一定条件下蒸发可得到一种纯净的不含结晶水的盐10.44g。
(1)化合物A所含的元素为____ ,化合物A与H2O反应的离子方程式为:____ 。
(2)化合物A可由FeCl3和KClO在强碱性条件下制得,其反应的离子方程式为:____ 。
(1)化合物A所含的元素为
(2)化合物A可由FeCl3和KClO在强碱性条件下制得,其反应的离子方程式为:
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐2】危化仓库中往往存有钠、钾、硫、白磷(P4)、硝酸铵和氰化钾(KCN)等危险品。请回答下列问题:
(1)NH4NO3为爆炸物,在某温度下按下式进行分解:5NH4NO3=4N2↑+2HNO3+9H2O则被氧化和被还原的氮元素质量之比为________ ;
(2)硫酸铜溶液是白磷引起中毒的一种解毒剂:1lP4+60CuSO4+96H2O=20Cu3P+24H3PO4+60H2SO4。若8molH3PO4生成,则被CuSO4氧化的P4的物质的量为______________ mol;
(3)处理CN一常用的一种方法是用氯气氧化。若某厂废水中含KCN,其浓度为650mg / L。现用氯氧化法处理,发生如下反应(其中N均为-3价):KCN+2KOH+Cl2 = KOCN+2KCl+H2O 。若投入过量液氯,可将氰酸盐进一步氧化为无毒的N2和CO2。请写出该反应的化学方程式,____ ,若处理上述废水20 L,使KCN完全转化为无毒物质,至少需液氯_________ g。
(1)NH4NO3为爆炸物,在某温度下按下式进行分解:5NH4NO3=4N2↑+2HNO3+9H2O则被氧化和被还原的氮元素质量之比为
(2)硫酸铜溶液是白磷引起中毒的一种解毒剂:1lP4+60CuSO4+96H2O=20Cu3P+24H3PO4+60H2SO4。若8molH3PO4生成,则被CuSO4氧化的P4的物质的量为
(3)处理CN一常用的一种方法是用氯气氧化。若某厂废水中含KCN,其浓度为650mg / L。现用氯氧化法处理,发生如下反应(其中N均为-3价):KCN+2KOH+Cl2 = KOCN+2KCl+H2O 。若投入过量液氯,可将氰酸盐进一步氧化为无毒的N2和CO2。请写出该反应的化学方程式,
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐3】(1)已知:将Cl2通入适量KOH溶液,产物中可能有KC1、KClO、KC1O3,且c(Cl-):c(ClO-)的值与温度高低有关。当n(KOH)=amol时,若某温度下,反应后c(Cl-):c(ClO-)=11,则溶液中c(ClO-):c(ClO3-)=_________________
(2)在P+CuSO4+H2O→Cu3P+H3PO4+H2SO4(未配平)的反应中,7.5molCuSO4可氧化P的物质的量为________ mol。生成1molCu3P时,参加反应的P的物质的量为________ mol。
(3)一定量的CuS和Cu2S的混合物投入足量的HNO3中,收集到气体VL(标准状况),向反应后的溶液中(存在Cu2+和SO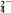 )加入足量NaOH,产生蓝色沉淀,过滤,洗涤,灼烧,得到CuO 16.0g,若上述气体为NO和NO2的混合物,且体积比为1∶1,则V的极小值为
)加入足量NaOH,产生蓝色沉淀,过滤,洗涤,灼烧,得到CuO 16.0g,若上述气体为NO和NO2的混合物,且体积比为1∶1,则V的极小值为________ mL。
(4)向一定量的Fe、FeO、Fe3O4的混合物中,加入1 mol/L 硝酸的溶液100 mL,恰好使混合物全部溶解,且放出336 mL(标准状况下)的气体,向所得溶液中加入KSCN溶液,溶液无红色出现;若取相同质量的Fe、FeO、Fe3O4的混合物,加入1 mol/L的稀硫酸溶液,也恰好使混合物完全溶解(假设还原产物唯一),反应后向所得溶液中加入KSCN溶液,溶液也无红色出现,则所加入的的稀硫酸的体积是__________ mL。
(2)在P+CuSO4+H2O→Cu3P+H3PO4+H2SO4(未配平)的反应中,7.5molCuSO4可氧化P的物质的量为
(3)一定量的CuS和Cu2S的混合物投入足量的HNO3中,收集到气体VL(标准状况),向反应后的溶液中(存在Cu2+和SO
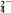 )加入足量NaOH,产生蓝色沉淀,过滤,洗涤,灼烧,得到CuO 16.0g,若上述气体为NO和NO2的混合物,且体积比为1∶1,则V的极小值为
)加入足量NaOH,产生蓝色沉淀,过滤,洗涤,灼烧,得到CuO 16.0g,若上述气体为NO和NO2的混合物,且体积比为1∶1,则V的极小值为(4)向一定量的Fe、FeO、Fe3O4的混合物中,加入1 mol/L 硝酸的溶液100 mL,恰好使混合物全部溶解,且放出336 mL(标准状况下)的气体,向所得溶液中加入KSCN溶液,溶液无红色出现;若取相同质量的Fe、FeO、Fe3O4的混合物,加入1 mol/L的稀硫酸溶液,也恰好使混合物完全溶解(假设还原产物唯一),反应后向所得溶液中加入KSCN溶液,溶液也无红色出现,则所加入的的稀硫酸的体积是
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】某复合肥的主要成分有KCl、NH4H2PO4和CO(NH2)2等。测定该复合肥中氮的质量分数的实验步骤如下:
步骤1:准确称取0.5000 g样品于锥形瓶中,加入足量浓硫酸并加热,不再有CO2溢出时,冷却至室温。
步骤2:向锥形瓶中加入100mL蒸馏水,再加入适量的CaCl2溶液,并用NaOH溶液调节溶液近中性,过滤,洗涤,得0.1550 gCa3(PO4)2沉淀和滤液A。
步骤3:向滤液A中加入过量的甲醛溶液,加指示剂,用0. 5000 mol/LNaOH标准溶液滴定至终点,消耗NaOH溶液22.00 mL。 [已知:4 NH4++6HCHO=4H++(CH2)6N4+6H2O]
(1)步骤1中,CO(NH2)2与硫酸反应的化学方程式为____________________ 。
(2)欲使滤液A中c(PO43—)≤4.0×10-6mol/L,应保持溶液中c(Ca2+)≥______________ mol/L[已知KSP[Ca3(PO4)2]=2.0×10-33]。
(3)复合肥样品中N的质量分数为___________ 。
(4)计算复合肥样品中NH4H2PO4和CO(NH2)2的物质的量之比_____________ (写出计算过程)。
步骤1:准确称取0.5000 g样品于锥形瓶中,加入足量浓硫酸并加热,不再有CO2溢出时,冷却至室温。
步骤2:向锥形瓶中加入100mL蒸馏水,再加入适量的CaCl2溶液,并用NaOH溶液调节溶液近中性,过滤,洗涤,得0.1550 gCa3(PO4)2沉淀和滤液A。
步骤3:向滤液A中加入过量的甲醛溶液,加指示剂,用0. 5000 mol/LNaOH标准溶液滴定至终点,消耗NaOH溶液22.00 mL。 [已知:4 NH4++6HCHO=4H++(CH2)6N4+6H2O]
(1)步骤1中,CO(NH2)2与硫酸反应的化学方程式为
(2)欲使滤液A中c(PO43—)≤4.0×10-6mol/L,应保持溶液中c(Ca2+)≥
(3)复合肥样品中N的质量分数为
(4)计算复合肥样品中NH4H2PO4和CO(NH2)2的物质的量之比
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐2】已知黄钠铁矾[NaxFey(SO4)m(OH)n]具有沉淀颗粒大、沉淀速率快、容易过滤等特点。某研究小组先将某废水中Fe2+氧化为Fe3+,再加入Na2SO4使其生成黄钠铁矾而除去。该小组为测定黄钠铁矾的组成,进行了如下实验:
①称取4.850 g样品,加盐酸完全溶解后,配成100.00 mL溶液A;
②量取25.00 mL溶液A,加入足量的KI,用0.2500 mol·L-1Na2S2O3溶液进行滴定(反应为I2+2Na2S2O3=2NaI+Na2S4O6),消耗30.00 mLNa2S2O3溶液至终点。
③另取25.00 mL溶液A,加足量BaCl2溶液充分反应后,过滤、洗涤、干燥后得沉淀1.165 g。
(1)如何证明步骤③中的沉淀已洗涤干净?___________ 。
(2)用Na2S2O3溶液进行滴定时,使用的指示剂为________ ,滴定到终点的颜色变化为_________ 。
(3)通过计算确定黄钠铁矾的化学式_________ (写出计算过程)。
①称取4.850 g样品,加盐酸完全溶解后,配成100.00 mL溶液A;
②量取25.00 mL溶液A,加入足量的KI,用0.2500 mol·L-1Na2S2O3溶液进行滴定(反应为I2+2Na2S2O3=2NaI+Na2S4O6),消耗30.00 mLNa2S2O3溶液至终点。
③另取25.00 mL溶液A,加足量BaCl2溶液充分反应后,过滤、洗涤、干燥后得沉淀1.165 g。
(1)如何证明步骤③中的沉淀已洗涤干净?
(2)用Na2S2O3溶液进行滴定时,使用的指示剂为
(3)通过计算确定黄钠铁矾的化学式
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】ClO2广泛用于水处理、纸浆漂白等。
(1)制备ClO2原料有NaClO2等,产生的ClO2(g)用蒸馏水吸收得到吸收液A。
①ClO2中氯元素的化合价为___ 。
②NaClO2与盐酸在微热条件下生成ClO2气体(及少量副产物Cl2),写出其反应生成ClO2、NaCl和水的化学方程式:___ 。
(2)碘量法测定ClO2吸收液A中ClO2和Cl2的浓度的主要实验步骤如下:
步骤1.向锥形瓶中加入50mL蒸馏水、25mL100g·L-1KI溶液(足量),再向其中加入5.00mLClO2吸收液(发生反应:2ClO2+2KI=2KClO2+I2,Cl2+2KI=2KCl+I2)。
步骤2.用0.1000mol·L-1Na2S2O3标准溶液滴定(2Na2S2O3+I2=2NaI+Na2S4O6)至浅黄色,再加入1mL淀粉溶液,继续滴定至蓝色刚好消失,消耗Na2S2O3溶液6.00mL。
步骤3.向步骤2的溶液中加入5mL2mol·L-1硫酸溶液酸化,发生反应:KClO2+4KI+2H2SO4=KCl+2K2SO4+2I2+2H2O。
步骤4.重复步骤2操作,第二次滴定又消耗0.1000mol·L-1Na2S2O3溶液20.00mL。
根据上述数据,计算ClO2吸收液A中ClO2和Cl2的浓度___ (单位g·L-1,写出计算过程)。
(1)制备ClO2原料有NaClO2等,产生的ClO2(g)用蒸馏水吸收得到吸收液A。
①ClO2中氯元素的化合价为
②NaClO2与盐酸在微热条件下生成ClO2气体(及少量副产物Cl2),写出其反应生成ClO2、NaCl和水的化学方程式:
(2)碘量法测定ClO2吸收液A中ClO2和Cl2的浓度的主要实验步骤如下:
步骤1.向锥形瓶中加入50mL蒸馏水、25mL100g·L-1KI溶液(足量),再向其中加入5.00mLClO2吸收液(发生反应:2ClO2+2KI=2KClO2+I2,Cl2+2KI=2KCl+I2)。
步骤2.用0.1000mol·L-1Na2S2O3标准溶液滴定(2Na2S2O3+I2=2NaI+Na2S4O6)至浅黄色,再加入1mL淀粉溶液,继续滴定至蓝色刚好消失,消耗Na2S2O3溶液6.00mL。
步骤3.向步骤2的溶液中加入5mL2mol·L-1硫酸溶液酸化,发生反应:KClO2+4KI+2H2SO4=KCl+2K2SO4+2I2+2H2O。
步骤4.重复步骤2操作,第二次滴定又消耗0.1000mol·L-1Na2S2O3溶液20.00mL。
根据上述数据,计算ClO2吸收液A中ClO2和Cl2的浓度
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐1】工业废水中常含有一定量的 ,易被人体吸收积累而导致肝癌。处理工业含铬废水的方法通常是将
,易被人体吸收积累而导致肝癌。处理工业含铬废水的方法通常是将 转化为
转化为 ,再将
,再将 转化为
转化为 沉淀。
沉淀。
(1) 和
和 类似,也是两性氢氧化物,写出
类似,也是两性氢氧化物,写出 的酸式电离方程式:
的酸式电离方程式:_____ 。
(2) 在强碱中可被双氧水氧化为
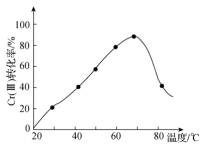
在强碱中可被双氧水氧化为 ,控制其他条件不变,反应温度对
,控制其他条件不变,反应温度对 转化率的影响如图所示。请分析温度超过70℃时,
转化率的影响如图所示。请分析温度超过70℃时, 转化率下降的原因是
转化率下降的原因是_______ 。
(3)溶液中的 与强碱性溶液反应,使
与强碱性溶液反应,使 完全沉淀的
完全沉淀的 为
为_______ {通常认为溶液中离子浓度小于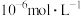 为沉淀完全;
为沉淀完全; 的
的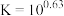 ,
,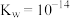 ,
, }。
}。
(4)25℃时,将 的醋酸与
的醋酸与 氢氧化钠等体积混合,反应后溶液恰好显中性,用含a、b式子表示醋酸的电离平衡常数为
氢氧化钠等体积混合,反应后溶液恰好显中性,用含a、b式子表示醋酸的电离平衡常数为_______ 。
(5)标准状况下,将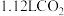 通入
通入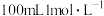 的
的 溶液中,用溶液中微粒的浓度符号完成下列等式:
溶液中,用溶液中微粒的浓度符号完成下列等式: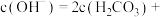
_______ 。
 ,易被人体吸收积累而导致肝癌。处理工业含铬废水的方法通常是将
,易被人体吸收积累而导致肝癌。处理工业含铬废水的方法通常是将 转化为
转化为 ,再将
,再将 转化为
转化为 沉淀。
沉淀。(1)
 和
和 类似,也是两性氢氧化物,写出
类似,也是两性氢氧化物,写出 的酸式电离方程式:
的酸式电离方程式:(2)
 在强碱中可被双氧水氧化为
在强碱中可被双氧水氧化为 ,控制其他条件不变,反应温度对
,控制其他条件不变,反应温度对 转化率的影响如图所示。请分析温度超过70℃时,
转化率的影响如图所示。请分析温度超过70℃时, 转化率下降的原因是
转化率下降的原因是
(3)溶液中的
 与强碱性溶液反应,使
与强碱性溶液反应,使 完全沉淀的
完全沉淀的 为
为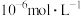 为沉淀完全;
为沉淀完全; 的
的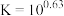 ,
,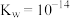 ,
, }。
}。(4)25℃时,将
 的醋酸与
的醋酸与 氢氧化钠等体积混合,反应后溶液恰好显中性,用含a、b式子表示醋酸的电离平衡常数为
氢氧化钠等体积混合,反应后溶液恰好显中性,用含a、b式子表示醋酸的电离平衡常数为(5)标准状况下,将
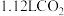 通入
通入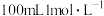 的
的 溶液中,用溶液中微粒的浓度符号完成下列等式:
溶液中,用溶液中微粒的浓度符号完成下列等式: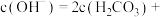
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】按要求回答下列问题。
(1)已知25℃时Ksp[Fe(OH)3]=4.0×10-38,此温度下若在实验室中配制5 mol·L-1 100 mL FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加入_______ mL 2 mol·L-1的盐酸(忽略加入盐酸体积)。
(2)CaSO3溶液与CaCl2溶液混合会生成难溶的CaSO3(Ksp=3.1×10-7),现将等体积的CaCl2溶液与Na2SO3溶液混合,若混合前Na2SO3溶液的浓度为2×10-3 mol·L-1,则生成沉淀所需CaCl2溶液的最小浓度为_______ 。
(3)汽车尾气中的SO2可用石灰水来吸收,生成亚硫酸钙浊液。常温下,测得某纯CaSO3与水形成的浊液pH为9,已知Ka1(H2SO3)=1.8×10-2,Ka2(H2SO3)=6.0×10-9,忽略 的第二步水解,则Ksp(CaSO3)=
的第二步水解,则Ksp(CaSO3)=_______ 。
(4)在某温度下,Ksp(FeS)=6.25×10-18,FeS饱和溶液中 c(H+)与c(S2-)之间存在关系:c2(H+)·c(S2-)=1.0×10-22,为了使溶液里c(Fe2+) 达到1 mol·L-1,现将适量FeS投入其饱和溶液中,应调节溶液中的c(H+)约为_______ 。
(1)已知25℃时Ksp[Fe(OH)3]=4.0×10-38,此温度下若在实验室中配制5 mol·L-1 100 mL FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加入
(2)CaSO3溶液与CaCl2溶液混合会生成难溶的CaSO3(Ksp=3.1×10-7),现将等体积的CaCl2溶液与Na2SO3溶液混合,若混合前Na2SO3溶液的浓度为2×10-3 mol·L-1,则生成沉淀所需CaCl2溶液的最小浓度为
(3)汽车尾气中的SO2可用石灰水来吸收,生成亚硫酸钙浊液。常温下,测得某纯CaSO3与水形成的浊液pH为9,已知Ka1(H2SO3)=1.8×10-2,Ka2(H2SO3)=6.0×10-9,忽略
 的第二步水解,则Ksp(CaSO3)=
的第二步水解,则Ksp(CaSO3)=(4)在某温度下,Ksp(FeS)=6.25×10-18,FeS饱和溶液中 c(H+)与c(S2-)之间存在关系:c2(H+)·c(S2-)=1.0×10-22,为了使溶液里c(Fe2+) 达到1 mol·L-1,现将适量FeS投入其饱和溶液中,应调节溶液中的c(H+)约为
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】电解质水溶液中存在电离平衡、水解平衡、溶解平衡等,请回答下列问题。
(1)已知部分弱酸的电离常数如下表:
①0.1mol/L NaCN溶液和0.1mol/L NaHCO3溶液中,c(CN-)______ c(HCO3- )(填“>”、“<”或“=”)。
②将浓度均为0.1mol/L的CH3COONa、NaCN、NaHCO3和Na2CO3溶液分别稀释100倍,pH变化最小的是__________ 。
③将少量CO2通入NaCN溶液,反应的离子方程式是_____ 。
④室温下,—定浓度的CH3COONa溶液pH=9,用离子方程式表示溶液呈碱性的原因是_____ ,溶液中c(CH3COO-)/c(CH3COOH) =___________ 。
⑤室温下,某溶液中存在着CH3COOH(aq)+HCO3-( aq)⇌CH3COO-(aq) +H2CO3(aq),该反应的平衡常数K =___________ 。
⑥室温下,pH =4的CH3COOH与pH =10的CH3COONa溶液中,由水电离出的c(H+)之比_______ 。
(2)已知室温下Cu(OH)2的Ksp=2×10-20,又知室温下某CuSO4溶液中c(Cu2+)=0.02mol/L,如果要生成Cu(OH)2沉淀,则应调整溶液的pH大于___________
(1)已知部分弱酸的电离常数如下表:
| 弱酸 | CH3COOH | HCN | H2CO3 |
| 电离常数(室温) | Ka= 1.8×10-5 | Ka=4.3×10-10 | Ka1=5.0×10-7 Ka2=5.6×10-11 |
①0.1mol/L NaCN溶液和0.1mol/L NaHCO3溶液中,c(CN-)
②将浓度均为0.1mol/L的CH3COONa、NaCN、NaHCO3和Na2CO3溶液分别稀释100倍,pH变化最小的是
③将少量CO2通入NaCN溶液,反应的离子方程式是
④室温下,—定浓度的CH3COONa溶液pH=9,用离子方程式表示溶液呈碱性的原因是
⑤室温下,某溶液中存在着CH3COOH(aq)+HCO3-( aq)⇌CH3COO-(aq) +H2CO3(aq),该反应的平衡常数K =
⑥室温下,pH =4的CH3COOH与pH =10的CH3COONa溶液中,由水电离出的c(H+)之比
(2)已知室温下Cu(OH)2的Ksp=2×10-20,又知室温下某CuSO4溶液中c(Cu2+)=0.02mol/L,如果要生成Cu(OH)2沉淀,则应调整溶液的pH大于
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】某复合肥的主要成分有KCl、NH4H2PO4和CO(NH2)2等。测定该复合肥中氮的质量分数的实验步骤如下:
步骤1:准确称取0.5000 g样品于锥形瓶中,加入足量浓硫酸并加热,不再有CO2溢出时,冷却至室温。
步骤2:向锥形瓶中加入100mL蒸馏水,再加入适量的CaCl2溶液,并用NaOH溶液调节溶液近中性,过滤,洗涤,得0.1550 gCa3(PO4)2沉淀和滤液A。
步骤3:向滤液A中加入过量的甲醛溶液,加指示剂,用0. 5000 mol/LNaOH标准溶液滴定至终点,消耗NaOH溶液22.00 mL。 [已知:4 NH4++6HCHO=4H++(CH2)6N4+6H2O]
(1)步骤1中,CO(NH2)2与硫酸反应的化学方程式为____________________ 。
(2)欲使滤液A中c(PO43—)≤4.0×10-6mol/L,应保持溶液中c(Ca2+)≥______________ mol/L[已知KSP[Ca3(PO4)2]=2.0×10-33]。
(3)复合肥样品中N的质量分数为___________ 。
(4)计算复合肥样品中NH4H2PO4和CO(NH2)2的物质的量之比_____________ (写出计算过程)。
步骤1:准确称取0.5000 g样品于锥形瓶中,加入足量浓硫酸并加热,不再有CO2溢出时,冷却至室温。
步骤2:向锥形瓶中加入100mL蒸馏水,再加入适量的CaCl2溶液,并用NaOH溶液调节溶液近中性,过滤,洗涤,得0.1550 gCa3(PO4)2沉淀和滤液A。
步骤3:向滤液A中加入过量的甲醛溶液,加指示剂,用0. 5000 mol/LNaOH标准溶液滴定至终点,消耗NaOH溶液22.00 mL。 [已知:4 NH4++6HCHO=4H++(CH2)6N4+6H2O]
(1)步骤1中,CO(NH2)2与硫酸反应的化学方程式为
(2)欲使滤液A中c(PO43—)≤4.0×10-6mol/L,应保持溶液中c(Ca2+)≥
(3)复合肥样品中N的质量分数为
(4)计算复合肥样品中NH4H2PO4和CO(NH2)2的物质的量之比
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】Na2O2曾经是潜水艇或航天器中最理想的供氧剂。下表是人体呼出气体的成分(均为体积百分含量)。
(1)已知一个人一天大约要产生16molCO2,若全部被Na2O2吸收,需要Na2O2_________ g。
(2)若要使被吸收的CO2与产生的O2体积相等,就需要在Na2O2中添加KO2。计算要达到该目的,Na2O2与KO2的物质的量之比______ 已知: 4KO2 + 2CO2 → 2K2CO3 + 3O2
(3)计算100 L空气经过人体呼吸后,呼出气体中O2、H2O(g)、CO2的体积(相同状况下,保留2位小数)。__________________
(4)为保持航天器中空气成分恒定,并充分利用资源,需对人体呼出的气体进行处理,无用物质排出航天器。100L空气经过人体呼吸后,欲使呼出的气体经过处理后恢复原空气成分且体积仍为100L(可供使用的化学试剂只有Na2O2)。通过计算回答:若先利用CO2,是否还要利用水蒸气?若需要利用水蒸气,需要水蒸气多少升?_________
| 空气成分 | 人体呼出 气体成分 | |
| N2 | 78% | 73.65% |
| O2 | 21% | 15.92% |
| H2O | 0.5% | 5.97% |
| CO2 | 0.03% | 3.98% |
(1)已知一个人一天大约要产生16molCO2,若全部被Na2O2吸收,需要Na2O2
(2)若要使被吸收的CO2与产生的O2体积相等,就需要在Na2O2中添加KO2。计算要达到该目的,Na2O2与KO2的物质的量之比
(3)计算100 L空气经过人体呼吸后,呼出气体中O2、H2O(g)、CO2的体积(相同状况下,保留2位小数)。
(4)为保持航天器中空气成分恒定,并充分利用资源,需对人体呼出的气体进行处理,无用物质排出航天器。100L空气经过人体呼吸后,欲使呼出的气体经过处理后恢复原空气成分且体积仍为100L(可供使用的化学试剂只有Na2O2)。通过计算回答:若先利用CO2,是否还要利用水蒸气?若需要利用水蒸气,需要水蒸气多少升?
您最近一年使用:0次



