已知黄钠铁矾[NaxFey(SO4)m(OH)n]具有沉淀颗粒大、沉淀速率快、容易过滤等特点。某研究小组先将某废水中Fe2+氧化为Fe3+,再加入Na2SO4使其生成黄钠铁矾而除去。该小组为测定黄钠铁矾的组成,进行了如下实验:
①称取4.850 g样品,加盐酸完全溶解后,配成100.00 mL溶液A;
②量取25.00 mL溶液A,加入足量的KI,用0.2500 mol·L-1Na2S2O3溶液进行滴定(反应为I2+2Na2S2O3=2NaI+Na2S4O6),消耗30.00 mLNa2S2O3溶液至终点。
③另取25.00 mL溶液A,加足量BaCl2溶液充分反应后,过滤、洗涤、干燥后得沉淀1.165 g。
(1)如何证明步骤③中的沉淀已洗涤干净?___________ 。
(2)用Na2S2O3溶液进行滴定时,使用的指示剂为________ ,滴定到终点的颜色变化为_________ 。
(3)通过计算确定黄钠铁矾的化学式_________ (写出计算过程)。
①称取4.850 g样品,加盐酸完全溶解后,配成100.00 mL溶液A;
②量取25.00 mL溶液A,加入足量的KI,用0.2500 mol·L-1Na2S2O3溶液进行滴定(反应为I2+2Na2S2O3=2NaI+Na2S4O6),消耗30.00 mLNa2S2O3溶液至终点。
③另取25.00 mL溶液A,加足量BaCl2溶液充分反应后,过滤、洗涤、干燥后得沉淀1.165 g。
(1)如何证明步骤③中的沉淀已洗涤干净?
(2)用Na2S2O3溶液进行滴定时,使用的指示剂为
(3)通过计算确定黄钠铁矾的化学式
更新时间:2021-06-06 20:12:04
|
相似题推荐
计算题
|
较难
(0.4)
解题方法
【推荐1】K3[Fe(C2O4)3](三草酸合铁酸钾)可用于摄影和蓝色印刷。工业上制备K3[Fe(C2O4)3]的反应原理如下:
氧化:6FeC2O4+3H2O2+6K2C2O4═4K3[Fe(C2O4)3]+2Fe(OH)3
转化:2Fe(OH)3+3K2C2O4+3H2C2O4═2K3[Fe(C2O4)3]+6H2O
(1)制备1mol三草酸合铁酸钾至少需要H2O2的物质的量为___ 。
(2)制备过程中需防止草酸被H2O2氧化,写出草酸被H2O2氧化的化学方程式:___ 。
(3)K3[Fe(C2O4)3]·xH2O(三草酸合铁酸钾晶体)是一种光敏材料,为测定该晶体中草酸根的含量和结晶水的含量,某实验小组进行了如下实验:
①称量9.820g三草酸合铁酸钾晶体,配制成250mL溶液。
②取所配溶液25.00mL于锥形瓶中,滴加KMnO4溶液至C2O42-全部转化成CO2时,恰好消耗24.00mL0.1000mol•L-1KMnO4溶液。C2O42-被全部转化的标志是___ 。
③计算该晶体的化学式,并写出计算过程。___
氧化:6FeC2O4+3H2O2+6K2C2O4═4K3[Fe(C2O4)3]+2Fe(OH)3
转化:2Fe(OH)3+3K2C2O4+3H2C2O4═2K3[Fe(C2O4)3]+6H2O
(1)制备1mol三草酸合铁酸钾至少需要H2O2的物质的量为
(2)制备过程中需防止草酸被H2O2氧化,写出草酸被H2O2氧化的化学方程式:
(3)K3[Fe(C2O4)3]·xH2O(三草酸合铁酸钾晶体)是一种光敏材料,为测定该晶体中草酸根的含量和结晶水的含量,某实验小组进行了如下实验:
①称量9.820g三草酸合铁酸钾晶体,配制成250mL溶液。
②取所配溶液25.00mL于锥形瓶中,滴加KMnO4溶液至C2O42-全部转化成CO2时,恰好消耗24.00mL0.1000mol•L-1KMnO4溶液。C2O42-被全部转化的标志是
③计算该晶体的化学式,并写出计算过程。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】准确称取6g铝土矿(含Al2O3、Fe2O3、SiO2)样品,放入盛有100 mL H2SO4
溶液的烧杯中,充分反应后过滤,向滤液中加入10 mol/L NaOH溶液,产生沉淀的量与所加NaOH溶液的体积的关系如图所示。求
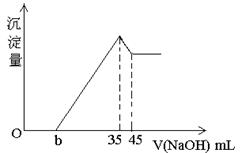
(1)硫酸溶液的物质的量浓度。
(2)若b=2.3,求铝土矿中SiO2的质量分数。
溶液的烧杯中,充分反应后过滤,向滤液中加入10 mol/L NaOH溶液,产生沉淀的量与所加NaOH溶液的体积的关系如图所示。求

(1)硫酸溶液的物质的量浓度。
(2)若b=2.3,求铝土矿中SiO2的质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】(1)写出氯碱工业电解饱和食盐水的化学方程式:_______________
(2)已知:2KMnO4 + 16HCl =2KCl+2MnCl2 +5Cl2↑+8H2O,15.8g KMnO4 与 100mL12mol/L浓盐酸充分反应,固体完全溶解,生成标准状况下氯气的体积为______ L,转移的电子数____ 个,若向反应后的溶液中加入足量的硝酸银,过滤、洗涤、干燥,可得到固体 _____ mol。
(3)将标准状况下 6.72L 的 HCl 溶于水形成 250mL 溶液,取出 10mL 于锥形瓶中,溶质的物质的量浓度为_________ mol/L,向锥形瓶中滴加 0.5mol/LBa(OH)2 溶液,恰好反应,消耗Ba(OH)2 的体积为______ mL。
(2)已知:2KMnO4 + 16HCl =2KCl+2MnCl2 +5Cl2↑+8H2O,15.8g KMnO4 与 100mL12mol/L浓盐酸充分反应,固体完全溶解,生成标准状况下氯气的体积为
(3)将标准状况下 6.72L 的 HCl 溶于水形成 250mL 溶液,取出 10mL 于锥形瓶中,溶质的物质的量浓度为
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】向铜片中加入某浓度的硫酸120ml,在加热条件下反应,待铜片全部溶解后,将其溶液稀释到500ml。再加入足量锌粉,使之充分反应,收集到标准状况下氢气2.24L,过滤残留固体,干燥后称量,质量减轻了7.50g。求:
(1)溶解的铜的质量。______
(2)原硫酸的物质的量浓度。(要求写出简要计算过程)_______
(1)溶解的铜的质量。
(2)原硫酸的物质的量浓度。(要求写出简要计算过程)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】ClO2广泛用于水处理、纸浆漂白等。
(1)制备ClO2原料有NaClO2等,产生的ClO2(g)用蒸馏水吸收得到吸收液A。
①ClO2中氯元素的化合价为___ 。
②NaClO2与盐酸在微热条件下生成ClO2气体(及少量副产物Cl2),写出其反应生成ClO2、NaCl和水的化学方程式:___ 。
(2)碘量法测定ClO2吸收液A中ClO2和Cl2的浓度的主要实验步骤如下:
步骤1.向锥形瓶中加入50mL蒸馏水、25mL100g·L-1KI溶液(足量),再向其中加入5.00mLClO2吸收液(发生反应:2ClO2+2KI=2KClO2+I2,Cl2+2KI=2KCl+I2)。
步骤2.用0.1000mol·L-1Na2S2O3标准溶液滴定(2Na2S2O3+I2=2NaI+Na2S4O6)至浅黄色,再加入1mL淀粉溶液,继续滴定至蓝色刚好消失,消耗Na2S2O3溶液6.00mL。
步骤3.向步骤2的溶液中加入5mL2mol·L-1硫酸溶液酸化,发生反应:KClO2+4KI+2H2SO4=KCl+2K2SO4+2I2+2H2O。
步骤4.重复步骤2操作,第二次滴定又消耗0.1000mol·L-1Na2S2O3溶液20.00mL。
根据上述数据,计算ClO2吸收液A中ClO2和Cl2的浓度___ (单位g·L-1,写出计算过程)。
(1)制备ClO2原料有NaClO2等,产生的ClO2(g)用蒸馏水吸收得到吸收液A。
①ClO2中氯元素的化合价为
②NaClO2与盐酸在微热条件下生成ClO2气体(及少量副产物Cl2),写出其反应生成ClO2、NaCl和水的化学方程式:
(2)碘量法测定ClO2吸收液A中ClO2和Cl2的浓度的主要实验步骤如下:
步骤1.向锥形瓶中加入50mL蒸馏水、25mL100g·L-1KI溶液(足量),再向其中加入5.00mLClO2吸收液(发生反应:2ClO2+2KI=2KClO2+I2,Cl2+2KI=2KCl+I2)。
步骤2.用0.1000mol·L-1Na2S2O3标准溶液滴定(2Na2S2O3+I2=2NaI+Na2S4O6)至浅黄色,再加入1mL淀粉溶液,继续滴定至蓝色刚好消失,消耗Na2S2O3溶液6.00mL。
步骤3.向步骤2的溶液中加入5mL2mol·L-1硫酸溶液酸化,发生反应:KClO2+4KI+2H2SO4=KCl+2K2SO4+2I2+2H2O。
步骤4.重复步骤2操作,第二次滴定又消耗0.1000mol·L-1Na2S2O3溶液20.00mL。
根据上述数据,计算ClO2吸收液A中ClO2和Cl2的浓度
您最近一年使用:0次
【推荐3】往硫酸与硝酸的混合溶液中投入一块未除氧化膜的铝箔,微热使之完全反应,产生2.24 L (已折算为标准状况)NO与H2的混合气体,且该混合气体的平均摩尔质量为13.20 g/mol。
(1)混合气体中NO的体积分数为_________ 。
(2)若将所得混合气体与一定量的氧气在一定条件下充分反应后,恰好全部转化为硝酸溶液。则所用氧气在标准状况下的体积为_________ L。
(3)向铝箔与混酸反应后的溶液中趁热加入一定质量的(NH4)2SO4,冷却后全部溶液正好转化为40.77 g铝铵矾晶体[化学式:NH4Al(SO4)2·12H2O,式量:453]。
①原铝箔中金属铝的质量为_________ g。氧化膜的物质的量为___________ mol。
②计算原混酸中硫酸的质量分数(保留三位小数,写出计算过程)。___________ 。
(1)混合气体中NO的体积分数为
(2)若将所得混合气体与一定量的氧气在一定条件下充分反应后,恰好全部转化为硝酸溶液。则所用氧气在标准状况下的体积为
(3)向铝箔与混酸反应后的溶液中趁热加入一定质量的(NH4)2SO4,冷却后全部溶液正好转化为40.77 g铝铵矾晶体[化学式:NH4Al(SO4)2·12H2O,式量:453]。
①原铝箔中金属铝的质量为
②计算原混酸中硫酸的质量分数(保留三位小数,写出计算过程)。
您最近一年使用:0次



