Na2O2曾经是潜水艇或航天器中最理想的供氧剂。下表是人体呼出气体的成分(均为体积百分含量)。
(1)已知一个人一天大约要产生16molCO2,若全部被Na2O2吸收,需要Na2O2_________ g。
(2)若要使被吸收的CO2与产生的O2体积相等,就需要在Na2O2中添加KO2。计算要达到该目的,Na2O2与KO2的物质的量之比______ 已知: 4KO2 + 2CO2 → 2K2CO3 + 3O2
(3)计算100 L空气经过人体呼吸后,呼出气体中O2、H2O(g)、CO2的体积(相同状况下,保留2位小数)。__________________
(4)为保持航天器中空气成分恒定,并充分利用资源,需对人体呼出的气体进行处理,无用物质排出航天器。100L空气经过人体呼吸后,欲使呼出的气体经过处理后恢复原空气成分且体积仍为100L(可供使用的化学试剂只有Na2O2)。通过计算回答:若先利用CO2,是否还要利用水蒸气?若需要利用水蒸气,需要水蒸气多少升?_________
| 空气成分 | 人体呼出 气体成分 | |
| N2 | 78% | 73.65% |
| O2 | 21% | 15.92% |
| H2O | 0.5% | 5.97% |
| CO2 | 0.03% | 3.98% |
(1)已知一个人一天大约要产生16molCO2,若全部被Na2O2吸收,需要Na2O2
(2)若要使被吸收的CO2与产生的O2体积相等,就需要在Na2O2中添加KO2。计算要达到该目的,Na2O2与KO2的物质的量之比
(3)计算100 L空气经过人体呼吸后,呼出气体中O2、H2O(g)、CO2的体积(相同状况下,保留2位小数)。
(4)为保持航天器中空气成分恒定,并充分利用资源,需对人体呼出的气体进行处理,无用物质排出航天器。100L空气经过人体呼吸后,欲使呼出的气体经过处理后恢复原空气成分且体积仍为100L(可供使用的化学试剂只有Na2O2)。通过计算回答:若先利用CO2,是否还要利用水蒸气?若需要利用水蒸气,需要水蒸气多少升?
2013·上海徐汇·二模 查看更多[1]
(已下线)上海市三区(徐汇、松江、金山)2013届高三(二模)化学试题
更新时间:2020-03-28 19:26:41
|
相似题推荐
计算题
|
较难
(0.4)
解题方法
【推荐1】实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。某同学取一定量铁铝合金与100mL某浓度的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入 的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。
的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。
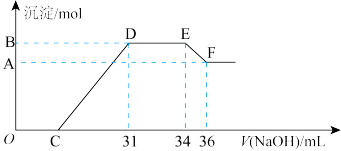
试回答:
(1)写出铁与该硝酸反应的离子方程式_______ ;
(2)合金中铁的质量为_______ g;
(3)原硝酸的物质的量浓度为_______  。
。
 的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。
的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。
试回答:
(1)写出铁与该硝酸反应的离子方程式
(2)合金中铁的质量为
(3)原硝酸的物质的量浓度为
 。
。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】用含FeS290%的硫铁矿为原料,用接触法制硫酸,如果原料的利用率为96%,硫酸的产率为90%,30t硫铁矿能生产98%的硫酸多少吨?
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】1.(1)已知20℃时的溶解度:Na2CO3:S=21.2g; NaHCO3:S=9.6g。则20℃恒温条件下向121.2g饱和碳酸钠溶液中通入足量的CO2气体,理论上可以析出NaHCO3__________ g(小数点后保留1位)
(2)向500mL KOH溶液中缓慢通入一定量的CO2气体,充分反应后,在减压低温下蒸发溶液,得到白色固体。若通入CO2气体为2.24L(标准状况下),得到11.9g的白色固体。则所用的KOH溶液的物质的量浓度为______ mol/L。
(3)将一定质量的钠加入到89g水中,完全反应后的溶液为100g,则该溶液的质量分数为________
(4)现有甲、乙两瓶无色溶液,已知它们可能是AlCl3溶液和NaOH溶液.现做如下实验:
① 取440mL甲与120mL乙反应,产生1.56g沉淀;
② 取440mL乙与120mL甲反应,也产生1.56g沉淀;
③ 取120mL甲溶液与400mL乙溶液反应,则产生3.12g沉淀;
通过必要的计算和推理判定:
甲溶液为________ 溶液,其物质的量浓度为__________ mol·L-1;
乙溶液为_______ 溶液,其物质的量浓度是___________ mol·L-1
(2)向500mL KOH溶液中缓慢通入一定量的CO2气体,充分反应后,在减压低温下蒸发溶液,得到白色固体。若通入CO2气体为2.24L(标准状况下),得到11.9g的白色固体。则所用的KOH溶液的物质的量浓度为
(3)将一定质量的钠加入到89g水中,完全反应后的溶液为100g,则该溶液的质量分数为
(4)现有甲、乙两瓶无色溶液,已知它们可能是AlCl3溶液和NaOH溶液.现做如下实验:
① 取440mL甲与120mL乙反应,产生1.56g沉淀;
② 取440mL乙与120mL甲反应,也产生1.56g沉淀;
③ 取120mL甲溶液与400mL乙溶液反应,则产生3.12g沉淀;
通过必要的计算和推理判定:
甲溶液为
乙溶液为

您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】将a mol的Na2O2和b mol NaHCO3固体混合后,在密闭容器中加热到250℃,让其充分反应。
(1)当剩余固体为Na2CO3,排出气体为O2,H2O时,a:b的值为________ 。
(2)当剩余固体为Na2CO3,NaOH,排出气体为O2时,a:b的值为________ 。
(3)当a:b>1时,剩余固体为________ ,排出气体为________ 。
(4)当排出的O2和H2O为等物质的量时,则a:b的值为________ 。
(1)当剩余固体为Na2CO3,排出气体为O2,H2O时,a:b的值为
(2)当剩余固体为Na2CO3,NaOH,排出气体为O2时,a:b的值为
(3)当a:b>1时,剩余固体为
(4)当排出的O2和H2O为等物质的量时,则a:b的值为
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐2】将1 mol NaHCO3和a mol Na2O2固体混合后,在密闭容器中加热到250℃,让其充分反应,剩余固体为Na2CO3、NaOH,在剩余固体中加入足量6 mol·Lˉ1盐酸。请计算:
(1)加入足量盐酸后产生标准状况下气体体积为________________ L;
(2)固体混合物中Na2O2的物质的量a的取值范围为______________________ 。
(1)加入足量盐酸后产生标准状况下气体体积为
(2)固体混合物中Na2O2的物质的量a的取值范围为
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】不同的卤素原子之间要化合形成一系列化合物,这类化合物叫卤素互化物。现将4.66gBrClx溶于水后,通入足量SO2气体与其反应,生成氢溴酸、盐酸和硫酸。用NaOH溶液将溶液调至中性后加入过量Ba(NO3)2溶液,充分反应后滤去沉淀物,再向溶液中加入过量的AgNO3溶液,最后得15.46g卤化银沉淀。计算确定BrClx中x的值_______ 。
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐2】根据要求,完成下列各题:
(1)把含有 和
和 的混合溶液VL分成两等份,一份加入含a mol
的混合溶液VL分成两等份,一份加入含a mol 的溶液,恰好使
的溶液,恰好使 完全沉淀:另一份加入含bmol NaOH的溶液,恰好使
完全沉淀:另一份加入含bmol NaOH的溶液,恰好使 完全转化为沉淀,则原混合溶液中
完全转化为沉淀,则原混合溶液中 的数目为
的数目为___________ 。
(2)某气态氧化物化学式为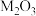 ,在标准状况下,1.52g该氧化物的体积是448mL,则M的摩尔质量为
,在标准状况下,1.52g该氧化物的体积是448mL,则M的摩尔质量为___________ 。
(3)标准状况下,把11.2L 通入一定量的过氧化钠固体中,充分反应后收集到8.96L气体,则这8.96L气体的质量是
通入一定量的过氧化钠固体中,充分反应后收集到8.96L气体,则这8.96L气体的质量是___________ g。
(4)现有下列10种物质:①铜②熔融NaCl③盐酸④液氯⑤ 晶体⑥胆矾⑦碳酸钙⑧
晶体⑥胆矾⑦碳酸钙⑧ ⑨氢氧化铁胶体⑩乙醇;上述物质中属于电解质的有
⑨氢氧化铁胶体⑩乙醇;上述物质中属于电解质的有___________ ,属于非电解质的有___________ ,能导电的有___________ 。(填序号)
(1)把含有
 和
和 的混合溶液VL分成两等份,一份加入含a mol
的混合溶液VL分成两等份,一份加入含a mol 的溶液,恰好使
的溶液,恰好使 完全沉淀:另一份加入含bmol NaOH的溶液,恰好使
完全沉淀:另一份加入含bmol NaOH的溶液,恰好使 完全转化为沉淀,则原混合溶液中
完全转化为沉淀,则原混合溶液中 的数目为
的数目为(2)某气态氧化物化学式为
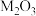 ,在标准状况下,1.52g该氧化物的体积是448mL,则M的摩尔质量为
,在标准状况下,1.52g该氧化物的体积是448mL,则M的摩尔质量为(3)标准状况下,把11.2L
 通入一定量的过氧化钠固体中,充分反应后收集到8.96L气体,则这8.96L气体的质量是
通入一定量的过氧化钠固体中,充分反应后收集到8.96L气体,则这8.96L气体的质量是(4)现有下列10种物质:①铜②熔融NaCl③盐酸④液氯⑤
 晶体⑥胆矾⑦碳酸钙⑧
晶体⑥胆矾⑦碳酸钙⑧ ⑨氢氧化铁胶体⑩乙醇;上述物质中属于电解质的有
⑨氢氧化铁胶体⑩乙醇;上述物质中属于电解质的有
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】甲、乙、丙三组实验中均取30 mL同浓度的盐酸,加入同一种镁铝合金粉末,加入合金的质量与生成气体的体积(已换算成标准状况下)的有关数据如表所示:
(1)甲、乙两组实验中,哪一组盐酸是已完全反应的?___ (填“甲”或“乙”),理由是_______ 。
(2)盐酸的物质的量浓度为________ 。
(3)合金中Mg、Al的物质的量之比为_____________ 。
| 实验序号 | 甲 | 乙 | 丙 |
| 合金的质量/mg | 255 | 385 | 459 |
| 生成气体的体积/mL | 280 | 336 | 336 |
(2)盐酸的物质的量浓度为
(3)合金中Mg、Al的物质的量之比为
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】某复合肥的主要成分有KCl、NH4H2PO4和CO(NH2)2等。测定该复合肥中氮的质量分数的实验步骤如下:
步骤1:准确称取0.5000 g样品于锥形瓶中,加入足量浓硫酸并加热,不再有CO2溢出时,冷却至室温。
步骤2:向锥形瓶中加入100mL蒸馏水,再加入适量的CaCl2溶液,并用NaOH溶液调节溶液近中性,过滤,洗涤,得0.1550 gCa3(PO4)2沉淀和滤液A。
步骤3:向滤液A中加入过量的甲醛溶液,加指示剂,用0. 5000 mol/LNaOH标准溶液滴定至终点,消耗NaOH溶液22.00 mL。 [已知:4 NH4++6HCHO=4H++(CH2)6N4+6H2O]
(1)步骤1中,CO(NH2)2与硫酸反应的化学方程式为____________________ 。
(2)欲使滤液A中c(PO43—)≤4.0×10-6mol/L,应保持溶液中c(Ca2+)≥______________ mol/L[已知KSP[Ca3(PO4)2]=2.0×10-33]。
(3)复合肥样品中N的质量分数为___________ 。
(4)计算复合肥样品中NH4H2PO4和CO(NH2)2的物质的量之比_____________ (写出计算过程)。
步骤1:准确称取0.5000 g样品于锥形瓶中,加入足量浓硫酸并加热,不再有CO2溢出时,冷却至室温。
步骤2:向锥形瓶中加入100mL蒸馏水,再加入适量的CaCl2溶液,并用NaOH溶液调节溶液近中性,过滤,洗涤,得0.1550 gCa3(PO4)2沉淀和滤液A。
步骤3:向滤液A中加入过量的甲醛溶液,加指示剂,用0. 5000 mol/LNaOH标准溶液滴定至终点,消耗NaOH溶液22.00 mL。 [已知:4 NH4++6HCHO=4H++(CH2)6N4+6H2O]
(1)步骤1中,CO(NH2)2与硫酸反应的化学方程式为
(2)欲使滤液A中c(PO43—)≤4.0×10-6mol/L,应保持溶液中c(Ca2+)≥
(3)复合肥样品中N的质量分数为
(4)计算复合肥样品中NH4H2PO4和CO(NH2)2的物质的量之比
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐2】已知黄钠铁矾[NaxFey(SO4)m(OH)n]具有沉淀颗粒大、沉淀速率快、容易过滤等特点。某研究小组先将某废水中Fe2+氧化为Fe3+,再加入Na2SO4使其生成黄钠铁矾而除去。该小组为测定黄钠铁矾的组成,进行了如下实验:
①称取4.850 g样品,加盐酸完全溶解后,配成100.00 mL溶液A;
②量取25.00 mL溶液A,加入足量的KI,用0.2500 mol·L-1Na2S2O3溶液进行滴定(反应为I2+2Na2S2O3=2NaI+Na2S4O6),消耗30.00 mLNa2S2O3溶液至终点。
③另取25.00 mL溶液A,加足量BaCl2溶液充分反应后,过滤、洗涤、干燥后得沉淀1.165 g。
(1)如何证明步骤③中的沉淀已洗涤干净?___________ 。
(2)用Na2S2O3溶液进行滴定时,使用的指示剂为________ ,滴定到终点的颜色变化为_________ 。
(3)通过计算确定黄钠铁矾的化学式_________ (写出计算过程)。
①称取4.850 g样品,加盐酸完全溶解后,配成100.00 mL溶液A;
②量取25.00 mL溶液A,加入足量的KI,用0.2500 mol·L-1Na2S2O3溶液进行滴定(反应为I2+2Na2S2O3=2NaI+Na2S4O6),消耗30.00 mLNa2S2O3溶液至终点。
③另取25.00 mL溶液A,加足量BaCl2溶液充分反应后,过滤、洗涤、干燥后得沉淀1.165 g。
(1)如何证明步骤③中的沉淀已洗涤干净?
(2)用Na2S2O3溶液进行滴定时,使用的指示剂为
(3)通过计算确定黄钠铁矾的化学式
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】Na、Fe、Cu、Al是常见的金属元素,回答下列问题:
(1)一定条件下,4.6g的Na与O2完全反应生成7.2 g产物时失去的电子数为___________ 。
(2)向氯化铜溶液中加入一定量的铁粉和铝粉混合物,充分反应后,下列情况可能出现的是___________ (填字母)。
a.溶液中有Fe3+、Al3+,不溶物为Cu
b.溶液中有Fe2+,不溶物为Cu、Al
c.溶液中有Cu2+、Fe2+、Al3+,不溶物为Cu
d.溶液中有Fe2+、Al3+,不溶物为Cu、Fe
(3)铁的某种氧化物的化学式表示为FexO(x<1),已知铁元素在该氧化物中的质量分数为75%,则x=____________ (精确至0.01)。
(4)将一定质量的铁、铝、铜合金,加入1 L一定物质的量浓度的硝酸中,合金完全溶解,测得溶液中(忽略溶液体积的变化)c(H+)=0.5 mol·L-1,c(Cu2+)=0.3 mol·L-1,c(Al3+)=0.2 mol·L-1,c(NO)=2 mol·L-1,则混合物中铁的质量为___________ g。
(1)一定条件下,4.6g的Na与O2完全反应生成7.2 g产物时失去的电子数为
(2)向氯化铜溶液中加入一定量的铁粉和铝粉混合物,充分反应后,下列情况可能出现的是
a.溶液中有Fe3+、Al3+,不溶物为Cu
b.溶液中有Fe2+,不溶物为Cu、Al
c.溶液中有Cu2+、Fe2+、Al3+,不溶物为Cu
d.溶液中有Fe2+、Al3+,不溶物为Cu、Fe
(3)铁的某种氧化物的化学式表示为FexO(x<1),已知铁元素在该氧化物中的质量分数为75%,则x=
(4)将一定质量的铁、铝、铜合金,加入1 L一定物质的量浓度的硝酸中,合金完全溶解,测得溶液中(忽略溶液体积的变化)c(H+)=0.5 mol·L-1,c(Cu2+)=0.3 mol·L-1,c(Al3+)=0.2 mol·L-1,c(NO)=2 mol·L-1,则混合物中铁的质量为
您最近一年使用:0次



