工业废水中常含有一定量的 ,易被人体吸收积累而导致肝癌。处理工业含铬废水的方法通常是将
,易被人体吸收积累而导致肝癌。处理工业含铬废水的方法通常是将 转化为
转化为 ,再将
,再将 转化为
转化为 沉淀。
沉淀。
(1) 和
和 类似,也是两性氢氧化物,写出
类似,也是两性氢氧化物,写出 的酸式电离方程式:
的酸式电离方程式:_____ 。
(2) 在强碱中可被双氧水氧化为
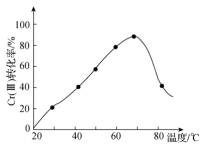
在强碱中可被双氧水氧化为 ,控制其他条件不变,反应温度对
,控制其他条件不变,反应温度对 转化率的影响如图所示。请分析温度超过70℃时,
转化率的影响如图所示。请分析温度超过70℃时, 转化率下降的原因是
转化率下降的原因是_______ 。
(3)溶液中的 与强碱性溶液反应,使
与强碱性溶液反应,使 完全沉淀的
完全沉淀的 为
为_______ {通常认为溶液中离子浓度小于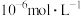 为沉淀完全;
为沉淀完全; 的
的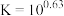 ,
,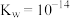 ,
, }。
}。
(4)25℃时,将 的醋酸与
的醋酸与 氢氧化钠等体积混合,反应后溶液恰好显中性,用含a、b式子表示醋酸的电离平衡常数为
氢氧化钠等体积混合,反应后溶液恰好显中性,用含a、b式子表示醋酸的电离平衡常数为_______ 。
(5)标准状况下,将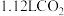 通入
通入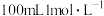 的
的 溶液中,用溶液中微粒的浓度符号完成下列等式:
溶液中,用溶液中微粒的浓度符号完成下列等式: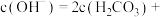
_______ 。
 ,易被人体吸收积累而导致肝癌。处理工业含铬废水的方法通常是将
,易被人体吸收积累而导致肝癌。处理工业含铬废水的方法通常是将 转化为
转化为 ,再将
,再将 转化为
转化为 沉淀。
沉淀。(1)
 和
和 类似,也是两性氢氧化物,写出
类似,也是两性氢氧化物,写出 的酸式电离方程式:
的酸式电离方程式:(2)
 在强碱中可被双氧水氧化为
在强碱中可被双氧水氧化为 ,控制其他条件不变,反应温度对
,控制其他条件不变,反应温度对 转化率的影响如图所示。请分析温度超过70℃时,
转化率的影响如图所示。请分析温度超过70℃时, 转化率下降的原因是
转化率下降的原因是
(3)溶液中的
 与强碱性溶液反应,使
与强碱性溶液反应,使 完全沉淀的
完全沉淀的 为
为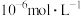 为沉淀完全;
为沉淀完全; 的
的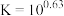 ,
,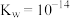 ,
, }。
}。(4)25℃时,将
 的醋酸与
的醋酸与 氢氧化钠等体积混合,反应后溶液恰好显中性,用含a、b式子表示醋酸的电离平衡常数为
氢氧化钠等体积混合,反应后溶液恰好显中性,用含a、b式子表示醋酸的电离平衡常数为(5)标准状况下,将
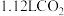 通入
通入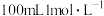 的
的 溶液中,用溶液中微粒的浓度符号完成下列等式:
溶液中,用溶液中微粒的浓度符号完成下列等式: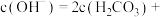
更新时间:2023-03-02 22:30:02
|
相似题推荐
计算题
|
较难
(0.4)
【推荐1】(1)已知某温度时,KW=1.0×10-12 ,Na2CO3溶液的水解常数Kh=2.0×10-3,则当溶液中c(HCO )∶c(CO
)∶c(CO )=2∶1时,试求该溶液的pH=
)=2∶1时,试求该溶液的pH=______ 。
(2)已知25 ℃时,NH3·H2O的电离平衡常数Kb=1.8×10-5,该温度下1 mol·L-1的NH4Cl溶液中c(H+)=____________ mol·L-1。(已知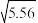 ≈2.36)
≈2.36)
(3)25 ℃时,H2SO3 HSO
HSO +H+的电离常数Ka=1×10-2,则该温度下NaHSO3水解反应的平衡常数Kh=
+H+的电离常数Ka=1×10-2,则该温度下NaHSO3水解反应的平衡常数Kh=________________ ,若向NaHSO3溶液中加入少量的I2,则溶液中 将
将________ (填“增大”“减小”或“不变”)。
(4)已知常温下CN-的水解常数Kh=1.61×10-5。
①常温下,含等物质的量浓度的HCN与NaCN的混合溶液显_____ (填“酸”“碱”或“中”)性,c(CN-)________ (填“>”“<”或“=”)c(HCN)。该溶液中各离子浓度由大到小的顺序为____________ 。
②常温下,若将c mol·L-1盐酸与0.62 mol·L-1KCN溶液等体积混合后恰好得到中性溶液,则c=________ (小数点后保留4位数字)。
 )∶c(CO
)∶c(CO )=2∶1时,试求该溶液的pH=
)=2∶1时,试求该溶液的pH=(2)已知25 ℃时,NH3·H2O的电离平衡常数Kb=1.8×10-5,该温度下1 mol·L-1的NH4Cl溶液中c(H+)=
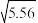 ≈2.36)
≈2.36)(3)25 ℃时,H2SO3
 HSO
HSO +H+的电离常数Ka=1×10-2,则该温度下NaHSO3水解反应的平衡常数Kh=
+H+的电离常数Ka=1×10-2,则该温度下NaHSO3水解反应的平衡常数Kh= 将
将(4)已知常温下CN-的水解常数Kh=1.61×10-5。
①常温下,含等物质的量浓度的HCN与NaCN的混合溶液显
②常温下,若将c mol·L-1盐酸与0.62 mol·L-1KCN溶液等体积混合后恰好得到中性溶液,则c=
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】(1)某温度(t℃)时,水的Kw=1×10-12,则该温度___________ (填“>”“<”或“=”)25℃,其理由是___________ 。
(2)该温度下,c(H+)=1×10-7mol·L-1的溶液呈___________ (填“酸性”“碱性”或“中性”);若该溶液中只存在NaOH溶质,则由H2O电离出来的c(OH-)=___________ mol·L-1。
(3)实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡___________ (填“向左”“向右”或“不”,下同)移动。在新制氯水中加入少量NaCl固体,水的电离平衡___________ 移动。
(4)25℃时,0.1mol·L-1下列物质的溶液,水电离出的c(H+)由大到小的关系是___________ (填序号)。
①HCl②H2SO4③CH3COOH(Ka=1.7×10-5)④NH3·H2O(Kb=1.7×10-5)⑤NaOH⑥Ba(OH)2
(5)25℃时,pH=4的盐酸中水的电离程度___________ pH=10的Ba(OH)2溶液中水的电离程度。
(2)该温度下,c(H+)=1×10-7mol·L-1的溶液呈
(3)实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡
(4)25℃时,0.1mol·L-1下列物质的溶液,水电离出的c(H+)由大到小的关系是
①HCl②H2SO4③CH3COOH(Ka=1.7×10-5)④NH3·H2O(Kb=1.7×10-5)⑤NaOH⑥Ba(OH)2
(5)25℃时,pH=4的盐酸中水的电离程度
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】电解质水溶液中存在电离平衡、水解平衡、溶解平衡等,请回答下列问题。
(1)已知部分弱酸的电离常数如下表:
①0.1mol/L NaCN溶液和0.1mol/L NaHCO3溶液中,c(CN-)______ c(HCO3- )(填“>”、“<”或“=”)。
②将浓度均为0.1mol/L的CH3COONa、NaCN、NaHCO3和Na2CO3溶液分别稀释100倍,pH变化最小的是__________ 。
③将少量CO2通入NaCN溶液,反应的离子方程式是_____ 。
④室温下,—定浓度的CH3COONa溶液pH=9,用离子方程式表示溶液呈碱性的原因是_____ ,溶液中c(CH3COO-)/c(CH3COOH) =___________ 。
⑤室温下,某溶液中存在着CH3COOH(aq)+HCO3-( aq)⇌CH3COO-(aq) +H2CO3(aq),该反应的平衡常数K =___________ 。
⑥室温下,pH =4的CH3COOH与pH =10的CH3COONa溶液中,由水电离出的c(H+)之比_______ 。
(2)已知室温下Cu(OH)2的Ksp=2×10-20,又知室温下某CuSO4溶液中c(Cu2+)=0.02mol/L,如果要生成Cu(OH)2沉淀,则应调整溶液的pH大于___________
(1)已知部分弱酸的电离常数如下表:
| 弱酸 | CH3COOH | HCN | H2CO3 |
| 电离常数(室温) | Ka= 1.8×10-5 | Ka=4.3×10-10 | Ka1=5.0×10-7 Ka2=5.6×10-11 |
①0.1mol/L NaCN溶液和0.1mol/L NaHCO3溶液中,c(CN-)
②将浓度均为0.1mol/L的CH3COONa、NaCN、NaHCO3和Na2CO3溶液分别稀释100倍,pH变化最小的是
③将少量CO2通入NaCN溶液,反应的离子方程式是
④室温下,—定浓度的CH3COONa溶液pH=9,用离子方程式表示溶液呈碱性的原因是
⑤室温下,某溶液中存在着CH3COOH(aq)+HCO3-( aq)⇌CH3COO-(aq) +H2CO3(aq),该反应的平衡常数K =
⑥室温下,pH =4的CH3COOH与pH =10的CH3COONa溶液中,由水电离出的c(H+)之比
(2)已知室温下Cu(OH)2的Ksp=2×10-20,又知室温下某CuSO4溶液中c(Cu2+)=0.02mol/L,如果要生成Cu(OH)2沉淀,则应调整溶液的pH大于
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】水溶液广泛存在于生命体及其赖以生存的环境中。弱电解质的电离平衡、盐类的水解平衡和难溶电解质的沉淀溶解平衡都与日常生活、工农业生产等息息相关。回答下列问题:
(1)25℃时, 溶液呈酸性的原因是
溶液呈酸性的原因是_______ (用离子方程式表示),把 溶液蒸干并灼烧得到的固体产物是
溶液蒸干并灼烧得到的固体产物是_______ (填化学式),该固体产物可用作_______ (填一种常见的用途)。
(2)25℃时,柠檬酸(用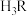 表示)为三元弱酸,其电离常数:
表示)为三元弱酸,其电离常数: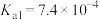 ,
,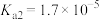 ,
,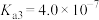 ;电离常数的负对数:
;电离常数的负对数: ,
,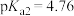 ,
, 。
。
①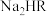 溶液呈
溶液呈_______ (填“酸”、“中”或“碱”)性,原因是_______ (结合计算分析)。
②在含有浓度均为 的
的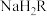 和
和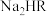 的混合液中,
的混合液中,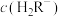
_______ (填“<”、“>”或“=”)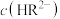 ;
;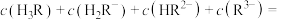
_______ (填写准确数值,下同);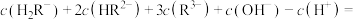
_______ 。
③当 时,溶液的pH=
时,溶液的pH=_______ 。(保留三位有效数字,已知: )
)
(1)25℃时,
 溶液呈酸性的原因是
溶液呈酸性的原因是 溶液蒸干并灼烧得到的固体产物是
溶液蒸干并灼烧得到的固体产物是(2)25℃时,柠檬酸(用
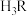 表示)为三元弱酸,其电离常数:
表示)为三元弱酸,其电离常数: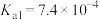 ,
,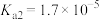 ,
,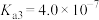 ;电离常数的负对数:
;电离常数的负对数: ,
,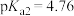 ,
, 。
。①
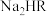 溶液呈
溶液呈②在含有浓度均为
 的
的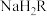 和
和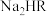 的混合液中,
的混合液中,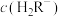
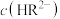 ;
;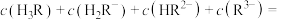
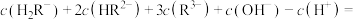
③当
 时,溶液的pH=
时,溶液的pH= )
)
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐2】常温下,如果取0.1mol/LHA溶液与0.1mol/LNaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8。试回答下列问题:
(1)混合溶液pH=8的原因是______________ (用离子方程式表示)
(2)混合溶液中由水电离出的c(OH-)___________ (填“大于”、“等于”或“小于”)0.1mol/LNaOH溶液中由水电离出的c(OH-)
(3)求出混合溶液中下列算式的精确计算结果(填具体数字):
c(Na+)- c(A-)=____________ mol/L, c(OH-)- c(HA)=____________ mol/L
常温下,将PH=2的酸HA溶液与PH=12的NaOH溶液等体积混合后,所得溶液PH_________ 7 (填“大于”、“等于”或“小于”)
(5)已知NH4A溶液为中性,又知HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的PH___________ 7(填“大于”、“等于”或“小于”)。
(1)混合溶液pH=8的原因是
(2)混合溶液中由水电离出的c(OH-)
(3)求出混合溶液中下列算式的精确计算结果(填具体数字):
c(Na+)- c(A-)=
常温下,将PH=2的酸HA溶液与PH=12的NaOH溶液等体积混合后,所得溶液PH
(5)已知NH4A溶液为中性,又知HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的PH
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐3】回答下列问题:
(1)常温下,将pH=9的NaOH溶液稀释1000倍,溶液中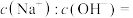
______
(2)常温下,已知醋酸的电离常数为Ka,向100mL0.1mol/L的醋酸溶液中,加入______ mL0.1mol/L的NaOH,可使反应所得的溶液pH=7(用含Ka的式子表达)
(3)常温下,100mLpH=0盐酸和硫酸的混合溶液中加入200mLpH=13的 ,恰好沉淀完全,则原溶液中c(HCl)=
,恰好沉淀完全,则原溶液中c(HCl)=______
(4)常温下,设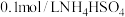 溶液的pH为a,则
溶液的pH为a,则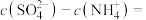
______ (用含a的精确式子表达)
(1)常温下,将pH=9的NaOH溶液稀释1000倍,溶液中
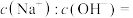
(2)常温下,已知醋酸的电离常数为Ka,向100mL0.1mol/L的醋酸溶液中,加入
(3)常温下,100mLpH=0盐酸和硫酸的混合溶液中加入200mLpH=13的
 ,恰好沉淀完全,则原溶液中c(HCl)=
,恰好沉淀完全,则原溶液中c(HCl)=(4)常温下,设
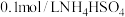 溶液的pH为a,则
溶液的pH为a,则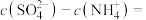
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐1】根据要求,回答下列问题:
(1)某温度下,纯水中的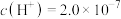 mol·L
mol·L ,则该温度时的水的离子积
,则该温度时的水的离子积
_______ ;保持温度不变,滴入稀盐酸使溶液中的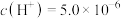 mol·L
mol·L ,则溶液中的
,则溶液中的 为
为_______ mol·L ;
;
(2)将浓度均为0.1 mo/L的 和
和 等体积混合,溶液
等体积混合,溶液 。分析该溶液中离子浓度从大到小依次是:
。分析该溶液中离子浓度从大到小依次是:_______ ;
(3)将 溶液蒸干、灼烧,最后所得的固体的主要成份是
溶液蒸干、灼烧,最后所得的固体的主要成份是_______ ;
(4)物质的量浓度相同的三种盐NaX、NaY、NaZ的溶液,其pH依次为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序是_______ ;
(5)已知:a. ,
, ,
,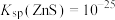 ,
,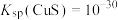
b.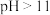 时,
时, 会转化为
会转化为
c.离子浓度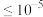 mol/L,即认为其完全沉淀
mol/L,即认为其完全沉淀
①若加入 来沉淀
来沉淀 和
和 ,当溶液中ZnS和CuS共存时,
,当溶液中ZnS和CuS共存时,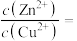
_______ 。
②若加入NaOH溶液来调节pH,使 和
和 完全沉淀,pH应满足的条件为
完全沉淀,pH应满足的条件为_______ 。
(1)某温度下,纯水中的
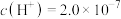 mol·L
mol·L ,则该温度时的水的离子积
,则该温度时的水的离子积
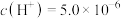 mol·L
mol·L ,则溶液中的
,则溶液中的 为
为 ;
;(2)将浓度均为0.1 mo/L的
 和
和 等体积混合,溶液
等体积混合,溶液 。分析该溶液中离子浓度从大到小依次是:
。分析该溶液中离子浓度从大到小依次是:(3)将
 溶液蒸干、灼烧,最后所得的固体的主要成份是
溶液蒸干、灼烧,最后所得的固体的主要成份是(4)物质的量浓度相同的三种盐NaX、NaY、NaZ的溶液,其pH依次为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序是
(5)已知:a.
 ,
, ,
,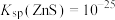 ,
,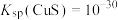
b.
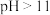 时,
时, 会转化为
会转化为
c.离子浓度
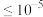 mol/L,即认为其完全沉淀
mol/L,即认为其完全沉淀①若加入
 来沉淀
来沉淀 和
和 ,当溶液中ZnS和CuS共存时,
,当溶液中ZnS和CuS共存时,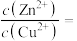
②若加入NaOH溶液来调节pH,使
 和
和 完全沉淀,pH应满足的条件为
完全沉淀,pH应满足的条件为
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐2】回答下列问题:
(1)已知25℃, 的
的 ,
, 的
的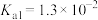 ,
, 。若氨水的浓度为
。若氨水的浓度为 ,溶液中的
,溶液中的
_______  ,将
,将 通入该氨水中,当
通入该氨水中,当 降至
降至 时,溶液中的
时,溶液中的
_______ 。
(2) 可以被
可以被 溶液捕获。若所得溶液
溶液捕获。若所得溶液 ,
, 主要转化为
主要转化为_______ (写离子符号);若所得溶液 ,溶液
,溶液
_______ 。(室温下, 的
的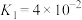 ;
; )
)
(3)在25℃下,将 的氨水与
的氨水与 的盐酸等体积混合,反应平衡时溶液中
的盐酸等体积混合,反应平衡时溶液中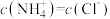 ,则溶液显性
,则溶液显性_______ (填“酸”、“碱”或“中”);用含a的代数式表示 的电离常数
的电离常数
_______ 。
(4)常温下,向一定体积的
 溶液中滴加等体积的
溶液中滴加等体积的 的盐酸使溶液呈中性(不考虑盐酸和醋酸的挥发),用含a和b的代数式表示醋酸的电离常数
的盐酸使溶液呈中性(不考虑盐酸和醋酸的挥发),用含a和b的代数式表示醋酸的电离常数
_______ 。
(5)已知 ,若向
,若向
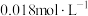 的
的 溶液中加入
溶液中加入
 的盐酸,混合后溶液中的
的盐酸,混合后溶液中的 的浓度为
的浓度为_______  ,pH为
,pH为_______ 。
(1)已知25℃,
 的
的 ,
, 的
的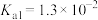 ,
, 。若氨水的浓度为
。若氨水的浓度为 ,溶液中的
,溶液中的
 ,将
,将 通入该氨水中,当
通入该氨水中,当 降至
降至 时,溶液中的
时,溶液中的
(2)
 可以被
可以被 溶液捕获。若所得溶液
溶液捕获。若所得溶液 ,
, 主要转化为
主要转化为 ,溶液
,溶液
 的
的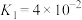 ;
; )
)(3)在25℃下,将
 的氨水与
的氨水与 的盐酸等体积混合,反应平衡时溶液中
的盐酸等体积混合,反应平衡时溶液中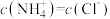 ,则溶液显性
,则溶液显性 的电离常数
的电离常数
(4)常温下,向一定体积的

 溶液中滴加等体积的
溶液中滴加等体积的 的盐酸使溶液呈中性(不考虑盐酸和醋酸的挥发),用含a和b的代数式表示醋酸的电离常数
的盐酸使溶液呈中性(不考虑盐酸和醋酸的挥发),用含a和b的代数式表示醋酸的电离常数
(5)已知
 ,若向
,若向
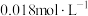 的
的 溶液中加入
溶液中加入
 的盐酸,混合后溶液中的
的盐酸,混合后溶液中的 的浓度为
的浓度为 ,pH为
,pH为
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】按要求回答下列问题。
(1)已知25℃时Ksp[Fe(OH)3]=4.0×10-38,此温度下若在实验室中配制5 mol·L-1 100 mL FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加入_______ mL 2 mol·L-1的盐酸(忽略加入盐酸体积)。
(2)CaSO3溶液与CaCl2溶液混合会生成难溶的CaSO3(Ksp=3.1×10-7),现将等体积的CaCl2溶液与Na2SO3溶液混合,若混合前Na2SO3溶液的浓度为2×10-3 mol·L-1,则生成沉淀所需CaCl2溶液的最小浓度为_______ 。
(3)汽车尾气中的SO2可用石灰水来吸收,生成亚硫酸钙浊液。常温下,测得某纯CaSO3与水形成的浊液pH为9,已知Ka1(H2SO3)=1.8×10-2,Ka2(H2SO3)=6.0×10-9,忽略 的第二步水解,则Ksp(CaSO3)=
的第二步水解,则Ksp(CaSO3)=_______ 。
(4)在某温度下,Ksp(FeS)=6.25×10-18,FeS饱和溶液中 c(H+)与c(S2-)之间存在关系:c2(H+)·c(S2-)=1.0×10-22,为了使溶液里c(Fe2+) 达到1 mol·L-1,现将适量FeS投入其饱和溶液中,应调节溶液中的c(H+)约为_______ 。
(1)已知25℃时Ksp[Fe(OH)3]=4.0×10-38,此温度下若在实验室中配制5 mol·L-1 100 mL FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加入
(2)CaSO3溶液与CaCl2溶液混合会生成难溶的CaSO3(Ksp=3.1×10-7),现将等体积的CaCl2溶液与Na2SO3溶液混合,若混合前Na2SO3溶液的浓度为2×10-3 mol·L-1,则生成沉淀所需CaCl2溶液的最小浓度为
(3)汽车尾气中的SO2可用石灰水来吸收,生成亚硫酸钙浊液。常温下,测得某纯CaSO3与水形成的浊液pH为9,已知Ka1(H2SO3)=1.8×10-2,Ka2(H2SO3)=6.0×10-9,忽略
 的第二步水解,则Ksp(CaSO3)=
的第二步水解,则Ksp(CaSO3)=(4)在某温度下,Ksp(FeS)=6.25×10-18,FeS饱和溶液中 c(H+)与c(S2-)之间存在关系:c2(H+)·c(S2-)=1.0×10-22,为了使溶液里c(Fe2+) 达到1 mol·L-1,现将适量FeS投入其饱和溶液中,应调节溶液中的c(H+)约为
您最近一年使用:0次




