丙烷燃烧可以通过以下两种途径:
途径Ⅰ:
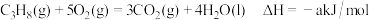
途径II:

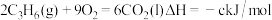
 (a、b、c、d均为正值)
(a、b、c、d均为正值)
请回答下列问题:
(1)判断等量的丙烷通过两种途径放出的热量,途径I放出的热量____________ 填“大于”、“等于”或“小于”)途径II放出的热量。
(2)在 的反应中,反应物具有的总能量
的反应中,反应物具有的总能量___________ (填“大于”、“等于”或“小于”)生成物具有的总能量。
(3)b与a、c、d的数学关系式是_________
(4)已知25℃、101 kPa下,
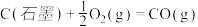 ;
; 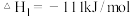
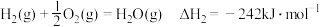
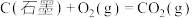
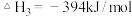
请写出一氧化碳与水蒸气作用生成氢气和二氧化碳的热化学方程式:__________
途径Ⅰ:
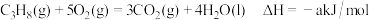
途径II:

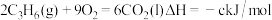
 (a、b、c、d均为正值)
(a、b、c、d均为正值)请回答下列问题:
(1)判断等量的丙烷通过两种途径放出的热量,途径I放出的热量
(2)在
 的反应中,反应物具有的总能量
的反应中,反应物具有的总能量(3)b与a、c、d的数学关系式是
(4)已知25℃、101 kPa下,
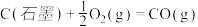 ;
; 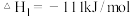
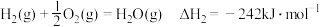
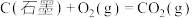
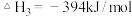
请写出一氧化碳与水蒸气作用生成氢气和二氧化碳的热化学方程式:
更新时间:2021-01-14 11:13:14
|
相似题推荐
计算题
|
较易
(0.85)
【推荐1】天然气的主要成分为CH4,一般还含有C2H6等烃类,是重要的燃料和化工原料。乙烷在一定条件可发生如下反应:C2H6(g)=C2H4(g)+H2(g) ∆H,相关物质的燃烧热数据如下表所示:
∆H=_______ kJ·mol−1。
| 物质 | C2H6(g) | C2H4(g) | H2(g) |
| 燃烧热∆H/(kJ·mol−1) | −1560 | −1411 | -286 |
∆H=
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐2】氮氧化物( )是电厂排放的主要污染物之一、
)是电厂排放的主要污染物之一、
(1)工业上采用氨脱硝处理后排放,原理如下:
①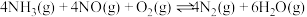
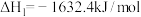
②
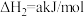
当反应温度过高时, 发生氧化反应:
发生氧化反应:
③
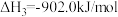
反应②中的
_______ 。
(2)甲醇既是重要的化工原料,又可作为燃料,利用合成气(主要成分为 、
、 和
和 )在催化剂作用下合成甲醇。发生的主要反应如下:
)在催化剂作用下合成甲醇。发生的主要反应如下:
④

⑤

⑥
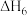
已知反应④中相关化学键的键能数据如表所示:
由此计算
_______  ;已知
;已知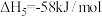 ,则
,则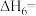
_______  。
。
 )是电厂排放的主要污染物之一、
)是电厂排放的主要污染物之一、(1)工业上采用氨脱硝处理后排放,原理如下:
①
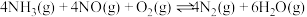
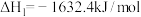
②

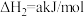
当反应温度过高时,
 发生氧化反应:
发生氧化反应:③

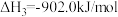
反应②中的

(2)甲醇既是重要的化工原料,又可作为燃料,利用合成气(主要成分为
 、
、 和
和 )在催化剂作用下合成甲醇。发生的主要反应如下:
)在催化剂作用下合成甲醇。发生的主要反应如下:④


⑤


⑥

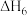
已知反应④中相关化学键的键能数据如表所示:
| 化学键 |  |  |  |  |  |
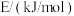 | 436 | 351 | 1076 | 463 | 413 |

 ;已知
;已知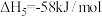 ,则
,则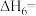
 。
。
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐1】采用科学技术减少氮氧化物等物质的排放可促进社会主义生态文明建设。
用CH4催化还原氮氧化物的相关热化学方程式如下:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(1)∆H=-662kJ•mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(l)∆H=-1248kJ•mol-1
反应CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(l)∆H=_____ kJ•mol-1
用CH4催化还原氮氧化物的相关热化学方程式如下:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(1)∆H=-662kJ•mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(l)∆H=-1248kJ•mol-1
反应CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(l)∆H=
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐2】下图是2SO2(g) + O2(g) = 2SO3(g)反应过程中的能量变化, 已知1mol SO2(g)完全氧化为1mol SO3的ΔH= —99kJ·mol-1,请回答下列问题:

(1)图中A、C分别表的物质是__________________ 、________________ ,E的大小对该反应的焓变有无影响?___________ (填“有”或“无”)(该反应通常用V2O5作催化剂,加V2O5会使图中B点降低。);
(2)图中△H =_____________ kJ·mol-1;
(3)已知:S(s) + O2(g) = SO2(g) ΔH=-296 kJ·mol-1,计算由3 mol S(s)与氧气反应生成3 molSO3(g)的△H =______________ 。

(1)图中A、C分别表的物质是
(2)图中△H =
(3)已知:S(s) + O2(g) = SO2(g) ΔH=-296 kJ·mol-1,计算由3 mol S(s)与氧气反应生成3 molSO3(g)的△H =
您最近一年使用:0次
【推荐3】(1)若适量的N2和O2完全反应,每生成23g NO2需要吸收16.95kJ热量。其热化学方程式为_ 。
(2)甲醇(CH3OH)的燃烧热为725.8kJ/mol,写出甲醇的燃烧热的热化学方程式_____ 。
(3)已知H-H键的键能为436kJ·mol-1,Cl-Cl键的键能为243 kJ·mol-1,H-Cl键的键能为431kJ·mol-1,则H2(g)+Cl2(g)=2HCl(g)的反应热(ΔH)等于_____ kJ·mol-1
(4)研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s)⇌NaNO3(s)+ClNO(g) K1 ΔH1
2NO(g)+Cl2(g)⇌2ClNO(g) K2 ΔH2
则4NO2(g)+2NaCl(s)⇌2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=___ (用含有K1、K2的式子表示);其反应热为______ (用含有ΔH1、ΔH2的式子表示)。
(2)甲醇(CH3OH)的燃烧热为725.8kJ/mol,写出甲醇的燃烧热的热化学方程式
(3)已知H-H键的键能为436kJ·mol-1,Cl-Cl键的键能为243 kJ·mol-1,H-Cl键的键能为431kJ·mol-1,则H2(g)+Cl2(g)=2HCl(g)的反应热(ΔH)等于
(4)研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s)⇌NaNO3(s)+ClNO(g) K1 ΔH1
2NO(g)+Cl2(g)⇌2ClNO(g) K2 ΔH2
则4NO2(g)+2NaCl(s)⇌2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=
您最近一年使用:0次

 O2(g)=CO(g)
O2(g)=CO(g)

