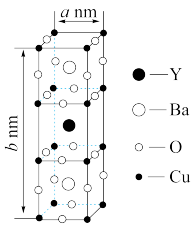
1 . 已知:钇钡铜氧晶体的晶胞是一个长方体(如图所示),其晶胞参数分别为a nm、bnm,阿伏加 德罗常数的值为NA。则该晶体的密度为________ g /cm3(列出计算式即可)。(原子量:Y-89 Ba-137 Cu-64 O-16)

您最近一年使用:0次
解题方法
2 . 常温下一种烷烃A和一种单烯烃B组成混合气体,A或B分子最多只含有4个碳原子,且B分子的碳原子数比A分子的多。
(1)将该混合气体1L充分燃烧在同温、同压下得2.5LCO2,试推断原混合气体A中和B所有可能的组合及其体积比___ 。
(2)120℃时取1L该混合气体与9L氧气混合,充分燃烧后,当恢复到120℃和燃烧前的压强时,体积增大6.25%,试通过计算确定混合气中各成分的分子式___ 。
(1)将该混合气体1L充分燃烧在同温、同压下得2.5LCO2,试推断原混合气体A中和B所有可能的组合及其体积比
(2)120℃时取1L该混合气体与9L氧气混合,充分燃烧后,当恢复到120℃和燃烧前的压强时,体积增大6.25%,试通过计算确定混合气中各成分的分子式
您最近一年使用:0次
解题方法
3 . 400K、 时,2L烃A的蒸气能在VL氧气中完全燃烧,反应后体积增至
时,2L烃A的蒸气能在VL氧气中完全燃烧,反应后体积增至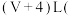 体积在同前的条件下测定
体积在同前的条件下测定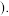 请回答:
请回答:
(1)烃A在组成上应满足的条件是______ .
(2)当 时,该烃可能的分子式为
时,该烃可能的分子式为______ .
(3)若A在常温常压下为气态,V的取值范围是______ .
 时,2L烃A的蒸气能在VL氧气中完全燃烧,反应后体积增至
时,2L烃A的蒸气能在VL氧气中完全燃烧,反应后体积增至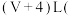 体积在同前的条件下测定
体积在同前的条件下测定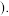 请回答:
请回答:(1)烃A在组成上应满足的条件是
(2)当
 时,该烃可能的分子式为
时,该烃可能的分子式为(3)若A在常温常压下为气态,V的取值范围是
您最近一年使用:0次
解题方法
4 . 将5.1 g镁铝合金溶于60 mL 5.0mol·L H
H SO
SO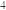 溶液中,完全溶解后再加入a mL10.0 mol·L
溶液中,完全溶解后再加入a mL10.0 mol·L 的NaOH溶液,此时溶液中的Mg
的NaOH溶液,此时溶液中的Mg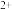 、Al
、Al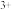 恰好完全沉淀,再继续滴加5 mL该NaOH溶液,得到的沉淀质量为9.7 g。
恰好完全沉淀,再继续滴加5 mL该NaOH溶液,得到的沉淀质量为9.7 g。
(1)当加入a=_________ mLNaOH溶液时,可使溶液中的Mg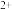 和Al
和Al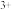 恰好完全沉淀。沉淀的最大值为
恰好完全沉淀。沉淀的最大值为__________ g。
(2)计算合金溶于硫酸时所产生的氢气在标准状况下的体积___________ 。(写出计算过程)
 H
H SO
SO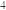 溶液中,完全溶解后再加入a mL10.0 mol·L
溶液中,完全溶解后再加入a mL10.0 mol·L 的NaOH溶液,此时溶液中的Mg
的NaOH溶液,此时溶液中的Mg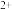 、Al
、Al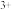 恰好完全沉淀,再继续滴加5 mL该NaOH溶液,得到的沉淀质量为9.7 g。
恰好完全沉淀,再继续滴加5 mL该NaOH溶液,得到的沉淀质量为9.7 g。(1)当加入a=
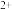 和Al
和Al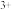 恰好完全沉淀。沉淀的最大值为
恰好完全沉淀。沉淀的最大值为(2)计算合金溶于硫酸时所产生的氢气在标准状况下的体积
您最近一年使用:0次
2019·广东广州·一模
解题方法
5 . 在标准状况下进行甲、乙、丙三组实验。三组实验各取同浓度的盐酸30mL,加入同一种镁铝合金粉末,产生气体。有关数据列表如下(气体体积均为标准状况下测得):
(1)乙组实验中,盐酸_____________ (填“过量”、“适量”或“不足量”),理由是_________ 。
(2)要计算盐酸的物质的量浓度,题中可做计算依据的是____ 。
(3)合金中Mg、Al的物质的量之比为_________________ 。
(4)在丙组实验后,向容器中加入1mol/L的NaOH溶液,能使合金中的铝恰好溶解,不形成铝的沉淀,并使Mg2+刚好沉淀完全,求所加NaOH溶液的体积。(写出计算过程)_____________
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 255 | 385 | 459 |
| 气体体积/mL | 280 | 336 | 336 |
(1)乙组实验中,盐酸
(2)要计算盐酸的物质的量浓度,题中可做计算依据的是
(3)合金中Mg、Al的物质的量之比为
(4)在丙组实验后,向容器中加入1mol/L的NaOH溶液,能使合金中的铝恰好溶解,不形成铝的沉淀,并使Mg2+刚好沉淀完全,求所加NaOH溶液的体积。(写出计算过程)
您最近一年使用:0次
2019·广东广州·一模
解题方法
6 . 将某有机物样品3.0g通入足量的氧气后充分燃烧,在120℃条件下将燃烧后的气体通入足量的浓H2SO4中,浓H2SO4增重1.8g,然后将气体再通入足量的氢氧化钡溶液中,可得到沉淀19.7g(不考虑溶解的沉淀物),此时还有标准状况下的气体2.24L,该气体能用于抢救危重病人。实验测得该有机物蒸气的密度是相同条件下氦气的15倍。求该有机物的分子式和通入氧气的总体积(标准状况)?____________
您最近一年使用:0次
解题方法
7 . 将5.1g镁铝合金溶于600mL0.5mol·L-1H2SO4溶液中,完全溶解后再加入1.0mol·L-1的NaOH溶液,得到沉淀的质量为13.6g,继续滴加NaOH溶液时则沉淀会减少。
(1)当加入__ mLNaOH溶液时,可使溶解在硫酸中的Mg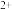 和Al
和Al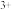 恰好完全沉淀。
恰好完全沉淀。
(2)计算合金溶于硫酸时所产生的氢气在标准状况下的体积。(列出算式)___
(1)当加入
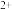 和Al
和Al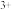 恰好完全沉淀。
恰好完全沉淀。(2)计算合金溶于硫酸时所产生的氢气在标准状况下的体积。(列出算式)
您最近一年使用:0次
8 . 臭氧(O3)能与KI溶液反应,生成氧气等。在反应后的溶液中滴入酚酞变为红色。若滴入淀粉则变为蓝色。为测定环境中空气的臭氧含量,将0℃、1.01×105Pa的空气33.6m3通过KI溶液,使反应完全,在所得溶液中用0.0100mol·L-1的Na2S2O3溶液60.0mL恰好滴定达终点,反应为:2Na2S2O3+I2→Na2S4O6+2NaI
(1)臭氧通入KI溶液中的化学方程式是________ ,每消耗1molO3,转移___ mole-。
(2)计算大气中臭氧的体积分数___ 。(写出计算过程)
(1)臭氧通入KI溶液中的化学方程式是
(2)计算大气中臭氧的体积分数
您最近一年使用:0次
9 . 0.80gCuSO4•5H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如下图所示。
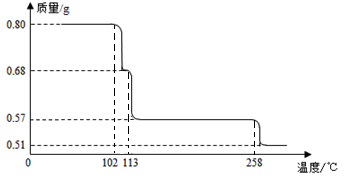
请回答下列问题:
(1)试确定200℃时固体物质的化学式______________ (要求写出推断过程);
(2)取270℃所得样品,于570℃灼烧得到的主要产物是黑色粉末和一种氧化性气体,该反应的化学方程式为______________ 。把该黑色粉末溶解于稀硫酸中,经浓缩、冷却,有晶体析出,该晶体的化学式为_________ ,其存在的最高温度是_____________ ;
(3)上述氧化性气体与水反应生成一种化合物,该化合物的浓溶液与Cu在加热时发生反应的化学方程式为________________ ;
(4)在0.10mol·L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=________________ mol·L-1(Ksp[Cu(OH)2]=2.2×10-20)。若在0.1mol·L-1硫酸铜溶液中通入过量H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的H+浓度是_______________ mol·L-1。

请回答下列问题:
(1)试确定200℃时固体物质的化学式
(2)取270℃所得样品,于570℃灼烧得到的主要产物是黑色粉末和一种氧化性气体,该反应的化学方程式为
(3)上述氧化性气体与水反应生成一种化合物,该化合物的浓溶液与Cu在加热时发生反应的化学方程式为
(4)在0.10mol·L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=
您最近一年使用:0次
2019-01-30更新
|
1974次组卷
|
5卷引用:2017届广东省华侨中学高三上学期摸底考试理综化学试卷
2017届广东省华侨中学高三上学期摸底考试理综化学试卷2011年普通高等学校招生全国统一考试化学卷(新课标)(已下线)2012届陕西省兴平市秦岭中学高三上学期期末练习化学试卷(已下线)2014陕西省西安铁一中、铁一中国际校高三下一模化学试卷黑龙江嫩江市高级中学2021届高三上学期第二次月考化学试题
10 . 将一定质量的铁粉加入装有100 mL某浓度稀硝酸的容器中充分反应。试回答:
(1)容器中剩余mg铁粉,收集到NO气体448 mL(标准状况下)。
①所得溶液中溶质的化学式为__________ 。
②原稀硝酸的物质的量浓度为__________ 。
(2)向(1)中所得的固液混合物中逐滴滴加稀硫酸至刚好不再产生遇空气变成红棕色的气体为止,此时容器中剩余铁粉ng。
①此时溶液中溶质的化学式为__________ 。
②m-n的值为_______ (精确到0.1)。
(1)容器中剩余mg铁粉,收集到NO气体448 mL(标准状况下)。
①所得溶液中溶质的化学式为
②原稀硝酸的物质的量浓度为
(2)向(1)中所得的固液混合物中逐滴滴加稀硫酸至刚好不再产生遇空气变成红棕色的气体为止,此时容器中剩余铁粉ng。
①此时溶液中溶质的化学式为
②m-n的值为
您最近一年使用:0次
2018-04-22更新
|
389次组卷
|
6卷引用:2019年广东省汕头市高三第一次模拟考试化学试题
2019年广东省汕头市高三第一次模拟考试化学试题2015-2016学年青海省平安县第一高中高一入学化学试卷2016-2017学年四川省资阳中学高一下学期3月月考化学试卷辽宁省六校协作体2017-2018学年高一下学期开学考试化学试题甘肃省武威市第六中学2017-2018学年高一下学期第一次学段考试(理)化学试题(已下线)3.3.3 硝酸的性质 人类活动对氮循环和环境的影响练习(2)——《高中新教材同步备课》(鲁科版 必修第一册)



