名校
1 . 完成下列问题
(1)常温下,某溶液由水电离出的c(H+)=10-12 mol·L-1,则该溶液的pH为_______ 。
(2)某温度下,纯水中c(H+)=5.0×10-7 mol·L-1,则该温度下的KW=_______ ,若温度不变,0.005 mol·L-1的H2SO4溶液中,由水电离出的c(H+)=_______ 。
(3)某温度(t℃)时,测得0.01mol•L-1的NaOH溶液的pH=13,请回答下列问题:该温度下水的Kw=_______ ;此温度下,将pH=a的NaOH溶液VaL与pH=b的H2SO4溶液VbL混合(忽略体积变化),若所得混合液为中性,且a=12,b=2,则Va:Vb=_______ 。
(4)25℃时,将0.1mol·L-1 NaOH溶液与0.06mol·L-1的H2SO4溶液等体积混合,(忽略混合后体积的变化),求所得溶液的pH为_______ 。
(5)将pH=5的H2SO4稀释1000倍后,c(H+):c(SO )约为
)约为_______ 。
(1)常温下,某溶液由水电离出的c(H+)=10-12 mol·L-1,则该溶液的pH为
(2)某温度下,纯水中c(H+)=5.0×10-7 mol·L-1,则该温度下的KW=
(3)某温度(t℃)时,测得0.01mol•L-1的NaOH溶液的pH=13,请回答下列问题:该温度下水的Kw=
(4)25℃时,将0.1mol·L-1 NaOH溶液与0.06mol·L-1的H2SO4溶液等体积混合,(忽略混合后体积的变化),求所得溶液的pH为
(5)将pH=5的H2SO4稀释1000倍后,c(H+):c(SO
 )约为
)约为
您最近一年使用:0次
2023-03-04更新
|
600次组卷
|
2卷引用:广东省湛江市第二十一中学2022-2023学年高二上学期期中考试化学试题
名校
解题方法
2 . 回答下列问题
(1)在25℃,101kpa下,1g甲醇( )燃烧生成
)燃烧生成 和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为
和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为___________ 。
(2)已知几种化学键的键能数据如表所示:
请写出氨气与溴蒸气反应的热化学方程式:___________ 。
(3)已知:
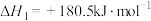

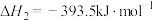
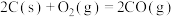
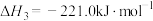
若某反应的平衡常数表达式为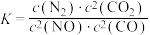 ,请写出此反应的热化学方程式
,请写出此反应的热化学方程式___________ 。
(4)根据图示信息写出热化学方程式:___________ 。
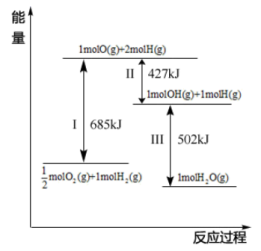
(5)已知:C(s)、CO(g)和 完全燃烧的热化学方程式分别为
完全燃烧的热化学方程式分别为




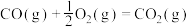
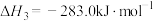
请你根据以上数据,写出C(s)与水蒸气反应生成CO和 的热化学方程式:
的热化学方程式:___________ 。
(1)在25℃,101kpa下,1g甲醇(
 )燃烧生成
)燃烧生成 和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为
和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为(2)已知几种化学键的键能数据如表所示:
| 化学键 | N—H |  | Br—Br | H—Br |
键能/ | 391 | 946 | 194 | 366 |
(3)已知:

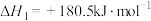

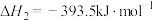
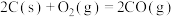
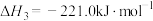
若某反应的平衡常数表达式为
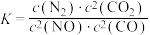 ,请写出此反应的热化学方程式
,请写出此反应的热化学方程式(4)根据图示信息写出热化学方程式:

(5)已知:C(s)、CO(g)和
 完全燃烧的热化学方程式分别为
完全燃烧的热化学方程式分别为



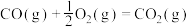
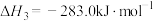
请你根据以上数据,写出C(s)与水蒸气反应生成CO和
 的热化学方程式:
的热化学方程式:
您最近一年使用:0次
解题方法
3 . 现将2.3克的金属钠投入到过量水中,完全反应,按照下列要求进行计算(可能用到的相对原子质量:H—1,O—16,Na—23)
(1)生成的氢气质量为多少?___________
(2)若最终有100克溶液,此时氢氧化钠的质量分数为多少?___________
(1)生成的氢气质量为多少?
(2)若最终有100克溶液,此时氢氧化钠的质量分数为多少?
您最近一年使用:0次
解题方法
4 . 回答下列问题。(lg2=0.3、lg5=0.7)
(1)25℃时,0.01mol/L的NaOH溶液的pH=_____ ;由水电离出的c(H+)=_____ mol/L。
(2)25℃时,pH=2的盐酸与pH=5的盐酸等体积混合后溶液的pH=_____ 。
(3)25℃时,将10mLpH=2醋酸溶液稀释到1000mL后溶液的pH_____ 4(填“大于”“小于”或“等于”)。
(4)某温度下纯水中c(H+)=4×10-7mol/L,则此时溶液中的c(OH-)=_____ mol/L。
(5)某温度时,Ksp[AgI]=9.0×10-16,求AgI饱和溶液中c(Ag+)=_____ mol/L。
(1)25℃时,0.01mol/L的NaOH溶液的pH=
(2)25℃时,pH=2的盐酸与pH=5的盐酸等体积混合后溶液的pH=
(3)25℃时,将10mLpH=2醋酸溶液稀释到1000mL后溶液的pH
(4)某温度下纯水中c(H+)=4×10-7mol/L,则此时溶液中的c(OH-)=
(5)某温度时,Ksp[AgI]=9.0×10-16,求AgI饱和溶液中c(Ag+)=
您最近一年使用:0次
解题方法
5 . 回答下列问题
(1)将Cl2通入KOH溶液,反应后得到KCl、 KClO 、KClO3的混合溶液(无其它溶质),经测定KClO和KClO3的个数之比为9:1,则Cl2和KOH溶液反应时,被还原和被氧化的Cl原子的个数之比为_______________ ,参加反应的Cl2和KOH个数之比为_______ 。
(2)Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,NaClO被还原成NaCl,若Na2Sx与NaClO的个数之比为1∶16,则x的值为_______________ 。
(1)将Cl2通入KOH溶液,反应后得到KCl、 KClO 、KClO3的混合溶液(无其它溶质),经测定KClO和KClO3的个数之比为9:1,则Cl2和KOH溶液反应时,被还原和被氧化的Cl原子的个数之比为
(2)Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,NaClO被还原成NaCl,若Na2Sx与NaClO的个数之比为1∶16,则x的值为
您最近一年使用:0次
6 . 用NA表示阿伏加德罗常数的值。则:
(1)0.5molCO2的质量为________ ,其中含有______ 个CO2分子,共有______ 个原子,共有______ 个电子。
(2)质量都是100g的H2S、CH4、CO2、N2四种气体中,在相同条件下体积最小的是_______ ,含有原子数目最多的是_______ 。
(3)在标准状况下,由CO和CO2组成的混合气体为4.48L,质量为7.2g,此混合物中C和O原子个数比是___________ 。
(4)欲配制 100mL 1mol/L CuSO4溶液,需称量CuSO4·5H2O_______ g 。
(5)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中的还原剂是_________________ ,氧化产物是___________ ,每生成1 mol Na2FeO4转移_______ mol电子。
(1)0.5molCO2的质量为
(2)质量都是100g的H2S、CH4、CO2、N2四种气体中,在相同条件下体积最小的是
(3)在标准状况下,由CO和CO2组成的混合气体为4.48L,质量为7.2g,此混合物中C和O原子个数比是
(4)欲配制 100mL 1mol/L CuSO4溶液,需称量CuSO4·5H2O
(5)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中的还原剂是
您最近一年使用:0次
解题方法
7 . 填空。
(1)已知乙炔(C2H2)气体的燃烧热为ΔH=-1299.6kJ·mol-1,请写出表示乙炔燃烧热的热化学方程式_______ 。
(2)已知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-560kJ·mol-l;
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ·mol-1;
①若用标准状况下4.48LCH4还原NO2生成N2,反应中转移的电子总数为_______ ,(用NA表示阿伏加德罗常数值),放出的热量为_______ kJ。
②若1molCH4还原NO2时放出的热量为710kJ,则生成的N2和NO的物质的量之比_______ 。
(1)已知乙炔(C2H2)气体的燃烧热为ΔH=-1299.6kJ·mol-1,请写出表示乙炔燃烧热的热化学方程式
(2)已知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-560kJ·mol-l;
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ·mol-1;
①若用标准状况下4.48LCH4还原NO2生成N2,反应中转移的电子总数为
②若1molCH4还原NO2时放出的热量为710kJ,则生成的N2和NO的物质的量之比
您最近一年使用:0次
名校
8 . 完成下列问题
(1)某温度(t ℃)时水中的离子浓度图象如下图,a点离子积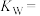
_______ ;该温度下, 的NaOH与
的NaOH与 的
的 等体积混合,溶液显
等体积混合,溶液显_______ 性。

(2)已知室温下, 的电离常数
的电离常数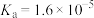 ,若初始时,醋酸中
,若初始时,醋酸中 的浓度为
的浓度为 ,则达到电离平衡时溶液中的
,则达到电离平衡时溶液中的 为
为_______ 。向其中加入少量 固体,当固体溶解后,测得溶液pH
固体,当固体溶解后,测得溶液pH_______ (填“增大”、“减小”或“不变”)。
(1)某温度(t ℃)时水中的离子浓度图象如下图,a点离子积
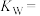
 的NaOH与
的NaOH与 的
的 等体积混合,溶液显
等体积混合,溶液显
(2)已知室温下,
 的电离常数
的电离常数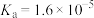 ,若初始时,醋酸中
,若初始时,醋酸中 的浓度为
的浓度为 ,则达到电离平衡时溶液中的
,则达到电离平衡时溶液中的 为
为 固体,当固体溶解后,测得溶液pH
固体,当固体溶解后,测得溶液pH
您最近一年使用:0次
名校
解题方法
9 . 将某碳酸钠和碳酸氢钠混合物2.43g加热到质量不再变化时,剩余物质的质量为2.12g,求:
(1)写出加热过程中发生反应的化学方程式_______ 。
(2)碳酸氢钠的质量为_______ 克?
(3)碳酸钠的质量分数为_______ (保留三位有效数字)?
(1)写出加热过程中发生反应的化学方程式
(2)碳酸氢钠的质量为
(3)碳酸钠的质量分数为
您最近一年使用:0次
2022-11-19更新
|
292次组卷
|
3卷引用:广东省汕尾华大实验学校2022-2023学年高一上学期12月月考化学试题
解题方法
10 . 2020 年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性。其中含氯消毒剂在生产生活中有着广泛的用途。
(1)①写出实验室中制取氯气的离子方程式___________ ;
②已知KMnO4与浓盐酸反应的化学方程式如下,该反应也可以用来制取氯气:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
15.8 g KMnO4能和_____ mol HCl发生上述反应、产生的Cl2在标准状况下的体积为___________ L;
③实验室还可以利用如下反应制取氯气:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。若制取标准状况下6.72 L氯气,反应过程中转移电子的物质的量为___________ mol;
(2)常温下,氯气与烧碱溶液反应得“84”消毒液,NaClO 是“84”消毒液的有效成分,在此次抗击新冠病毒中发挥了重要作用 ,浸泡衣物时加入“84”消毒液在空气中放置一段时间漂白效果更好,原因用化学方程式表示为:___________ ;
(1)①写出实验室中制取氯气的离子方程式
②已知KMnO4与浓盐酸反应的化学方程式如下,该反应也可以用来制取氯气:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
15.8 g KMnO4能和
③实验室还可以利用如下反应制取氯气:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。若制取标准状况下6.72 L氯气,反应过程中转移电子的物质的量为
(2)常温下,氯气与烧碱溶液反应得“84”消毒液,NaClO 是“84”消毒液的有效成分,在此次抗击新冠病毒中发挥了重要作用 ,浸泡衣物时加入“84”消毒液在空气中放置一段时间漂白效果更好,原因用化学方程式表示为:
您最近一年使用:0次



