名校
1 . 把7 molA气体和5 molB气体混合放入2 L密闭容器中,在一定条件下发生反应:3A(g)+B(g)⇌2C(s)+xD(g),经5min达到平衡,此时生成2 mol C,测得D的平均反应速率为0.2 mol·(L·min)-1,求:
(1)B的转化率_______
(2)x的值_______
(3)平衡时压强与初始时压强之比_______
(4)该温度下此反应的平衡常数_______
(1)B的转化率
(2)x的值
(3)平衡时压强与初始时压强之比
(4)该温度下此反应的平衡常数
您最近一年使用:0次
2021-01-06更新
|
1427次组卷
|
6卷引用:广东省雷州市第二中学2020-2021学年高二上学期期中考试化学试题
广东省雷州市第二中学2020-2021学年高二上学期期中考试化学试题吉林省长春市第二十九中学2021-2022学年高二上学期第一学程考试化学试题(已下线)2.2.2 化学平衡常数(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)2.2.1 化学平衡常数-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)山西运城盐湖五中2022-2023学年高二上学期阶段性测试化学试题(已下线)专题04 可逆反应、化学平衡状态、化学平衡常数【考题猜想】(5大题型)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)
2 . 回答下列问题:
(1)标准状况下,0.85 g NH3的体积为__________ L。
(2)Fe2(SO4)3溶液中SO 的浓度为0.3 mol∙L−1,c[Fe2(SO4)3]=
的浓度为0.3 mol∙L−1,c[Fe2(SO4)3]=__________ mol∙L−1。
(3)同温同压下,气体N2和O2的密度之比为__________ 。
(4)同温同压下,等体积的气体SO2和CO的物质的量之比为__________ 。
(5)标准状况下,0.66 g某气态氧化物RO2的体积为336 mL,则元素R的相对原子质量为__________ 。
(6)将7.8 g Na2O2溶于93.8 g水中充分反应后(此时溶液密度近似为1.0 g·cm−3),c(NaOH)=__________ mol∙L−1。
(1)标准状况下,0.85 g NH3的体积为
(2)Fe2(SO4)3溶液中SO
 的浓度为0.3 mol∙L−1,c[Fe2(SO4)3]=
的浓度为0.3 mol∙L−1,c[Fe2(SO4)3]=(3)同温同压下,气体N2和O2的密度之比为
(4)同温同压下,等体积的气体SO2和CO的物质的量之比为
(5)标准状况下,0.66 g某气态氧化物RO2的体积为336 mL,则元素R的相对原子质量为
(6)将7.8 g Na2O2溶于93.8 g水中充分反应后(此时溶液密度近似为1.0 g·cm−3),c(NaOH)=
您最近一年使用:0次
2020-12-15更新
|
133次组卷
|
2卷引用:广东省海珠区2022-2023学年高一上学期1月化学竞赛试题
名校
解题方法
3 . 一定温度下,将3mol A气体和1mol B气体通入一密闭容器中,发生如下反应:3A(g)+B (g) xC(g)。请填写下列空白:
xC(g)。请填写下列空白:
(1)若容器体积固定为2L,反应1min时测得剩余1.8molA,C的浓度为0.4 mol·L-1。
①则1min内,B的平均反应速率为_____ ,x=____ ;
②若反应经2min达到平衡,平衡时C的浓度____ 0.8 mol·L-1(填“>”、“=”或“<”);
③若平衡混合物中C的体积分数为25%,则A的转化率是_____ ;
④若改变起始物质的加入量,欲使反应达到平衡时C的物质的量分数与原平衡相等,则起始加入的三种物质的物质的量n(A)、n(B)、n(C)之间应满足的条件____ (可用两个方程表示,其中一个用n(A)和 n(C),另一个用n(B)和n(C)表示)。
(2)若维持容器压强不变。
①达到平衡时C的体积分数______ 25%,(填“大于”、“等于”或“小于”);
②若改变起始物质的加入量,欲使反应达到平衡时C的物质的量是原平衡的2倍,则应加入_____ molA气体和_____ molB气
 xC(g)。请填写下列空白:
xC(g)。请填写下列空白:(1)若容器体积固定为2L,反应1min时测得剩余1.8molA,C的浓度为0.4 mol·L-1。
①则1min内,B的平均反应速率为
②若反应经2min达到平衡,平衡时C的浓度
③若平衡混合物中C的体积分数为25%,则A的转化率是
④若改变起始物质的加入量,欲使反应达到平衡时C的物质的量分数与原平衡相等,则起始加入的三种物质的物质的量n(A)、n(B)、n(C)之间应满足的条件
(2)若维持容器压强不变。
①达到平衡时C的体积分数
②若改变起始物质的加入量,欲使反应达到平衡时C的物质的量是原平衡的2倍,则应加入
您最近一年使用:0次
名校
解题方法
4 . 北京奥运会主体育场的外形好似“鸟巢”,有一类物质的结构也好似“鸟巢”,如化学式为B5H9的五硼烷。计算:五硼烷的摩尔质量是________ ,96 g五硼烷的物质的量是________ 。
您最近一年使用:0次
名校
5 . 计算:
(1)将26.4gNa2O与Na2O2的混合物投入足量的水中溶解。反应后水溶液增重24.8g,则原混合Na2O与Na2O2的物质的量之比是___ 。
(2)将5mol·L-1的Mg(NO3)2溶液amL稀释至bmL,稀释后溶液中NO 的物质的量浓度为
的物质的量浓度为__ 。
(3)实验室用MnO2和浓盐酸制取氯气时,有21.9g氯化氢被氧化,所得Cl2全部用石灰乳吸收,可制得源白粉的质量是___ 。
(1)将26.4gNa2O与Na2O2的混合物投入足量的水中溶解。反应后水溶液增重24.8g,则原混合Na2O与Na2O2的物质的量之比是
(2)将5mol·L-1的Mg(NO3)2溶液amL稀释至bmL,稀释后溶液中NO
 的物质的量浓度为
的物质的量浓度为(3)实验室用MnO2和浓盐酸制取氯气时,有21.9g氯化氢被氧化,所得Cl2全部用石灰乳吸收,可制得源白粉的质量是
您最近一年使用:0次
名校
6 . 自然界存在的碳酸盐类铜矿的化学组成为:aCuCO3·bCu(OH)2(a、b为正整数,且a≤2,b≤2)。
(1)将某矿样加盐酸至完全溶解,耗用HCl物质的量与产生CO2物质的量之比为3∶1;则它的化学组成为:________ 。
(2)将另一份矿样等分为A、B两份。加盐酸使A样品完全溶解,产生CO2 3.36 L(标准状况),再加热B样品,完全分解后得到20 g CuO。则该矿样中的铜元素质量分数为________ 。(计算结果保留三位有效数字)
(1)将某矿样加盐酸至完全溶解,耗用HCl物质的量与产生CO2物质的量之比为3∶1;则它的化学组成为:
(2)将另一份矿样等分为A、B两份。加盐酸使A样品完全溶解,产生CO2 3.36 L(标准状况),再加热B样品,完全分解后得到20 g CuO。则该矿样中的铜元素质量分数为
您最近一年使用:0次
名校
7 . 将7.8g Na2O2 投入到 93.8g 水中充分反应,求:
(1)所得溶液的溶质质量分数;_________
(2)向该溶液中通入一定量CO2,然后小心蒸干,所得固体冷却干燥,称重为 13.7g,通过计算推出该固体物体的组成和质量____ 。(不要求写计算过程)
(1)所得溶液的溶质质量分数;
(2)向该溶液中通入一定量CO2,然后小心蒸干,所得固体冷却干燥,称重为 13.7g,通过计算推出该固体物体的组成和质量
您最近一年使用:0次
名校
8 . 如图为某品牌84消毒液的部分产品说明,完成下列问题
(1)该消毒液中c(Na+)浓度约为(保留整数)________ 。
(2)欲制取该品牌消毒液理论上需标准状况下的Cl2 L________ 。
| 84消毒液 (有效成分)NaClO (规格)1000 mL (质量分数)25% (密度)1.19 g·cm-3 |
(1)该消毒液中c(Na+)浓度约为(保留整数)
(2)欲制取该品牌消毒液理论上需标准状况下的Cl2 L
您最近一年使用:0次
名校
解题方法
9 . 氮氧化物是空气的主要污染物之一,研究氮氧化物的性质对于防治空气污染有重要意义。
温度为T1时,在三个容积均为1L的密闭容器中发生反应:2NO(g)+O2(g) 2NO2(g)ΔH<0。实验测得:v正=v(NO)消耗=2v(O2)消耗=k正c2(NO)·c(O2),v逆=v(NO2)消耗=k逆c2(NO2),k正、k逆为速率常数,受温度影响。回答下列问题:
2NO2(g)ΔH<0。实验测得:v正=v(NO)消耗=2v(O2)消耗=k正c2(NO)·c(O2),v逆=v(NO2)消耗=k逆c2(NO2),k正、k逆为速率常数,受温度影响。回答下列问题:
(1)温度为T1时,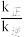 =
=__ ;当温度升高为T2时,k正、k逆分别增大m倍和n倍,则m__ n(填“>”、“<“或“=”)。
(2)若容器Ⅱ中达到平衡时 =1,则NO的转化率为
=1,则NO的转化率为__ 。
(3)容器Ⅲ中起始时v正__ v逆(填“>”、“<”或“=”),理由是__ 。
(4)T1时,在1L密闭容器中按照一定比例充入NO(g)和O2(g),达到平衡时NO2(g)的体积分数Φ(NO2)随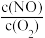 的变化如图所示,则A、B、C三点中NO的转化率最大的是
的变化如图所示,则A、B、C三点中NO的转化率最大的是__ ;当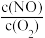 =2.3时,达到平衡时Φ(NO2)可能是D、E、F三点中的
=2.3时,达到平衡时Φ(NO2)可能是D、E、F三点中的__ 。

温度为T1时,在三个容积均为1L的密闭容器中发生反应:2NO(g)+O2(g)
 2NO2(g)ΔH<0。实验测得:v正=v(NO)消耗=2v(O2)消耗=k正c2(NO)·c(O2),v逆=v(NO2)消耗=k逆c2(NO2),k正、k逆为速率常数,受温度影响。回答下列问题:
2NO2(g)ΔH<0。实验测得:v正=v(NO)消耗=2v(O2)消耗=k正c2(NO)·c(O2),v逆=v(NO2)消耗=k逆c2(NO2),k正、k逆为速率常数,受温度影响。回答下列问题:| 容器编号 | 物质的起始浓度/mol·L−1 | 物质的平衡浓度/mol·L−1 | ||
| c(NO) | c(O2) | c(NO2) | c(O2) | |
| Ⅰ | 0.6 | 0.3 | 0 | 0.2 |
| Ⅱ | 0.5 | x | 0.3 | |
| Ⅲ | 0.3 | 0.25 | 0.2 | |
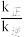 =
=(2)若容器Ⅱ中达到平衡时
 =1,则NO的转化率为
=1,则NO的转化率为(3)容器Ⅲ中起始时v正
(4)T1时,在1L密闭容器中按照一定比例充入NO(g)和O2(g),达到平衡时NO2(g)的体积分数Φ(NO2)随
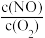 的变化如图所示,则A、B、C三点中NO的转化率最大的是
的变化如图所示,则A、B、C三点中NO的转化率最大的是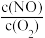 =2.3时,达到平衡时Φ(NO2)可能是D、E、F三点中的
=2.3时,达到平衡时Φ(NO2)可能是D、E、F三点中的
您最近一年使用:0次
2020-11-09更新
|
318次组卷
|
2卷引用:广东华侨中学2022-2023学年高二上学期期中考试化学试题
解题方法
10 . 某同学将3.84 g铜片投入300 mL足量稀硝酸中,铜片完全溶解。请回答下列问题。
已知:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O。
(1)铜在此反应中_____ (填“得”或“失”)电子,作_____ 剂(填“氧化”或“还原”)。
(2)参加反应的氧化剂与还原剂物质的量之比为______ 。
(3)此反应中生成的气体的体积为多少毫升?(标准状况下)______ 。
(4)生成Cu(NO3)2的浓度为?______ (忽略溶液体积变化)
已知:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O。
(1)铜在此反应中
(2)参加反应的氧化剂与还原剂物质的量之比为
(3)此反应中生成的气体的体积为多少毫升?(标准状况下)
(4)生成Cu(NO3)2的浓度为?
您最近一年使用:0次



