20. 某实验小组以石灰粉[主要成分为Ca(OH)
2和CaCO
3]为原料制备KClO
3的流程如图所示:
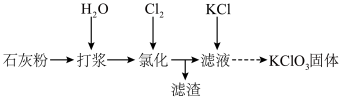
(1)“打浆”的目的是
_______。
(2)“氯化”过程控制氯气不过量,在75 ℃左右进行。氯化时,氯气与氢氧化钙生成次氯酸钙,次氯酸钙进一步分解为氯酸钙,少量次氯酸钙分解产生氯化钙和氧气;“氯化”温度较低时,Cl
2易与Ca(OH)
2反应而生成漂白粉,写出该反应的化学方程式:
________。 露置在空气中一段时间的漂白粉,加稀盐酸后产生的气体除了可能有O
2和HCl外,还可能含有
________(填化学式)。
(3)“氯化”过程中Cl
2与浆水反应生成Ca(ClO
3)
2的总反应为6Ca(OH)
2+ 6Cl
2 =Ca(ClO
3)
2 +5CaCl
2 +6H
2O,反应中还原产物为
_________(填化学式)。
(4)由于在“氯化”过程中易发生副反应,则“氯化”后溶液中
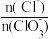
=
_____(填“>”“<”或“=”)5。
(5)向滤液中加入稍过量KCl固体,可将Ca(ClO
3)
2转化为KClO
3。从该溶液中析出KClO
3固体的方法是
_____。已知不同温度下,各物质的溶解度数据如表(单位/g):
| KCl | KClO3 | CaCl2 | Ca(ClO3)2 |
| 20℃ | 28 | 7.1 | 74.5 | 55 |
| 100℃ | 56. 7 | 57 | 159 | 70 |