某实验小组以石灰粉[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的流程如图所示:
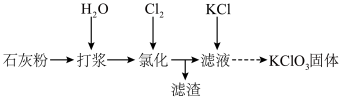
(1)“打浆”的目的是_______ 。
(2)“氯化”过程控制氯气不过量,在75 ℃左右进行。氯化时,氯气与氢氧化钙生成次氯酸钙,次氯酸钙进一步分解为氯酸钙,少量次氯酸钙分解产生氯化钙和氧气;“氯化”温度较低时,Cl2易与Ca(OH)2反应而生成漂白粉,写出该反应的化学方程式:________ 。 露置在空气中一段时间的漂白粉,加稀盐酸后产生的气体除了可能有O2和HCl外,还可能含有________ (填化学式)。
(3)“氯化”过程中Cl2与浆水反应生成Ca(ClO3)2的总反应为6Ca(OH)2+ 6Cl2 =Ca(ClO3)2 +5CaCl2 +6H2O,反应中还原产物为_________ (填化学式)。
(4)由于在“氯化”过程中易发生副反应,则“氯化”后溶液中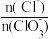 =
=_____ (填“>”“<”或“=”)5。
(5)向滤液中加入稍过量KCl固体,可将Ca(ClO3)2转化为KClO3。从该溶液中析出KClO3固体的方法是_____ 。已知不同温度下,各物质的溶解度数据如表(单位/g):

(1)“打浆”的目的是
(2)“氯化”过程控制氯气不过量,在75 ℃左右进行。氯化时,氯气与氢氧化钙生成次氯酸钙,次氯酸钙进一步分解为氯酸钙,少量次氯酸钙分解产生氯化钙和氧气;“氯化”温度较低时,Cl2易与Ca(OH)2反应而生成漂白粉,写出该反应的化学方程式:
(3)“氯化”过程中Cl2与浆水反应生成Ca(ClO3)2的总反应为6Ca(OH)2+ 6Cl2 =Ca(ClO3)2 +5CaCl2 +6H2O,反应中还原产物为
(4)由于在“氯化”过程中易发生副反应,则“氯化”后溶液中
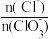 =
=(5)向滤液中加入稍过量KCl固体,可将Ca(ClO3)2转化为KClO3。从该溶液中析出KClO3固体的方法是
| KCl | KClO3 | CaCl2 | Ca(ClO3)2 | |
| 20℃ | 28 | 7.1 | 74.5 | 55 |
| 100℃ | 56. 7 | 57 | 159 | 70 |
更新时间:2020-11-06 11:51:55
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】溴及其化合物是重要的化工基础原料,广泛应用于制药、染料、电子、日化等行业。
Ⅰ.用图所示装置A可制取氯气。将纯净的氯气通入装置C的NaBr溶液中可以在实验室制取少量溴单质。_______ 。
(2)为了富集生成的溴单质,用热空气吹出,并在装置D中收集,则装置D中可选用的试剂为_______。
Ⅱ.工业上从海水中提取 过程更为复杂。研究集中在空气吹出法,空气吹出法提溴对原料的适应性高,但吹出设备庞大,且能耗高。某工厂针对空气吹出法的缺点进行工艺改造,提出连续双段真空提溴工艺,如图转化过程:
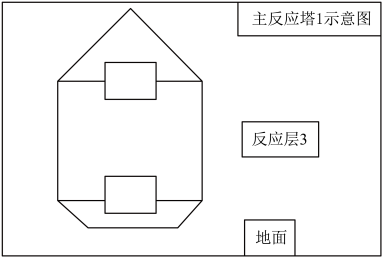
过程更为复杂。研究集中在空气吹出法,空气吹出法提溴对原料的适应性高,但吹出设备庞大,且能耗高。某工厂针对空气吹出法的缺点进行工艺改造,提出连续双段真空提溴工艺,如图转化过程:_______ 。主反应塔1中温度保持在82~99℃,减少了水蒸气的用量。从化学性质的角度分析这么做的主要目的有两点:①减少氯气与水的反应,②减少_______ 反应。从经济角度来看这么做还可以减少的_______ 用量。
(4)为了让原料卤水与氯气在主反应塔1中更充分反应,请将正确装置对应的选项填在图中“□”处:_______ 。_______ 。冷凝器需要铺设循环冷却水管道,循环冷却水管道中水流方向是_______ (填“从地面到顶端”或“从顶端到地面”),请说明原因_______ 。
(6)在分离器中经冷凝、分离、纯化后制得精溴。少量氯、溴与混合废气需要经过水蒸气喷射泵喷入气体吸收器。此时,还需进行酸化调节,再经过排水管通入主反应塔1中循环利用。请写出吸收器中酸化调节主要发生的离子反应方程式:_______ 。
Ⅰ.用图所示装置A可制取氯气。将纯净的氯气通入装置C的NaBr溶液中可以在实验室制取少量溴单质。
(2)为了富集生成的溴单质,用热空气吹出,并在装置D中收集,则装置D中可选用的试剂为_______。
A. | B.NaOH | C.KI | D. |
Ⅱ.工业上从海水中提取
 过程更为复杂。研究集中在空气吹出法,空气吹出法提溴对原料的适应性高,但吹出设备庞大,且能耗高。某工厂针对空气吹出法的缺点进行工艺改造,提出连续双段真空提溴工艺,如图转化过程:
过程更为复杂。研究集中在空气吹出法,空气吹出法提溴对原料的适应性高,但吹出设备庞大,且能耗高。某工厂针对空气吹出法的缺点进行工艺改造,提出连续双段真空提溴工艺,如图转化过程:
(4)为了让原料卤水与氯气在主反应塔1中更充分反应,请将正确装置对应的选项填在图中“□”处:

(6)在分离器中经冷凝、分离、纯化后制得精溴。少量氯、溴与混合废气需要经过水蒸气喷射泵喷入气体吸收器。此时,还需进行酸化调节,再经过排水管通入主反应塔1中循环利用。请写出吸收器中酸化调节主要发生的离子反应方程式:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
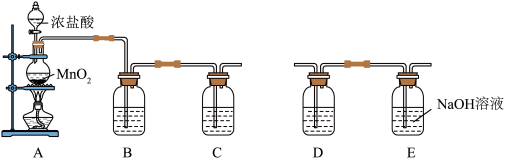
【推荐2】某化学小组用如图所示装置制备氯气并验证其性质。请回答下列问题:

(1)仪器A的名称是_______ ;请写出用二氧化锰和浓盐酸共热的化学方程式_______ ;装置B可贮存多余的气体,则装置B中所盛装的液体是_______ 。
(2)可用C,D装置制取氯酸钾、次氯酸钠,图中:C的试管里盛有15mL30%KOH溶液,置于水浴中;D的试管里盛有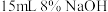 溶液,置于冰水浴中;比较制取氯酸钾和次氯酸钠的条件,二者的差异是①
溶液,置于冰水浴中;比较制取氯酸钾和次氯酸钠的条件,二者的差异是①_______ ;②_______ 。
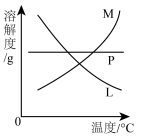
(3)反应完毕经冷却后,C的试管中有大量晶体析出。图中符合该晶体溶解度曲线的是_______ (填写编号字母);从C的试管中分离出该晶体的方法是_______ (填写操作名称)。
(4)装置E的作用是验证氯气无漂白性但在水溶液中有漂白性,则装置中Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是_______ (填写编号字母)。

(1)仪器A的名称是
(2)可用C,D装置制取氯酸钾、次氯酸钠,图中:C的试管里盛有15mL30%KOH溶液,置于水浴中;D的试管里盛有
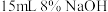 溶液,置于冰水浴中;比较制取氯酸钾和次氯酸钠的条件,二者的差异是①
溶液,置于冰水浴中;比较制取氯酸钾和次氯酸钠的条件,二者的差异是①(3)反应完毕经冷却后,C的试管中有大量晶体析出。图中符合该晶体溶解度曲线的是

(4)装置E的作用是验证氯气无漂白性但在水溶液中有漂白性,则装置中Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是
| 序号 | Ⅰ | Ⅱ | Ⅲ |
| A | 干燥的石蕊试纸 | 碱石灰 | 湿润的石蕊试纸 |
| B | 干燥的石蕊试纸 | 无水氯化钙 | 湿润的石蕊试纸 |
| C | 湿润的石蕊试纸 | 无水氯化钙 | 干燥的石蕊试纸 |
| D | 湿润的石蕊试纸 | 浓硫酸 | 干燥的石蕊试纸 |
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】肼(N2H4,无色液体)是一种用途广泛的化工原料。实验室中先制备次氯酸钠,再用次氯酸钠溶液和氨反应制备肼并验证肼的性质。实验装置如图所示。

已知:Cl2(g)+2NaOH(aq)=NaClO(aq)+NaCl(aq)+H2O(g) △H<0。当温度超过40℃时,Cl2与NaOH溶液反应生成NaClO3。回答下列问题:
(1)仪器a的名称是________________ ,装置B的作用是____________________________ 。
(2)为控制D装置中的反应温度,除用冷水浴外,还需采取的实验操作是________________ 。
(3)当三颈烧瓶中出现黄绿色气体时立即关闭分液漏斗活塞、移去酒精灯、关闭K1。此时装置C的作用是________________________________ 。
(4)将D装置水槽中的冷水换为热水,把三颈烧瓶中黄绿色气体赶走后,打开K2,通入NH3,使其与NaClO溶液反应制取肼。理论上通入三颈烧瓶的Cl2和NH3的最佳物质的量之比为______________ 。
(5)请从提供的下列试剂中选择合适试剂,设计合理的实验方案验证肼的还原性____________ (说明操作、现象和结论)。
①淀粉-KI溶液 ②稀硫酸(酚酞) ③NaHCO3 ④AgC1

已知:Cl2(g)+2NaOH(aq)=NaClO(aq)+NaCl(aq)+H2O(g) △H<0。当温度超过40℃时,Cl2与NaOH溶液反应生成NaClO3。回答下列问题:
(1)仪器a的名称是
(2)为控制D装置中的反应温度,除用冷水浴外,还需采取的实验操作是
(3)当三颈烧瓶中出现黄绿色气体时立即关闭分液漏斗活塞、移去酒精灯、关闭K1。此时装置C的作用是
(4)将D装置水槽中的冷水换为热水,把三颈烧瓶中黄绿色气体赶走后,打开K2,通入NH3,使其与NaClO溶液反应制取肼。理论上通入三颈烧瓶的Cl2和NH3的最佳物质的量之比为
(5)请从提供的下列试剂中选择合适试剂,设计合理的实验方案验证肼的还原性
①淀粉-KI溶液 ②稀硫酸(酚酞) ③NaHCO3 ④AgC1
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】软锰矿(主要成分是MnO2)与浓盐酸混合加热,产生了氯气。某学生使用这一原理设计如图所示的实验装置,并且利用制得的氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应),据此回答下列问题:

(1)A仪器的名称是__________
(2)漂白粉将在U形管中产生,其化学方程式是____________________ 。
(3)此实验结果所得Ca(ClO)2产率太低,经分析并查阅资料发现,主要原因是在U形管中存在两个副反应:
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是______________________________ 。
②试判断另一个副反应(写出此反应方程式):____________________ 。
(4)漂粉精同盐酸作用产生氯气:Ca(ClO)2+4HCl=2Cl2↑+CaCl2+2H2O,该反应中每生成1molCl2,转移电子的物质的量为__________ mol。
(5)有效氯是漂粉精中有效Ca(ClO)2的含量大小的标志。已知:有效氯=(漂粉精加盐酸所释放出的氯气的质量/漂粉精的质量) 100%,该漂粉精的有效氯为65%,则该漂粉精中Ca(ClO)2的质量分数为
100%,该漂粉精的有效氯为65%,则该漂粉精中Ca(ClO)2的质量分数为__________ (保留一位小数)

(1)A仪器的名称是
(2)漂白粉将在U形管中产生,其化学方程式是
(3)此实验结果所得Ca(ClO)2产率太低,经分析并查阅资料发现,主要原因是在U形管中存在两个副反应:
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是
②试判断另一个副反应(写出此反应方程式):
(4)漂粉精同盐酸作用产生氯气:Ca(ClO)2+4HCl=2Cl2↑+CaCl2+2H2O,该反应中每生成1molCl2,转移电子的物质的量为
(5)有效氯是漂粉精中有效Ca(ClO)2的含量大小的标志。已知:有效氯=(漂粉精加盐酸所释放出的氯气的质量/漂粉精的质量)
 100%,该漂粉精的有效氯为65%,则该漂粉精中Ca(ClO)2的质量分数为
100%,该漂粉精的有效氯为65%,则该漂粉精中Ca(ClO)2的质量分数为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】根据右边反应框图填空,已知反应①是工业上生产化合物D的反应,反应⑤是实验室鉴定化合物E的反应。工业上制取漂白粉的反应也在其中。

(1)单质L是_____ 。
(2)化合物B是____ 。
(3)图中除反应①以外,还有两个用于工业生产的反应,是________ 和_______ (填代号)。
请写出他们的化学反应方程式:____________ 、____________ 。

(1)单质L是
(2)化合物B是
(3)图中除反应①以外,还有两个用于工业生产的反应,是
请写出他们的化学反应方程式:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】含氯消毒剂在日常生产和生活中有着重要应用,某研究性学习小组利用下列装置制备漂白粉,并进行漂白粉有效成分的质量分数的测定。
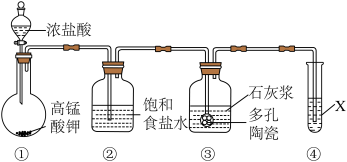
(1)装置④中的X试剂为___________ 。
(2)装置③中多孔陶瓷的作用是___________ ,漂白粉的有效成分是___________ (用化学式表示)。
(3)测定漂白粉有效成分的质量分数:称取1.000 g漂白粉于锥形瓶中,加水溶解,调节溶液的pH,以淀粉为指示剂,用0.1000 mol·L KI溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点,反应原理为:
KI溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点,反应原理为: ,
,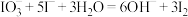 ,实验测得数据如下表所示。
,实验测得数据如下表所示。
该漂白粉中有效成分的质量分数为___________ ;若滴定过程中未充分振荡溶液,局部变浅蓝色时就停止滴定,则测定结果将___________ (填“偏高”“偏低”或“无影响”)。
(4)卤化银因具有感光性,可用于制造感光材料。已知室温下, ,
,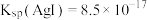 ,将AgCl与AgI的饱和溶液等体积混合,再加入足量浓
,将AgCl与AgI的饱和溶液等体积混合,再加入足量浓 溶液,关于所生成的沉淀说法正确的是
溶液,关于所生成的沉淀说法正确的是___________ 。

(1)装置④中的X试剂为
(2)装置③中多孔陶瓷的作用是
(3)测定漂白粉有效成分的质量分数:称取1.000 g漂白粉于锥形瓶中,加水溶解,调节溶液的pH,以淀粉为指示剂,用0.1000 mol·L
 KI溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点,反应原理为:
KI溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点,反应原理为: ,
,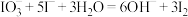 ,实验测得数据如下表所示。
,实验测得数据如下表所示。| 滴定次数 | 1 | 2 | 3 |
| KI溶液体积/mL | 19.98 | 20.02 | 20.00 |
(4)卤化银因具有感光性,可用于制造感光材料。已知室温下,
 ,
,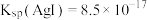 ,将AgCl与AgI的饱和溶液等体积混合,再加入足量浓
,将AgCl与AgI的饱和溶液等体积混合,再加入足量浓 溶液,关于所生成的沉淀说法正确的是
溶液,关于所生成的沉淀说法正确的是| A.只有AgI生成 | B.AgCl和AgI等量生成 |
| C.AgCl沉淀少于AgI沉淀 | D.AgCl沉淀多于AgI沉淀 |
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】碲(Te)为第VIA元素,其单质凭借优良的性能成为制作合金添加剂、半导体、光电元件的主体材料,并被广泛应用于冶金、航空航天、电子等领域。可从精炼铜的阳极泥(主要成分为Cu2Te)中回收碲,工艺流程如下 :
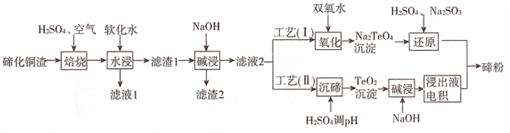
(1)“焙烧”后,碲主要以TeO2 形式存在,写出相应反应的化学方程式:_____________ 。
(2)为了选择最佳的焙烧工艺,进行了温度和硫酸加入量的条件实验,结果如下表所示:

则实验中应选择的条件为_______________ ,原因为_______________ 。
(3)工艺(I)中,“还原”时发生的总的化学方程式为_______________ 。
(4)由于工艺(I)中“氧化”对溶液和物料条件要求高,有研究者采用工艺(II)获得碲。则“电积”过程中,阴极的电极反应式为_______________ 。
(5)工业生产中,滤渣2经硫酸酸浸后得滤液3和滤渣3。
①滤液3 与滤液1合并,进入铜电积系统。该处理措施的优点为________________ 。
②滤渣3中若含Au和Ag,可用__________ 将二者分离。(填字母)
A.王水 B.稀硝酸 C.浓氢氧化钠溶液 D.浓盐酸

(1)“焙烧”后,碲主要以TeO2 形式存在,写出相应反应的化学方程式:
(2)为了选择最佳的焙烧工艺,进行了温度和硫酸加入量的条件实验,结果如下表所示:

则实验中应选择的条件为
(3)工艺(I)中,“还原”时发生的总的化学方程式为
(4)由于工艺(I)中“氧化”对溶液和物料条件要求高,有研究者采用工艺(II)获得碲。则“电积”过程中,阴极的电极反应式为
(5)工业生产中,滤渣2经硫酸酸浸后得滤液3和滤渣3。
①滤液3 与滤液1合并,进入铜电积系统。该处理措施的优点为
②滤渣3中若含Au和Ag,可用
A.王水 B.稀硝酸 C.浓氢氧化钠溶液 D.浓盐酸
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】某小组以含镍废料(主要含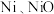 ,以及少量
,以及少量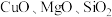 )为原料提取镍的流程如图所示:
)为原料提取镍的流程如图所示:
(1)固体2的主要成分为__________ (填化学式)。
(2)在“除镁”阶段,若溶液的 太小,会显著增加
太小,会显著增加 的用量,其原因为
的用量,其原因为____________________ (结合勒夏特列原理解释)。
(3) 可用于镍氢电池的正极材料。某镍氢电池的总反应为
可用于镍氢电池的正极材料。某镍氢电池的总反应为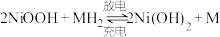 ,该电池充电时,阳极的电极反应式为
,该电池充电时,阳极的电极反应式为__________ 。
(4)可利用三室双膜法进行“电沉积”制镍,其原理如下:__________ 。
②可以通过电解法提纯粗镍,粗镍作______ (填“阳”或“阴”)极,阴极的电极反应式为_______________ 。
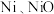 ,以及少量
,以及少量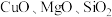 )为原料提取镍的流程如图所示:
)为原料提取镍的流程如图所示:
(1)固体2的主要成分为
(2)在“除镁”阶段,若溶液的
 太小,会显著增加
太小,会显著增加 的用量,其原因为
的用量,其原因为(3)
 可用于镍氢电池的正极材料。某镍氢电池的总反应为
可用于镍氢电池的正极材料。某镍氢电池的总反应为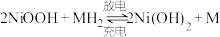 ,该电池充电时,阳极的电极反应式为
,该电池充电时,阳极的电极反应式为(4)可利用三室双膜法进行“电沉积”制镍,其原理如下:

②可以通过电解法提纯粗镍,粗镍作
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】一种银铟矿主要成分为 、
、 、
、 、
、 、
、 、
、 、
、 、
、 等物质,从该矿获得稀有金属的工艺流程如图所示:
等物质,从该矿获得稀有金属的工艺流程如图所示: 如表:
如表:
(1)“浸出”过程中金、银、铜分别转化为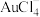 、
、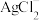 、
、 进入溶液,同时生成硫,写出
进入溶液,同时生成硫,写出 发生反应的离子方程式
发生反应的离子方程式___________ 。
(2)高温水蒸气除铁利用了 易水解的性质,写出该反应的化学方程式
易水解的性质,写出该反应的化学方程式___________ 。
(3)“二次还原”得到的滤渣主要成分___________ 。
(4)“二次中和”得到的滤渣除少量 外,主要成分还有
外,主要成分还有___________ 。(写化学式)。
(5)“分铅锌”步骤中,维持 饱和水溶液的浓度为0.01
饱和水溶液的浓度为0.01 ,为使
,为使 沉淀完全(沉淀完全是指离子浓度小于或等于
沉淀完全(沉淀完全是指离子浓度小于或等于 ),需控制溶液的
),需控制溶液的 不小于
不小于___________ 。
已知: ;
; ,
,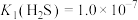 ;
;
(6)已知:氧化还原反应可看成由两个半反应组成,每个半反应具有一定的电极电势(用“ ”表示),
”表示), 越大则该物质的氧化性越强,
越大则该物质的氧化性越强, 越低则该物质的还原性越强。浸出步骤中金反应的两个半反应如下:
越低则该物质的还原性越强。浸出步骤中金反应的两个半反应如下: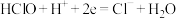 ,
,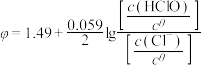 ;
; ,
,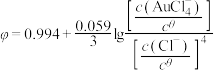 (
( 与半反应式的系数无关,仅与浓度有关,
与半反应式的系数无关,仅与浓度有关, )
)
下图是 的浸出率与
的浸出率与 溶液浓度的关系,请解释A点之前,金浸出率增大的原因是
溶液浓度的关系,请解释A点之前,金浸出率增大的原因是___________ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 等物质,从该矿获得稀有金属的工艺流程如图所示:
等物质,从该矿获得稀有金属的工艺流程如图所示:
 如表:
如表:| 金属离子 |  |  |  |  |  |  |
开始沉淀的 | 2.2 | 2.1 | 2.6 | 4.6 | 6.24 | 7.1 |
完全沉淀( )的 )的 | 3.2 | 3.4 | 4.3 | 6.6 | 8.24 | 9.1 |
(1)“浸出”过程中金、银、铜分别转化为
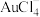 、
、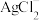 、
、 进入溶液,同时生成硫,写出
进入溶液,同时生成硫,写出 发生反应的离子方程式
发生反应的离子方程式(2)高温水蒸气除铁利用了
 易水解的性质,写出该反应的化学方程式
易水解的性质,写出该反应的化学方程式(3)“二次还原”得到的滤渣主要成分
(4)“二次中和”得到的滤渣除少量
 外,主要成分还有
外,主要成分还有(5)“分铅锌”步骤中,维持
 饱和水溶液的浓度为0.01
饱和水溶液的浓度为0.01 ,为使
,为使 沉淀完全(沉淀完全是指离子浓度小于或等于
沉淀完全(沉淀完全是指离子浓度小于或等于 ),需控制溶液的
),需控制溶液的 不小于
不小于已知:
 ;
; ,
, ;
;
(6)已知:氧化还原反应可看成由两个半反应组成,每个半反应具有一定的电极电势(用“
 ”表示),
”表示), 越大则该物质的氧化性越强,
越大则该物质的氧化性越强, 越低则该物质的还原性越强。浸出步骤中金反应的两个半反应如下:
越低则该物质的还原性越强。浸出步骤中金反应的两个半反应如下: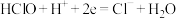 ,
,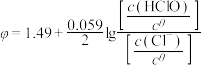 ;
; ,
,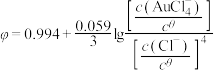 (
( 与半反应式的系数无关,仅与浓度有关,
与半反应式的系数无关,仅与浓度有关, )
)下图是
 的浸出率与
的浸出率与 溶液浓度的关系,请解释A点之前,金浸出率增大的原因是
溶液浓度的关系,请解释A点之前,金浸出率增大的原因是
您最近一年使用:0次




