名校
1 . 已知几种含碳物质间的转化及能量变化关系如图所示。
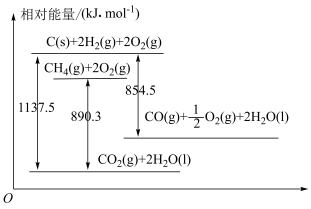
(1)写出表示CO燃烧热的热化学方程式:___________ 。
(2)反应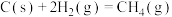

___________  ,该反应中反应物的总键能
,该反应中反应物的总键能___________ (填“大于”、“小于”或“等于”)生成物的总键能。若18gC(s)与 反应,完全转化成
反应,完全转化成 ,需要
,需要___________ (填“吸收”或“放出”)___________ kJ能量。
(3)在25℃、101kPa下,30g由 和CO组成的混合气体完全燃烧生成
和CO组成的混合气体完全燃烧生成 和液态水,放出热量1031.8kJ。则混合气体中
和液态水,放出热量1031.8kJ。则混合气体中 和CO的物质的量分别为
和CO的物质的量分别为___________ mol、___________ mol。

(1)写出表示CO燃烧热的热化学方程式:
(2)反应
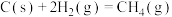

 ,该反应中反应物的总键能
,该反应中反应物的总键能 反应,完全转化成
反应,完全转化成 ,需要
,需要(3)在25℃、101kPa下,30g由
 和CO组成的混合气体完全燃烧生成
和CO组成的混合气体完全燃烧生成 和液态水,放出热量1031.8kJ。则混合气体中
和液态水,放出热量1031.8kJ。则混合气体中 和CO的物质的量分别为
和CO的物质的量分别为
您最近一年使用:0次
2023-11-21更新
|
142次组卷
|
2卷引用:广东省深圳市第三高级中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
2 . 运用氧化还原反应和离子反应知识回答下列问题:
Ⅰ.将H2S和空气的混合气体通入FeCl3、FeCl2和CuCl2的混合溶液中回收S,其转化如图所示(CuS不溶于水)。
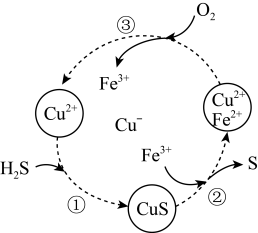
(1)写出过程②和过程中③发生反应的离子方程式:
i.过程②___________ 。
ii.过程③___________ 。
iii.整个转化过程中可以循环使用的离子是___________ 。
Ⅱ.新型纳米材料氧缺位铁酸盐(MFe2Ox,3<x<4,M=Mn、Zn、Ni,且均为+2价,下同)是由铁酸盐MFe2O4经过高温反应得到的。
(2)将纳米材料氧缺位铁酸盐分散在蒸馏水中,所形成的分散系属于___________ 。
(3)MFe2O4中Fe元素的化合价为___________ 。
(4)在酸性条件下,Fe2O 容易转化为Fe2+,某反应体系中共存在下列6种粒子:Fe2O
容易转化为Fe2+,某反应体系中共存在下列6种粒子:Fe2O 、Fe2+、H+、H2O、Cu2O、Cu2+,则Fe2O
、Fe2+、H+、H2O、Cu2O、Cu2+,则Fe2O 转化为Fe2+的离子方程式
转化为Fe2+的离子方程式___________ 。
(5)已知As2O3与Zn可以发生如下反应:As2O3+6Zn+6H2SO4=2AsH3↑+6ZnSO4+3H2O(反应前后H元素化合价未发生变化),请用单线桥法标出电子转移的方向和数目___________ 。
Ⅰ.将H2S和空气的混合气体通入FeCl3、FeCl2和CuCl2的混合溶液中回收S,其转化如图所示(CuS不溶于水)。

(1)写出过程②和过程中③发生反应的离子方程式:
i.过程②
ii.过程③
iii.整个转化过程中可以循环使用的离子是
Ⅱ.新型纳米材料氧缺位铁酸盐(MFe2Ox,3<x<4,M=Mn、Zn、Ni,且均为+2价,下同)是由铁酸盐MFe2O4经过高温反应得到的。
(2)将纳米材料氧缺位铁酸盐分散在蒸馏水中,所形成的分散系属于
(3)MFe2O4中Fe元素的化合价为
(4)在酸性条件下,Fe2O
 容易转化为Fe2+,某反应体系中共存在下列6种粒子:Fe2O
容易转化为Fe2+,某反应体系中共存在下列6种粒子:Fe2O 、Fe2+、H+、H2O、Cu2O、Cu2+,则Fe2O
、Fe2+、H+、H2O、Cu2O、Cu2+,则Fe2O 转化为Fe2+的离子方程式
转化为Fe2+的离子方程式(5)已知As2O3与Zn可以发生如下反应:As2O3+6Zn+6H2SO4=2AsH3↑+6ZnSO4+3H2O(反应前后H元素化合价未发生变化),请用单线桥法标出电子转移的方向和数目
您最近一年使用:0次
名校
解题方法
3 . 氮的化合物是化学研究的热点之一,请回答下列问题:
(1)汽车尾气中的 、
、 在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出
在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出 被
被 还原的化学方程式
还原的化学方程式_______ ,并用双线桥法标出电子转移的方向和数目。
(2)氮氧化物是造成雾霾天气的主要原因之一,利用 和
和 的溶液处理氮氧化物的反应过程如下:
的溶液处理氮氧化物的反应过程如下:
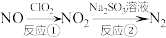
反应①的化学方程式是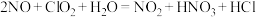 ,反应②的离子方程式是
,反应②的离子方程式是_______ ;若有1.4g 生成,需消耗
生成,需消耗
_______ g。
亚硝酸钠有咸味,有毒。已知: 。
。
(3)上述反应的还原剂为_______ (填化学式);若反应中有1分子 气体生成,则转移电子的数目为
气体生成,则转移电子的数目为_______ 。
(4)在酸性条件下,高锰酸钾可将 氧化为
氧化为 ,所得溶液中锰元素仅以
,所得溶液中锰元素仅以 形式存在,写出此反应的离子方程式:
形式存在,写出此反应的离子方程式:_______ 。
(1)汽车尾气中的
 、
、 在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出
在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出 被
被 还原的化学方程式
还原的化学方程式(2)氮氧化物是造成雾霾天气的主要原因之一,利用
 和
和 的溶液处理氮氧化物的反应过程如下:
的溶液处理氮氧化物的反应过程如下: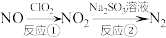
反应①的化学方程式是
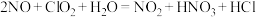 ,反应②的离子方程式是
,反应②的离子方程式是 生成,需消耗
生成,需消耗
亚硝酸钠有咸味,有毒。已知:
 。
。(3)上述反应的还原剂为
 气体生成,则转移电子的数目为
气体生成,则转移电子的数目为(4)在酸性条件下,高锰酸钾可将
 氧化为
氧化为 ,所得溶液中锰元素仅以
,所得溶液中锰元素仅以 形式存在,写出此反应的离子方程式:
形式存在,写出此反应的离子方程式:
您最近一年使用:0次
2023-10-15更新
|
235次组卷
|
2卷引用:广东北江实验学校2023—2024学年高一上学期10月月考化学试题
解题方法
4 . 某温度时,在2L容器中发生A、B两种气体间的转化反应,A、B物质的量随时间变化的曲线如图所示,M点的坐标为(7,0.24)请分析图中数据,回答下列问题。
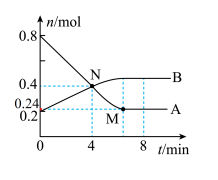
(1)该反应______ (填写“是”或“不是”)可逆反应。
(2)该化学方程式为______ 。
(3)反应从开始至4min时,用B的浓度变化来表示的反应速率为______ 。
(4)比较M、N两点该反应的正反应速率的相对大小v(M)正______ v(N)正(填写“>”、“<”或“=”)。
(5)运用图示数据计算该反应达到限度时A的转化率为______ %。

(1)该反应
(2)该化学方程式为
(3)反应从开始至4min时,用B的浓度变化来表示的反应速率为
(4)比较M、N两点该反应的正反应速率的相对大小v(M)正
(5)运用图示数据计算该反应达到限度时A的转化率为
您最近一年使用:0次
名校
5 . 计算
(1)15.6g Na2X中含有0.4mol Na+,则X的相对原子质量为_______ 。
(2)标准状况下,44.8L氯气通入足量NaOH溶液中,转移的电子数目为_______ 。
(3)标准状况下,甲烷和一氧化碳的混合气体共8.96 L,其质量为7.6 g,则混合气体中甲烷的物质的量为_______ 。
(4)测定Na2CO3样品(含氯化钠杂质)中Na2CO3的质量分数:称取m g样品放入烧杯内加水溶解,加入过量的氯化钙溶液充分反应,过滤、洗涤、干燥,称量沉淀的质量为n g。则样品中Na2CO3的质量分数为_______ 。
(1)15.6g Na2X中含有0.4mol Na+,则X的相对原子质量为
(2)标准状况下,44.8L氯气通入足量NaOH溶液中,转移的电子数目为
(3)标准状况下,甲烷和一氧化碳的混合气体共8.96 L,其质量为7.6 g,则混合气体中甲烷的物质的量为
(4)测定Na2CO3样品(含氯化钠杂质)中Na2CO3的质量分数:称取m g样品放入烧杯内加水溶解,加入过量的氯化钙溶液充分反应,过滤、洗涤、干燥,称量沉淀的质量为n g。则样品中Na2CO3的质量分数为
您最近一年使用:0次
名校
6 .  与
与 在高温下发生反应:
在高温下发生反应: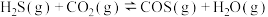
 。在
。在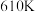 时,将
时,将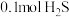 与
与 充入
充入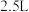 的空钢瓶中,经过
的空钢瓶中,经过 ,反应达到平衡,反应平衡时水蒸气的物质的量分数为0.125。
,反应达到平衡,反应平衡时水蒸气的物质的量分数为0.125。
(1)求 的平衡转化率
的平衡转化率_______ 。
(2)求该温度下的反应平衡常数_______ 。
 与
与 在高温下发生反应:
在高温下发生反应: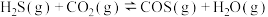
 。在
。在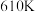 时,将
时,将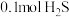 与
与 充入
充入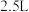 的空钢瓶中,经过
的空钢瓶中,经过 ,反应达到平衡,反应平衡时水蒸气的物质的量分数为0.125。
,反应达到平衡,反应平衡时水蒸气的物质的量分数为0.125。(1)求
 的平衡转化率
的平衡转化率(2)求该温度下的反应平衡常数
您最近一年使用:0次
名校
解题方法
7 . 在空气中灼烧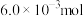 的
的 ,完全转化为
,完全转化为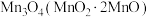 ,将其溶解于
,将其溶解于 溶有
溶有 的稀
的稀 溶液中,锰被还原为+2价。过量的
溶液中,锰被还原为+2价。过量的 需要
需要 的
的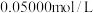 的
的 滴定,计算实验加入的
滴定,计算实验加入的 的质量(注:
的质量(注: 的相对分子质量为392)
的相对分子质量为392) _______ 。
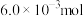 的
的 ,完全转化为
,完全转化为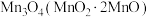 ,将其溶解于
,将其溶解于 溶有
溶有 的稀
的稀 溶液中,锰被还原为+2价。过量的
溶液中,锰被还原为+2价。过量的 需要
需要 的
的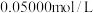 的
的 滴定,计算实验加入的
滴定,计算实验加入的 的质量(注:
的质量(注: 的相对分子质量为392)
的相对分子质量为392)
您最近一年使用:0次
名校
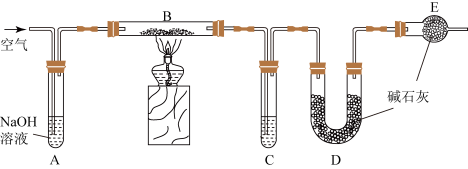
8 . 某食品膨松剂作用物质为 ,某兴趣小组研究加热情况下该膨松剂放出气体的量,设计实验的装置图如下。
,某兴趣小组研究加热情况下该膨松剂放出气体的量,设计实验的装置图如下。
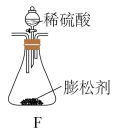
已知:碱石灰是固体氢氧化钠和氧化钙的混合物: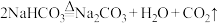 。
。
(1)A装置中 溶液的作用是除去空气中的
溶液的作用是除去空气中的________ ,C装置内所盛试剂是________ ,E装置的作用是________________________ ;
(2)若没有E装置,测定的结果________ (填“偏高”、“偏低”或“无影响”);若没有A装置,B装置左侧用橡皮塞封闭,实验结果将________ (填“偏高”、“偏低”或“无影响”)。
(3)取a克 与
与 混合物进行下列三组实验,其中能测定
混合物进行下列三组实验,其中能测定 质量分数的是
质量分数的是________ (填序号)。
A.充分加热,质量减少b克
B.与足量稀盐酸充分反应,加热、蒸干,灼烧,得b克固体
C.与足量稀硫酸充分反应,逸出气体用氧化钙吸收,增重b克
 ,某兴趣小组研究加热情况下该膨松剂放出气体的量,设计实验的装置图如下。
,某兴趣小组研究加热情况下该膨松剂放出气体的量,设计实验的装置图如下。

已知:碱石灰是固体氢氧化钠和氧化钙的混合物:
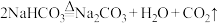 。
。(1)A装置中
 溶液的作用是除去空气中的
溶液的作用是除去空气中的(2)若没有E装置,测定的结果
(3)取a克
 与
与 混合物进行下列三组实验,其中能测定
混合物进行下列三组实验,其中能测定 质量分数的是
质量分数的是A.充分加热,质量减少b克
B.与足量稀盐酸充分反应,加热、蒸干,灼烧,得b克固体
C.与足量稀硫酸充分反应,逸出气体用氧化钙吸收,增重b克
您最近一年使用:0次
名校
9 . 氢叠氮酸( )和莫尔盐
)和莫尔盐 是两种常用原料。
是两种常用原料。
(1)氢叠氮酸易溶于水,25℃时,该酸的电离常数为
①氢叠氮酸在水溶液中的电离方程式为___________ 。
②0.1mol/L的 溶液与0.1mol/L的NaOH溶液等体积混合后,恢复到25℃时溶液中质子守恒关系式为
溶液与0.1mol/L的NaOH溶液等体积混合后,恢复到25℃时溶液中质子守恒关系式为___________ 。
③已知T℃时,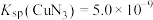 ,
, ,在此温度下,
,在此温度下,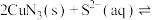
 ,该反应正反应方向
,该反应正反应方向___________ (填“能”或“不能”)基本进行彻底,请通过计算说明___________ 。
(2)在 溶液中,加入
溶液中,加入 固体可制备莫尔盐晶体,为了测定产品纯度,称取a g产品溶于水,配制成500mL溶液,用浓度为c mol/L的酸性高锰酸钾溶液滴定,每次所取待测液体积均为25.00mL,实验结果记录如下(已知莫尔盐的相对分子质量为392):
固体可制备莫尔盐晶体,为了测定产品纯度,称取a g产品溶于水,配制成500mL溶液,用浓度为c mol/L的酸性高锰酸钾溶液滴定,每次所取待测液体积均为25.00mL,实验结果记录如下(已知莫尔盐的相对分子质量为392):
滴定终点的现象是___________ ,通过实验数据,计算该产品的纯度为___________ (用含字母a、c的式子表示)。上表中第一次实验的记录数据明显大于后两次,其原因可能是___________ (填字母)。
A.第一次滴定时,锥形瓶用待装液润洗
B.该酸性高锰酸钾标准液保存时间过长,部分变质
C.滴定前酸式滴定管中尖嘴处有气泡,滴定结束后气泡消失
D.滴定前平视读数,滴定结束后俯视读数
 )和莫尔盐
)和莫尔盐 是两种常用原料。
是两种常用原料。(1)氢叠氮酸易溶于水,25℃时,该酸的电离常数为

①氢叠氮酸在水溶液中的电离方程式为
②0.1mol/L的
 溶液与0.1mol/L的NaOH溶液等体积混合后,恢复到25℃时溶液中质子守恒关系式为
溶液与0.1mol/L的NaOH溶液等体积混合后,恢复到25℃时溶液中质子守恒关系式为③已知T℃时,
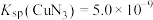 ,
, ,在此温度下,
,在此温度下,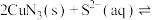
 ,该反应正反应方向
,该反应正反应方向(2)在
 溶液中,加入
溶液中,加入 固体可制备莫尔盐晶体,为了测定产品纯度,称取a g产品溶于水,配制成500mL溶液,用浓度为c mol/L的酸性高锰酸钾溶液滴定,每次所取待测液体积均为25.00mL,实验结果记录如下(已知莫尔盐的相对分子质量为392):
固体可制备莫尔盐晶体,为了测定产品纯度,称取a g产品溶于水,配制成500mL溶液,用浓度为c mol/L的酸性高锰酸钾溶液滴定,每次所取待测液体积均为25.00mL,实验结果记录如下(已知莫尔盐的相对分子质量为392):| 实验次数 | 第一次 | 第二次 | 第三次 |
消耗 溶液体积/mL 溶液体积/mL | 25.52 | 25.02 | 24.98 |
A.第一次滴定时,锥形瓶用待装液润洗
B.该酸性高锰酸钾标准液保存时间过长,部分变质
C.滴定前酸式滴定管中尖嘴处有气泡,滴定结束后气泡消失
D.滴定前平视读数,滴定结束后俯视读数
您最近一年使用:0次
10 . 在密闭容器中,通入a mol N2和b mol H2,若在一定条件下反应达到平衡时,容器中剩余c mol N2。
(1)达到平衡时,生成NH3的物质的量为_______
(2)若把容器的容积减小到原来的一半,则正反应速率_______ (填“增大”“减小”或“不变”,下同),逆反应速率_______ ,N2的转化率_______ 。
(1)达到平衡时,生成NH3的物质的量为
(2)若把容器的容积减小到原来的一半,则正反应速率
您最近一年使用:0次



