解题方法
1 . 通过实验探究发现化学反应中的某种规律,再寻求理论上的科学合理解释,是化学工作者的重要研究方法。
I.在体积可变的密闭容器中投入1 mol CO和2molH2,不同条件下发生反应:CO(g)+2H2(g) CH3OH(g)。实验测得平衡时CH3OH的物质的量随温度、压强的变化如图所示。
CH3OH(g)。实验测得平衡时CH3OH的物质的量随温度、压强的变化如图所示。

(1)M点H2的转化率为___________ ;反应速率N点v正(CO)___________ M点ν逆(CO)(填“>”“<”或“=”)
(2)若M点对应混合气体的体积为1L,则506K时,该反应平衡常数K=___________ (保留三位小数)。图表示平衡常数的对数(lgK)与温度的关系,B、C点中能正确表示该反应的lgK与T的关系的点为___________ 。

(3)在2L恒容密闭容器中充入a mol H2、2 mol CO和7.4 mol CH3OH(g),在506K下进行上述反应。为了使该反应逆向进行,a的取值范围为___________ 。
Ⅱ.砷及其化合物有着广泛的用途。砷有两种常见的弱酸,砷酸(H3AsO4)和亚砷酸(H3AsO3)。已知H3AsO4的pKa1、pKa2、pKa3依次为2.25、6.77、11.40(已知:pKa=-lgKa)。
回答下列问题:
(4)NaH2AsO4溶液呈___________ (填酸性”、“中性”或“碱性”),试通过计算说明___________ 。
(5)某小组同学欲探究可逆反应AsO33-+I2+2OH-⇌AsO43-+2I-+H2O,设计如图所示装置。加入试剂并连接装置,电流由C2流入C1。当电流变为零时,向装置左边烧杯中逐滴加入一定量2 mol/L HCl,发现又产生电流,实验中电流与时间的关系如图所示。

写出图4中c点对应的正极反应式___________ ,能判断该反应达到平衡状态的是___________ 。
a.2v(I-)正=v(AsO33-)逆b.溶液pH不再变化
c.电流表示数变为零d.右边烧杯中c(K+)不变
I.在体积可变的密闭容器中投入1 mol CO和2molH2,不同条件下发生反应:CO(g)+2H2(g)
 CH3OH(g)。实验测得平衡时CH3OH的物质的量随温度、压强的变化如图所示。
CH3OH(g)。实验测得平衡时CH3OH的物质的量随温度、压强的变化如图所示。
(1)M点H2的转化率为
(2)若M点对应混合气体的体积为1L,则506K时,该反应平衡常数K=

(3)在2L恒容密闭容器中充入a mol H2、2 mol CO和7.4 mol CH3OH(g),在506K下进行上述反应。为了使该反应逆向进行,a的取值范围为
Ⅱ.砷及其化合物有着广泛的用途。砷有两种常见的弱酸,砷酸(H3AsO4)和亚砷酸(H3AsO3)。已知H3AsO4的pKa1、pKa2、pKa3依次为2.25、6.77、11.40(已知:pKa=-lgKa)。
回答下列问题:
(4)NaH2AsO4溶液呈
(5)某小组同学欲探究可逆反应AsO33-+I2+2OH-⇌AsO43-+2I-+H2O,设计如图所示装置。加入试剂并连接装置,电流由C2流入C1。当电流变为零时,向装置左边烧杯中逐滴加入一定量2 mol/L HCl,发现又产生电流,实验中电流与时间的关系如图所示。

写出图4中c点对应的正极反应式
a.2v(I-)正=v(AsO33-)逆b.溶液pH不再变化
c.电流表示数变为零d.右边烧杯中c(K+)不变
您最近一年使用:0次
名校
解题方法
2 . 氮和硫的氧化物有多种,其中SO2和NOx都是大气污染物,对它们的研究有助于空气的净化。
(1)研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g) K1 ΔH1<0 (Ⅰ)
NaNO3(s)+ClNO(g) K1 ΔH1<0 (Ⅰ)
2NO(g)+Cl2(g) 2ClNO(g) K2 ΔH2<0 (Ⅱ)
2ClNO(g) K2 ΔH2<0 (Ⅱ)
则4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g) ΔH =
2NaNO3(s)+2NO(g)+Cl2(g) ΔH =________ (用ΔH1、ΔH2表示);平衡常数K=______ (用K1、K2表示)
(2)为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向2 L恒容密闭容器中加入0.2 mol NO和0.1 mol Cl2,10min时反应(Ⅱ)达到平衡。测得10min内v(ClNO)=7.5×10-3mol•L-1•min-1,NO的转化率α1=_______ 。其他条件保持不变,若反应(Ⅱ)在恒压条件下进行,平衡时NO的转化率α2____ α1(填“>”、“<”或“=”)。
(3)汽车使用乙醇汽油可减少石油的消耗,并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题。NO2尾气常用NaOH溶液吸收,生成NaNO3和 NaNO2 ,已知常温下NO2-的水解常数Kh=2×10-11 mol•L-1。 常温下某NaNO2和HNO2混合溶液的pH=5,则混合溶液中c(NO2-)和c(HNO2)的比值为_________ 。
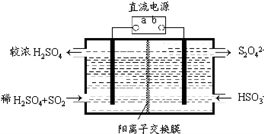
(4)利用右图所示装置(电极均为惰性电极)也可吸收SO2,并用阴极排出的溶液吸收NO2。阳极的电极反应式为_______________ 。在碱性条件下,用阴极排出的溶液吸收NO2,使其转化为无害气体N2,同时有SO42-生成。该应的离子方程式为___________________ 。
(5)某研究性学习小组欲探究SO2能否与BaCl2溶液反应生成BaSO3沉淀。查阅资料得知常温下BaSO3的Ksp=5.48×10-7,饱和亚硫酸中c(SO32-) =6.3×10-8 mol•L-1。将0.1 mol •L-1的BaCl2溶液滴入饱和亚硫酸中,_____ (填“能”、“不能”)生成BaSO3沉淀,原因是_______________________________ (写出推断过程)。
(1)研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s)
 NaNO3(s)+ClNO(g) K1 ΔH1<0 (Ⅰ)
NaNO3(s)+ClNO(g) K1 ΔH1<0 (Ⅰ)2NO(g)+Cl2(g)
 2ClNO(g) K2 ΔH2<0 (Ⅱ)
2ClNO(g) K2 ΔH2<0 (Ⅱ)则4NO2(g)+2NaCl(s)
 2NaNO3(s)+2NO(g)+Cl2(g) ΔH =
2NaNO3(s)+2NO(g)+Cl2(g) ΔH =(2)为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向2 L恒容密闭容器中加入0.2 mol NO和0.1 mol Cl2,10min时反应(Ⅱ)达到平衡。测得10min内v(ClNO)=7.5×10-3mol•L-1•min-1,NO的转化率α1=
(3)汽车使用乙醇汽油可减少石油的消耗,并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题。NO2尾气常用NaOH溶液吸收,生成NaNO3和 NaNO2 ,已知常温下NO2-的水解常数Kh=2×10-11 mol•L-1。 常温下某NaNO2和HNO2混合溶液的pH=5,则混合溶液中c(NO2-)和c(HNO2)的比值为
(4)利用右图所示装置(电极均为惰性电极)也可吸收SO2,并用阴极排出的溶液吸收NO2。阳极的电极反应式为

(5)某研究性学习小组欲探究SO2能否与BaCl2溶液反应生成BaSO3沉淀。查阅资料得知常温下BaSO3的Ksp=5.48×10-7,饱和亚硫酸中c(SO32-) =6.3×10-8 mol•L-1。将0.1 mol •L-1的BaCl2溶液滴入饱和亚硫酸中,
您最近一年使用:0次
2018-01-27更新
|
510次组卷
|
2卷引用:广东省肇庆市2018届高三第一学期二模化学试题
名校
3 . 磷单质及其化合物在工农业生产中有着广泛的应用。
(1)温度为T℃时,向2.0L恒容密闭容器中充入 ,发生反应
,发生反应 ,经过一段时间后达测平衡,反应过程中测定的部分数据如图。反应在前50s的平均速率
,经过一段时间后达测平衡,反应过程中测定的部分数据如图。反应在前50s的平均速率
___________ 。反应达到平衡后,升高温度,则v逆
________  填“增大”“减小”或“不变”
填“增大”“减小”或“不变” ,再次达到平衡后,
,再次达到平衡后, 的平衡浓度为
的平衡浓度为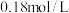 ,则反应
,则反应
_______  填“
填“ ”“
”“ ”或“
”或“ ”
”
(2)温度为T℃时,若平衡时体系的总压强为p,该反应的平衡常数
________ 。 用平衡分压代替平衡浓度计算,分压
用平衡分压代替平衡浓度计算,分压 总压
总压 物质的量分数
物质的量分数
(3)温度为T℃时,上述反应若在恒压容器中进行,则达到平衡后, 的物质的量
的物质的量_________  填“大于”“小于”或“等于”
填“大于”“小于”或“等于” 。
。
(4)已知 水解可生成亚磷酸
水解可生成亚磷酸 。常温下,
。常温下, 的
的 溶液的
溶液的 ,亚磷酸与足量的NaOH溶液反应生成
,亚磷酸与足量的NaOH溶液反应生成 。则
。则 的
的 溶液中各离子浓度由大到小的顺序是
溶液中各离子浓度由大到小的顺序是________ 。
(5)亚磷酸具有强还原性,可被氧化为 。
。 与NaOH溶液反应,反应混合物中含磷各微粒的分布分数
与NaOH溶液反应,反应混合物中含磷各微粒的分布分数 平衡时某微粒的浓度占微粒浓度之和的分数
平衡时某微粒的浓度占微粒浓度之和的分数 与pH的关系如图所示。
与pH的关系如图所示。
①为获得尽可能纯的 ,pH应控制在
,pH应控制在___________ 。
②已知:25℃时, ,
, ,
, ,则
,则 时,溶液中
时,溶液中
___________ 。
(1)温度为T℃时,向2.0L恒容密闭容器中充入
 ,发生反应
,发生反应 ,经过一段时间后达测平衡,反应过程中测定的部分数据如图。反应在前50s的平均速率
,经过一段时间后达测平衡,反应过程中测定的部分数据如图。反应在前50s的平均速率

 填“增大”“减小”或“不变”
填“增大”“减小”或“不变” ,再次达到平衡后,
,再次达到平衡后, 的平衡浓度为
的平衡浓度为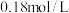 ,则反应
,则反应
 填“
填“ ”“
”“ ”或“
”或“ ”
”

(2)温度为T℃时,若平衡时体系的总压强为p,该反应的平衡常数

 用平衡分压代替平衡浓度计算,分压
用平衡分压代替平衡浓度计算,分压 总压
总压 物质的量分数
物质的量分数
(3)温度为T℃时,上述反应若在恒压容器中进行,则达到平衡后,
 的物质的量
的物质的量 填“大于”“小于”或“等于”
填“大于”“小于”或“等于” 。
。(4)已知
 水解可生成亚磷酸
水解可生成亚磷酸 。常温下,
。常温下, 的
的 溶液的
溶液的 ,亚磷酸与足量的NaOH溶液反应生成
,亚磷酸与足量的NaOH溶液反应生成 。则
。则 的
的 溶液中各离子浓度由大到小的顺序是
溶液中各离子浓度由大到小的顺序是(5)亚磷酸具有强还原性,可被氧化为
 。
。 与NaOH溶液反应,反应混合物中含磷各微粒的分布分数
与NaOH溶液反应,反应混合物中含磷各微粒的分布分数 平衡时某微粒的浓度占微粒浓度之和的分数
平衡时某微粒的浓度占微粒浓度之和的分数 与pH的关系如图所示。
与pH的关系如图所示。
①为获得尽可能纯的
 ,pH应控制在
,pH应控制在②已知:25℃时,
 ,
, ,
, ,则
,则 时,溶液中
时,溶液中
您最近一年使用:0次
2020-02-26更新
|
162次组卷
|
2卷引用:2019-2020广东省广州市广州中学高三10月考试化学试卷
名校
解题方法
4 . 化学平衡、电离平衡、水解平衡和溶解平衡均符合勒夏特列原理。
(1)高温下,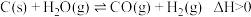 ,反应的化学平衡常数表达式
,反应的化学平衡常数表达式
_______ ,该反应随温度升高,K值_______ (填“增大”、“减小”或“不变”)。
(2)已知常温下部分弱电解质的电离平衡常数如下表:
①常温下,物质的量浓度相同的三种溶液①NaF溶液;②NaClO溶液;③ 溶液,其pH由大到小的顺序是
溶液,其pH由大到小的顺序是_______ (填序号)
②0.1mol/L的NaClO溶液和0.1mol/L的 溶液中,
溶液中,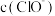
_______ 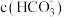 (填“>”“<”或“=”)
(填“>”“<”或“=”)
③常温下,0.1mol/L的氨水和0.1mol/L的 溶液等体积混合,判断混合溶液的酸碱性
溶液等体积混合,判断混合溶液的酸碱性_______ (填“酸性”“碱性”“中性”)
(3)已知几种离子开始沉淀时溶液的pH如下表所示:
当向含有相同浓度的 、
、 、
、 的溶液中滴加氢氧化钠溶液时,
的溶液中滴加氢氧化钠溶液时,_______ (填离子符号)先沉淀;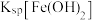
_______ (填“>”“=”或“<”)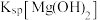 ;要使
;要使 的硫酸铜溶液中铜离子沉淀较完全(使铜离子的浓度降至原来的千分之一),则应向溶液中加入氢氧化钠使溶液
的硫酸铜溶液中铜离子沉淀较完全(使铜离子的浓度降至原来的千分之一),则应向溶液中加入氢氧化钠使溶液
_______ 。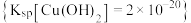
(1)高温下,
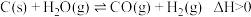 ,反应的化学平衡常数表达式
,反应的化学平衡常数表达式
(2)已知常温下部分弱电解质的电离平衡常数如下表:
| 化学式 | HF | HClO |  |  |
| 电离常数 | 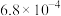 | 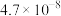 |  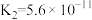 | 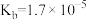 |
①常温下,物质的量浓度相同的三种溶液①NaF溶液;②NaClO溶液;③
 溶液,其pH由大到小的顺序是
溶液,其pH由大到小的顺序是②0.1mol/L的NaClO溶液和0.1mol/L的
 溶液中,
溶液中,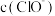
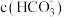 (填“>”“<”或“=”)
(填“>”“<”或“=”)③常温下,0.1mol/L的氨水和0.1mol/L的
 溶液等体积混合,判断混合溶液的酸碱性
溶液等体积混合,判断混合溶液的酸碱性(3)已知几种离子开始沉淀时溶液的pH如下表所示:
| 离子 |  |  |  |
| pH | 7.6 | 5.2 | 10.4 |
当向含有相同浓度的
 、
、 、
、 的溶液中滴加氢氧化钠溶液时,
的溶液中滴加氢氧化钠溶液时,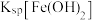
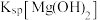 ;要使
;要使 的硫酸铜溶液中铜离子沉淀较完全(使铜离子的浓度降至原来的千分之一),则应向溶液中加入氢氧化钠使溶液
的硫酸铜溶液中铜离子沉淀较完全(使铜离子的浓度降至原来的千分之一),则应向溶液中加入氢氧化钠使溶液
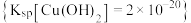
您最近一年使用:0次
解题方法
5 . 丙烯(C3H6)是重要的有机化工原料。丙烷脱氢制丙烯发生的主要反应及能量变化如下图。
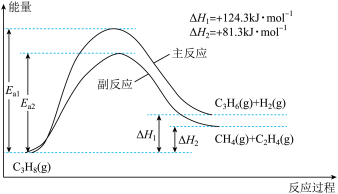
(1)丙烷脱氢制丙烯为强吸热过程。
①为提供反应所需热量,恒压时若向原料气中掺入水蒸气,则K(主反应)____ (填“增大”、“减小”或“不变”,下同),转化率α(C3H8)_____ 。
②温度升高,副反应更容易发生的主要原因是__________________________________ 。
(2)下图为丙烷直接脱氢法中丙烷和丙烯的平衡体积分数与温度、压强的关系(图中的压强分
别为104 Pa和105 Pa)。
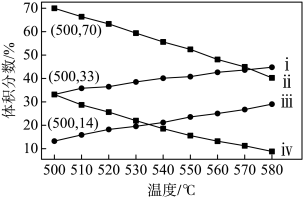
①104 Pa时,图中表示丙烯的曲线是____ (填“ⅰ”、“ⅱ”、“ⅲ”或“ⅳ”)。
②104 Pa、500 ℃时,主反应用平衡分压代替平衡浓度表示的化学平衡常数Kp=_____ (已知:气体分压=气体总压×体积分数)。
(3)利用CO2的弱氧化性,开发了丙烷氧化脱氢制丙烯的新工艺。
该工艺可采用铬的氧化物为催化剂,其反应机理如图。
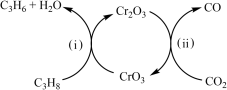
已知:CO和H2的燃烧热分别为△H =-283.0 kJ·mol-1、△H =-285.8 kJ·mol-1。
①图中催化剂为______ 。
②298 K 时,该工艺总反应的热化学方程式为_____________________________________ 。
③该工艺可以有效消除催化剂表面的积炭,维持催化剂活性,原因是__________ 。

(1)丙烷脱氢制丙烯为强吸热过程。
①为提供反应所需热量,恒压时若向原料气中掺入水蒸气,则K(主反应)
②温度升高,副反应更容易发生的主要原因是
(2)下图为丙烷直接脱氢法中丙烷和丙烯的平衡体积分数与温度、压强的关系(图中的压强分
别为104 Pa和105 Pa)。

①104 Pa时,图中表示丙烯的曲线是
②104 Pa、500 ℃时,主反应用平衡分压代替平衡浓度表示的化学平衡常数Kp=
(3)利用CO2的弱氧化性,开发了丙烷氧化脱氢制丙烯的新工艺。
该工艺可采用铬的氧化物为催化剂,其反应机理如图。

已知:CO和H2的燃烧热分别为△H =-283.0 kJ·mol-1、△H =-285.8 kJ·mol-1。
①图中催化剂为
②298 K 时,该工艺总反应的热化学方程式为
③该工艺可以有效消除催化剂表面的积炭,维持催化剂活性,原因是
您最近一年使用:0次
6 . [2017·新课标I]近期发现,H2S是继NO、CO之后的第三个生命体系气体信号分子,它具有参与调节神经信号传递、舒张血管减轻高血压的功能。回答下列问题:
(1)下列事实中,不能比较氢硫酸与亚硫酸的酸性强弱的是_________ (填标号)。
A.氢硫酸不能与碳酸氢钠溶液反应,而亚硫酸可以
B.氢硫酸的导电能力低于相同浓度的亚硫酸
C.0.10 mol·L−1的氢硫酸和亚硫酸的pH分别为4.5和2.1
D.氢硫酸的还原性强于亚硫酸
(2)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。______________ 、______________ ,制得等量H2所需能量较少的是_____________ 。 =
=_______ %,反应平衡常数K=________ 。
②在620 K重复试验,平衡后水的物质的量分数为0.03,H2S的转化率
_____  ,该反应的
,该反应的 H
H_____ 0。(填“>”“<”或“=”)
③向反应器中再分别充入下列气体,能使H2S转化率增大的是________ (填标号)
A.H2S B.CO2 C.COS D.N2
(1)下列事实中,不能比较氢硫酸与亚硫酸的酸性强弱的是
A.氢硫酸不能与碳酸氢钠溶液反应,而亚硫酸可以
B.氢硫酸的导电能力低于相同浓度的亚硫酸
C.0.10 mol·L−1的氢硫酸和亚硫酸的pH分别为4.5和2.1
D.氢硫酸的还原性强于亚硫酸
(2)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。

(3)H2S与CO2在高温下发生反应:H2S(g)+CO2(g) COS(g) +H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
COS(g) +H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
 =
=②在620 K重复试验,平衡后水的物质的量分数为0.03,H2S的转化率

 ,该反应的
,该反应的 H
H③向反应器中再分别充入下列气体,能使H2S转化率增大的是
A.H2S B.CO2 C.COS D.N2
您最近一年使用:0次
2017-08-09更新
|
10921次组卷
|
10卷引用:2018届广东省揭阳市高三上学期第一次月考化学试题
2018届广东省揭阳市高三上学期第一次月考化学试题【市级联考】广东省化州市2019年高三上学期第二次模拟考试理科综合化学试题广东省江门市新会区陈经纶中学2022-2023学年高二上学期第5段月考化学试题2017年全国普通高等学校招生统一考试理综化学(新课标Ⅰ卷精编版)河北省唐山市第一中学2017-2018学年高二上学期第一次月考化学试题重庆市第二中学2018届高三3月测试化学试题(已下线)《考前20天终极攻略》-5月29日 化学反应原理综合(已下线)解密20 原理综合题(教师版)——备战2018年高考化学之高频考点解密云南省大理白族自治州祥云县第一中学2020届高三下学期4月月考理综化学试题重庆十八中两江实验中学校2022-2023学年高二上学期第一次月考化学试题



