名校
解题方法
1 . 绿色甲醇 是2023年杭州亚运会主火炬燃料,制备绿色甲醇分为三个阶段:利用可再生能源制绿氢、
是2023年杭州亚运会主火炬燃料,制备绿色甲醇分为三个阶段:利用可再生能源制绿氢、 的捕集、
的捕集、 和
和 一步法制甲醇。
一步法制甲醇。
(1)磁场辅助光电分解水制氢的工作原理如下[磁场辅助光照电极材料促使单位时间内产生更多的“电子”和“空穴”( ,具有强氧化性),驱动并加快电极反应]。
,具有强氧化性),驱动并加快电极反应]。
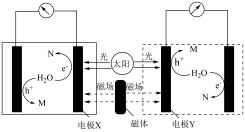
①电极X为______ (填“阴”或“阳”)极。
②理论上生成的气体M与N的质量之比为______ 。
③在酸性介质中生成M的电极反应式为______ 。
(2)工业上从高炉气中捕集 的示意图如图所示。
的示意图如图所示。
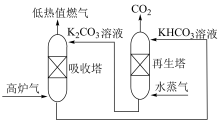
①高炉气从“吸收塔”底部通入, 溶液从塔顶喷洒,这样做的优点是
溶液从塔顶喷洒,这样做的优点是____________ 。
②若从“吸收塔”出来的盐溶液中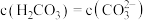 ,则该溶液的pH为
,则该溶液的pH为______
[该条件下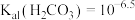 、
、 ,不考虑其他因素对pH的影响]。
,不考虑其他因素对pH的影响]。
③为研究温度对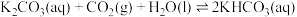 的影响,将一定量的
的影响,将一定量的 溶液置于密闭容器中,并充入一定量的
溶液置于密闭容器中,并充入一定量的 气体,保持其他初始实验条件不变,分别在不同温度下,经过相同时间测得
气体,保持其他初始实验条件不变,分别在不同温度下,经过相同时间测得 气体的浓度如图所示:
气体的浓度如图所示:
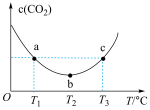
化学平衡常数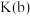
______ 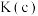 (填“>”“<”或“=”);
(填“>”“<”或“=”); 温度范围内,容器内
温度范围内,容器内 气体浓度呈减小的趋势,其原因是
气体浓度呈减小的趋势,其原因是______ 。
 是2023年杭州亚运会主火炬燃料,制备绿色甲醇分为三个阶段:利用可再生能源制绿氢、
是2023年杭州亚运会主火炬燃料,制备绿色甲醇分为三个阶段:利用可再生能源制绿氢、 的捕集、
的捕集、 和
和 一步法制甲醇。
一步法制甲醇。(1)磁场辅助光电分解水制氢的工作原理如下[磁场辅助光照电极材料促使单位时间内产生更多的“电子”和“空穴”(
 ,具有强氧化性),驱动并加快电极反应]。
,具有强氧化性),驱动并加快电极反应]。
①电极X为
②理论上生成的气体M与N的质量之比为
③在酸性介质中生成M的电极反应式为
(2)工业上从高炉气中捕集
 的示意图如图所示。
的示意图如图所示。
①高炉气从“吸收塔”底部通入,
 溶液从塔顶喷洒,这样做的优点是
溶液从塔顶喷洒,这样做的优点是②若从“吸收塔”出来的盐溶液中
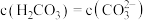 ,则该溶液的pH为
,则该溶液的pH为[该条件下
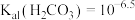 、
、 ,不考虑其他因素对pH的影响]。
,不考虑其他因素对pH的影响]。③为研究温度对
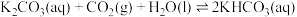 的影响,将一定量的
的影响,将一定量的 溶液置于密闭容器中,并充入一定量的
溶液置于密闭容器中,并充入一定量的 气体,保持其他初始实验条件不变,分别在不同温度下,经过相同时间测得
气体,保持其他初始实验条件不变,分别在不同温度下,经过相同时间测得 气体的浓度如图所示:
气体的浓度如图所示:
化学平衡常数
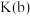
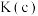 (填“>”“<”或“=”);
(填“>”“<”或“=”); 温度范围内,容器内
温度范围内,容器内 气体浓度呈减小的趋势,其原因是
气体浓度呈减小的趋势,其原因是
您最近一年使用:0次
2023-12-13更新
|
314次组卷
|
3卷引用:陕西省安康市高新中学2023-2024学年高三上学期阶段性测试四化学试题
解题方法
2 . 烟气脱硫脱硝技术是烟气治理的发展方向和研究热点,有着广泛的应用前景。
(1)可用NH3选择性脱除氮氧化物,已知:
①N2(g)+O2(g)=2NO(g) ∆H1=+180kJ∙mol-1
②4NH3(g)+5O2(g)=4NO(g)+6H2O(l) ∆H2=-1170kJ∙mol-1
③6NO(g)+4NH3(g)=5N2(g)+6H2O(l) ∆H3
则∆H3=_____ kJ∙mol-1
(2)目前,科学家正在研究一种以乙烯作还原剂的脱硝(NO)原理,其脱硝机理如图1所示,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2所示。

①写出该脱硝原理总反应的化学方程式:_____ 。
②为达到最佳的脱硝效果,应采取的条件为_____ (填温度和负载率)。
(3)用酸性KMnO4及添加物浆液也可高效脱除烟气中的NO和SO2.脱除NO时,NO被氧化为 ,
, 被还原为Mn2+,该反应的离子方程式为
被还原为Mn2+,该反应的离子方程式为_____ 。
(4)反应2NO(g)+O2(g)⇌2NO2(g) ∆H4=-112.3kJ∙mol-1,是由以下两步反应完成的:
I.____ ∆H5<0;
II.N2O2(g)+O2(g)⇌2NO2(g) ∆H6<0。
①第I步反应的化学方程式为___
②∆H5___ (填“>”、“=”或“<”,下同)-112.3kJ∙mol-1;若第I步反应为快反应,则活化能E(I)__ E(II)。
③若反应2NO(g)+O2⇌2NO2(g)的正、逆反应速率分别为v正=k正×c2(NO)∙c(O2)、v逆=k逆×c2(NO2),则该反应的化学平衡常数k=_______ (用含k正和k逆的代数式表示)。
(1)可用NH3选择性脱除氮氧化物,已知:
①N2(g)+O2(g)=2NO(g) ∆H1=+180kJ∙mol-1
②4NH3(g)+5O2(g)=4NO(g)+6H2O(l) ∆H2=-1170kJ∙mol-1
③6NO(g)+4NH3(g)=5N2(g)+6H2O(l) ∆H3
则∆H3=
(2)目前,科学家正在研究一种以乙烯作还原剂的脱硝(NO)原理,其脱硝机理如图1所示,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2所示。

①写出该脱硝原理总反应的化学方程式:
②为达到最佳的脱硝效果,应采取的条件为
(3)用酸性KMnO4及添加物浆液也可高效脱除烟气中的NO和SO2.脱除NO时,NO被氧化为
 ,
, 被还原为Mn2+,该反应的离子方程式为
被还原为Mn2+,该反应的离子方程式为(4)反应2NO(g)+O2(g)⇌2NO2(g) ∆H4=-112.3kJ∙mol-1,是由以下两步反应完成的:
I.____ ∆H5<0;
II.N2O2(g)+O2(g)⇌2NO2(g) ∆H6<0。
①第I步反应的化学方程式为
②∆H5
③若反应2NO(g)+O2⇌2NO2(g)的正、逆反应速率分别为v正=k正×c2(NO)∙c(O2)、v逆=k逆×c2(NO2),则该反应的化学平衡常数k=
您最近一年使用:0次



