1 . 高纯度 可用作玻璃擦光剂、搪瓷抛光剂、催化剂等。利用水解反应制备高纯度
可用作玻璃擦光剂、搪瓷抛光剂、催化剂等。利用水解反应制备高纯度 的原理为
的原理为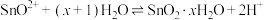 。某温度下,测得体系中
。某温度下,测得体系中 、
、 (
( 电离产生的
电离产生的 不考虑)与时间的关系如图所示。下列叙述正确的是
不考虑)与时间的关系如图所示。下列叙述正确的是
 可用作玻璃擦光剂、搪瓷抛光剂、催化剂等。利用水解反应制备高纯度
可用作玻璃擦光剂、搪瓷抛光剂、催化剂等。利用水解反应制备高纯度 的原理为
的原理为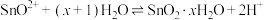 。某温度下,测得体系中
。某温度下,测得体系中 、
、 (
( 电离产生的
电离产生的 不考虑)与时间的关系如图所示。下列叙述正确的是
不考虑)与时间的关系如图所示。下列叙述正确的是
| A.正反应速率:a>c | B.平衡后增大 ,平衡常数K减小 ,平衡常数K减小 |
| C.b点时水解反应已停止 | D. |
您最近一年使用:0次
2 . 二氧化碳与氢气在一定条件下可制备甲醛(HCHO)、甲酸(HCOOH)和甲醇( )等有机物。回答下列问题:
)等有机物。回答下列问题:
(1)制备甲醛:反应机理如下图所示
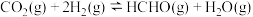

___________ (用 、
、 、
、 、
、 表示)。
表示)。
②将等物质的量的 与
与 充入恒温恒容密闭容器中发生反应
充入恒温恒容密闭容器中发生反应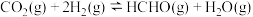 ,下列描述不能说明该反应达到平衡状态的是
,下列描述不能说明该反应达到平衡状态的是___________ (填字母)。
a. 的物质的量保持不变
的物质的量保持不变
b.单位时间内,断裂2molH—H键的同时断裂2molC—H键
C. 不再发生变化
不再发生变化
d.容器内混合气体的密度保持不变
(2)制备甲酸:反应原理为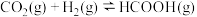
 。已知:
。已知: ,
, ,
, 、
、 为速率常数,
为速率常数,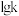 与温度的关系如下图所示。
与温度的关系如下图所示。
___________ (填“增大”“减小”或“不变”);该反应的
___________ (填“ ”“
”“ ”或“
”或“ ”)0。
”)0。
②向某恒容密闭容器中加入物质的量均为1mol的 和
和 发生该反应,
发生该反应, 时平衡常数为20、平衡压强为
时平衡常数为20、平衡压强为 ,若温度为
,若温度为 时,
时, ,则
,则 时的平衡压强
时的平衡压强___________ (填“ ”“
”“ ”或“
”或“ ”)
”) 。
。
(3)近年来,有研究人员用 通过电催化生成
通过电催化生成 ,实现
,实现 的回收利用,其工作原理如下图所示。写出Cu电极上的电极反应式:
的回收利用,其工作原理如下图所示。写出Cu电极上的电极反应式:___________ 。 用于制备苯乙烯有助于实现“碳中和”。
用于制备苯乙烯有助于实现“碳中和”。 参与反应的机理如上图所示(
参与反应的机理如上图所示( 、
、 表示乙苯分子中C或H原子的位置;AB为催化剂的活性位点,其中A位点带部分正电荷,
表示乙苯分子中C或H原子的位置;AB为催化剂的活性位点,其中A位点带部分正电荷, 、
、 位点带部分负电荷)。根据元素电负性的变化规律,上图所示的反应机理中步骤Ⅰ和步骤Ⅱ可描述为乙苯
位点带部分负电荷)。根据元素电负性的变化规律,上图所示的反应机理中步骤Ⅰ和步骤Ⅱ可描述为乙苯 带部分正电荷,被带部分负电荷的
带部分正电荷,被带部分负电荷的 位点吸引,随后解离出
位点吸引,随后解离出 并吸附在
并吸附在 位点上;
位点上;___________ 。
②保持混合气体总压(p)等其他条件不变, 的分压
的分压 与乙苯转化率的关系如下图所示。
与乙苯转化率的关系如下图所示。 时,乙苯转化率下降的原因是
时,乙苯转化率下降的原因是___________ 。
 )等有机物。回答下列问题:
)等有机物。回答下列问题:(1)制备甲醛:反应机理如下图所示


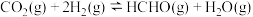

 、
、 、
、 、
、 表示)。
表示)。②将等物质的量的
 与
与 充入恒温恒容密闭容器中发生反应
充入恒温恒容密闭容器中发生反应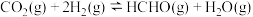 ,下列描述不能说明该反应达到平衡状态的是
,下列描述不能说明该反应达到平衡状态的是a.
 的物质的量保持不变
的物质的量保持不变b.单位时间内,断裂2molH—H键的同时断裂2molC—H键
C.
 不再发生变化
不再发生变化d.容器内混合气体的密度保持不变
(2)制备甲酸:反应原理为
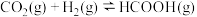
 。已知:
。已知: ,
, ,
, 、
、 为速率常数,
为速率常数,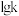 与温度的关系如下图所示。
与温度的关系如下图所示。


 ”“
”“ ”或“
”或“ ”)0。
”)0。②向某恒容密闭容器中加入物质的量均为1mol的
 和
和 发生该反应,
发生该反应, 时平衡常数为20、平衡压强为
时平衡常数为20、平衡压强为 ,若温度为
,若温度为 时,
时, ,则
,则 时的平衡压强
时的平衡压强 ”“
”“ ”或“
”或“ ”)
”) 。
。(3)近年来,有研究人员用
 通过电催化生成
通过电催化生成 ,实现
,实现 的回收利用,其工作原理如下图所示。写出Cu电极上的电极反应式:
的回收利用,其工作原理如下图所示。写出Cu电极上的电极反应式:
 用于制备苯乙烯有助于实现“碳中和”。
用于制备苯乙烯有助于实现“碳中和”。
 参与反应的机理如上图所示(
参与反应的机理如上图所示( 、
、 表示乙苯分子中C或H原子的位置;AB为催化剂的活性位点,其中A位点带部分正电荷,
表示乙苯分子中C或H原子的位置;AB为催化剂的活性位点,其中A位点带部分正电荷, 、
、 位点带部分负电荷)。根据元素电负性的变化规律,上图所示的反应机理中步骤Ⅰ和步骤Ⅱ可描述为乙苯
位点带部分负电荷)。根据元素电负性的变化规律,上图所示的反应机理中步骤Ⅰ和步骤Ⅱ可描述为乙苯 带部分正电荷,被带部分负电荷的
带部分正电荷,被带部分负电荷的 位点吸引,随后解离出
位点吸引,随后解离出 并吸附在
并吸附在 位点上;
位点上;②保持混合气体总压(p)等其他条件不变,
 的分压
的分压 与乙苯转化率的关系如下图所示。
与乙苯转化率的关系如下图所示。 时,乙苯转化率下降的原因是
时,乙苯转化率下降的原因是
您最近一年使用:0次
名校
3 . 水气变换反应(CO+H2O H2+CO2)是工业上大规模制氢的重要方法,HCOOH是中间产物。研究发现,在反应
H2+CO2)是工业上大规模制氢的重要方法,HCOOH是中间产物。研究发现,在反应 、
、 中,
中, 仅对反应
仅对反应 有催化加速作用;反应
有催化加速作用;反应 速率远大于反应Ⅱ,近似认为反应
速率远大于反应Ⅱ,近似认为反应 建立平衡后始终处于平衡状态,T°C下,在密封石英管内完全充满1.0mol/LHCOOH水溶液,分解产物均完全溶于水中,发生如下反应:
建立平衡后始终处于平衡状态,T°C下,在密封石英管内完全充满1.0mol/LHCOOH水溶液,分解产物均完全溶于水中,发生如下反应:
Ⅰ.HCOOH(aq) CO(aq)+H2O(1)
CO(aq)+H2O(1)
Ⅱ.HCOOH(aq) CO2(aq)+H2(aq)
CO2(aq)+H2(aq)
含碳粒子浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式):
 H2+CO2)是工业上大规模制氢的重要方法,HCOOH是中间产物。研究发现,在反应
H2+CO2)是工业上大规模制氢的重要方法,HCOOH是中间产物。研究发现,在反应 、
、 中,
中, 仅对反应
仅对反应 有催化加速作用;反应
有催化加速作用;反应 速率远大于反应Ⅱ,近似认为反应
速率远大于反应Ⅱ,近似认为反应 建立平衡后始终处于平衡状态,T°C下,在密封石英管内完全充满1.0mol/LHCOOH水溶液,分解产物均完全溶于水中,发生如下反应:
建立平衡后始终处于平衡状态,T°C下,在密封石英管内完全充满1.0mol/LHCOOH水溶液,分解产物均完全溶于水中,发生如下反应:Ⅰ.HCOOH(aq)
 CO(aq)+H2O(1)
CO(aq)+H2O(1)Ⅱ.HCOOH(aq)
 CO2(aq)+H2(aq)
CO2(aq)+H2(aq)含碳粒子浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式):
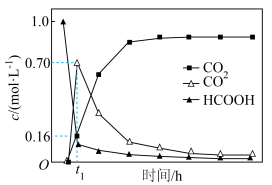
A.反应 活化能大于反应 活化能大于反应 |
| B.混合体系达平衡后:c(CO)+c(CO2)=1.0mol/L |
C. 时,反应 时,反应 正反应速率<逆反应速率 正反应速率<逆反应速率 |
D.若在起始溶液中加入盐酸,则CO达浓度峰值时, 的值与未加盐酸时相同 的值与未加盐酸时相同 |
您最近一年使用:0次
4 . SiHCl3被应用于制造多晶硅及硅烷偶联剂等领域。50℃时将nmolSiHCl3置于密闭容器中发生如下反应: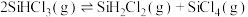 ,SiHCl3的转化率随时间变化的曲线如下图所示。下列说法正确的是
,SiHCl3的转化率随时间变化的曲线如下图所示。下列说法正确的是
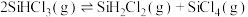 ,SiHCl3的转化率随时间变化的曲线如下图所示。下列说法正确的是
,SiHCl3的转化率随时间变化的曲线如下图所示。下列说法正确的是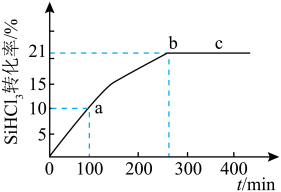
| A.SiH2Cl2和SiCl4均为由极性键构成的非极性分子 |
B.0~100min内,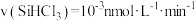 |
C.50℃时该反应的平衡常数 |
| D.b-c段平均速率大于a-b段平均速率 |
您最近一年使用:0次
名校
5 . 常温下向 的混合液中滴加
的混合液中滴加 溶液,混合液中
溶液,混合液中 与
与 的关系如图所示,
的关系如图所示, 或
或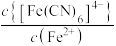 或
或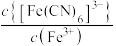 。下列叙述正确的是
。下列叙述正确的是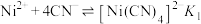 ;
;
② ;
;
③ ,且
,且 。
。
 的混合液中滴加
的混合液中滴加 溶液,混合液中
溶液,混合液中 与
与 的关系如图所示,
的关系如图所示, 或
或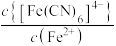 或
或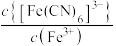 。下列叙述正确的是
。下列叙述正确的是
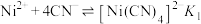 ;
;②
 ;
;③
 ,且
,且 。
。A.直线a代表 与 与 的关系 的关系 |
B.平衡常数 的数量级为 的数量级为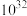 |
C.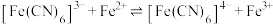 不易发生 不易发生 |
D.向含相同浓度的 和 和 的溶液中滴加 的溶液中滴加 溶液,先生成 溶液,先生成 |
您最近一年使用:0次
7日内更新
|
98次组卷
|
2卷引用:2024届重庆市南开中学校高三下学期5月月考化学试题
名校
6 . 工业上用 生产甲醇的反应为
生产甲醇的反应为 。在一定条件下的密闭容器中,分别充入
。在一定条件下的密闭容器中,分别充入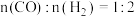 的混合气体,
的混合气体, 的平衡转化率与温度、压强的关系如图所示:
的平衡转化率与温度、压强的关系如图所示:
 生产甲醇的反应为
生产甲醇的反应为 。在一定条件下的密闭容器中,分别充入
。在一定条件下的密闭容器中,分别充入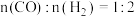 的混合气体,
的混合气体, 的平衡转化率与温度、压强的关系如图所示:
的平衡转化率与温度、压强的关系如图所示:
A. |
B.压强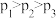 |
C.a、b点的平衡常数: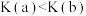 |
| D.体系中气体的总物质的量不变时,反应达到平衡 |
您最近一年使用:0次
7 . 工业上常用 除去
除去 :
: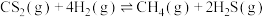 。一定温度下,向恒容反应器中按照不同投料(见下表)充入气体。按照①进行投料时,测得体系中各成分的物质的量随时间变化如图所示。
。一定温度下,向恒容反应器中按照不同投料(见下表)充入气体。按照①进行投料时,测得体系中各成分的物质的量随时间变化如图所示。
不正确 的是
 除去
除去 :
: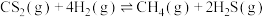 。一定温度下,向恒容反应器中按照不同投料(见下表)充入气体。按照①进行投料时,测得体系中各成分的物质的量随时间变化如图所示。
。一定温度下,向恒容反应器中按照不同投料(见下表)充入气体。按照①进行投料时,测得体系中各成分的物质的量随时间变化如图所示。| 投料 | 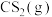 |  |  | 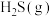 |
| ① |  |  | 0 | 0 |
| ② |  |  | 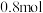 |  |
| ③ |  |  | 0 | 0 |

A.图中 对应的物质是 对应的物质是 | B.①中达到平衡时, |
| C.按照②进行投料时,反应向逆反应方向进行 | D.任意时刻③中 的体积分数均为 的体积分数均为 |
您最近一年使用:0次
8 .  稀溶液中存在如下平衡:
稀溶液中存在如下平衡:
Ⅰ.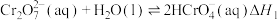
Ⅱ.
关于该溶液的说法不正确 的是(温度变化忽略不计)
 稀溶液中存在如下平衡:
稀溶液中存在如下平衡:Ⅰ.
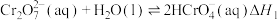
Ⅱ.

关于该溶液的说法
| A.加水稀释,溶液中离子总数增加 |
B.加入少量浓 溶液,Ⅰ和Ⅱ均向正反应方向移动 溶液,Ⅰ和Ⅱ均向正反应方向移动 |
C.加入少量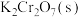 ,溶液颜色不再变化时, ,溶液颜色不再变化时,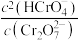 比原溶液中的小 比原溶液中的小 |
D.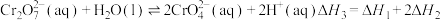 |
您最近一年使用:0次
9 . 反应 可用于去除氮氧化物。
可用于去除氮氧化物。 催化该反应的过程如图所示。下列说法不正确的是
催化该反应的过程如图所示。下列说法不正确的是
 可用于去除氮氧化物。
可用于去除氮氧化物。 催化该反应的过程如图所示。下列说法不正确的是
催化该反应的过程如图所示。下列说法不正确的是
A.反应过程中, 参与反应,降低了反应的焓变 参与反应,降低了反应的焓变 |
B.该反应的平衡常数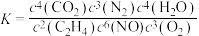 |
C.其他条件不变时,增大 ,NO的平衡转化率增大 ,NO的平衡转化率增大 |
D.步骤Ⅲ中每消耗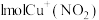 ,转移电子数目为 ,转移电子数目为 |
您最近一年使用:0次
解题方法
10 . 在一定条件下,将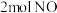 和
和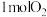 通入恒容密闭容器中进行反应,容器中发生两个反应
通入恒容密闭容器中进行反应,容器中发生两个反应 和
和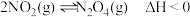 。在不同温度下,测得平衡时体系中
。在不同温度下,测得平衡时体系中 的物质的量与温度的关系如图所示。下列说法正确的是
的物质的量与温度的关系如图所示。下列说法正确的是
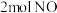 和
和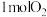 通入恒容密闭容器中进行反应,容器中发生两个反应
通入恒容密闭容器中进行反应,容器中发生两个反应 和
和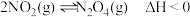 。在不同温度下,测得平衡时体系中
。在不同温度下,测得平衡时体系中 的物质的量与温度的关系如图所示。下列说法正确的是
的物质的量与温度的关系如图所示。下列说法正确的是
A.曲线c代表 的物质的量与温度的关系 的物质的量与温度的关系 |
B.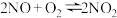 的平衡常数 的平衡常数 (x点) (x点)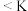 (y点) (y点) |
C.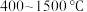 时,随着温度升高, 时,随着温度升高, 的体积分数不断增大 的体积分数不断增大 |
| D.一定温度下,当恒容密闭容器中混合气体的压强不再改变时,反应体系达到平衡状态 |
您最近一年使用:0次



