1 . 某温度下,若反应
 的化学平衡常数K1=25,则该温度下HI(g)⇌
的化学平衡常数K1=25,则该温度下HI(g)⇌ H2(g)+
H2(g)+ I2(g)的化学平衡常数K2为
I2(g)的化学平衡常数K2为
| A.0.2 | B.0.4 | C.0.004 | D.5 |
您最近一年使用:0次
解题方法
2 . 在容积不变的密闭容器中,一定量的 与
与 发生反应:
发生反应: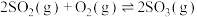 。温度分别为
。温度分别为 和
和 时,
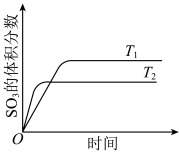
时,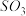 的体积分数随时间的变化如图所示。下列判断错误的是
的体积分数随时间的变化如图所示。下列判断错误的是
 与
与 发生反应:
发生反应: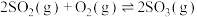 。温度分别为
。温度分别为 和
和 时,
时,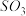 的体积分数随时间的变化如图所示。下列判断错误的是
的体积分数随时间的变化如图所示。下列判断错误的是
A.反应温度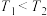 |
B.该反应的 |
C.若 和 和 时的平衡常数分别为 时的平衡常数分别为 和 和 ,则 ,则 |
D.若 和 和 时使用相同的催化剂,其催化效果可能不同 时使用相同的催化剂,其催化效果可能不同 |
您最近一年使用:0次
名校
3 . 向密闭容器中充入一定量 和
和 混合气体,在一定条件下,发生反应:
混合气体,在一定条件下,发生反应:
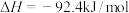 。测得
。测得 在不同温度下的平衡时产率与压强的关系如图所示。下列说法正确的是
在不同温度下的平衡时产率与压强的关系如图所示。下列说法正确的是
 和
和 混合气体,在一定条件下,发生反应:
混合气体,在一定条件下,发生反应:
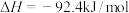 。测得
。测得 在不同温度下的平衡时产率与压强的关系如图所示。下列说法正确的是
在不同温度下的平衡时产率与压强的关系如图所示。下列说法正确的是
A.平衡常数: | B.逆反应速率: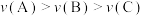 |
C.反应温度: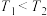 | D.混合气体平均摩尔质量: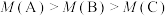 |
您最近一年使用:0次
2024高三下·全国·专题练习
4 . 甲醇是重要的化工原料,又可作燃料。利用CO生产甲醇的反应为2H2(g)+CO(g) CH3OH(g)。已知:v正=k正·x(CO)·x2(H2),v逆=k逆·x(CH3OH),其中v正、v逆为正、逆反应速率,k正、k逆为速率常数,x为各组分的体积分数。在密闭容器中按物质的量之比为2∶1充入H2和CO,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图所示。
CH3OH(g)。已知:v正=k正·x(CO)·x2(H2),v逆=k逆·x(CH3OH),其中v正、v逆为正、逆反应速率,k正、k逆为速率常数,x为各组分的体积分数。在密闭容器中按物质的量之比为2∶1充入H2和CO,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图所示。
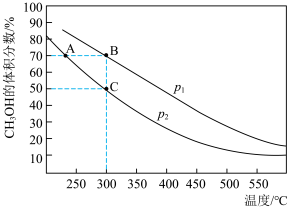
(1)该反应的ΔH______ 0(填“>”或“<”);B点与C点的平衡常数关系为KB______ KC(填“>”“<”或“=”)。向平衡体系中加入高效催化剂, 将
将______ (填“增大”“减小”或“不变”);再次增大体系压强,k正-k逆的值将______ (填“增大”“减小”或“不变”)。
(2)C点对应的平衡常数Kp=______ (Kp为以分压表示的平衡常数,气体分压=气体总压×体积分数)。
(3)一定温度下,将H2和CO按物质的量之比为1∶1、1∶2和2∶1进行初始投料。则达到平衡后,初始投料比为______ 时,H2转化率最大。
 CH3OH(g)。已知:v正=k正·x(CO)·x2(H2),v逆=k逆·x(CH3OH),其中v正、v逆为正、逆反应速率,k正、k逆为速率常数,x为各组分的体积分数。在密闭容器中按物质的量之比为2∶1充入H2和CO,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图所示。
CH3OH(g)。已知:v正=k正·x(CO)·x2(H2),v逆=k逆·x(CH3OH),其中v正、v逆为正、逆反应速率,k正、k逆为速率常数,x为各组分的体积分数。在密闭容器中按物质的量之比为2∶1充入H2和CO,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图所示。
(1)该反应的ΔH
 将
将(2)C点对应的平衡常数Kp=
(3)一定温度下,将H2和CO按物质的量之比为1∶1、1∶2和2∶1进行初始投料。则达到平衡后,初始投料比为
您最近一年使用:0次
名校
5 . K、 、
、 分别表示化学平衡常数、电离常数和水的离子积常数,下列判断正确的是
分别表示化学平衡常数、电离常数和水的离子积常数,下列判断正确的是
 、
、 分别表示化学平衡常数、电离常数和水的离子积常数,下列判断正确的是
分别表示化学平衡常数、电离常数和水的离子积常数,下列判断正确的是A.25℃时,pH均为4的盐酸和 溶液中 溶液中 不相等 不相等 |
| B.在500℃时,在5L密闭容器中进行合成氨的反应,使用催化剂后K增大 |
C.相同温度下 ,说明酸性: ,说明酸性: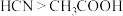 |
D. 达平衡后,改变某一条件时K不变, 达平衡后,改变某一条件时K不变, 的转化率可能增大 的转化率可能增大 |
您最近一年使用:0次
名校
解题方法
6 . 工业上合成尿素的反应为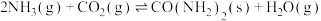
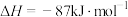 ,氨气的平衡转化率随着条件甲和条件乙的变化曲线如图所示,条件甲和条件乙表示温度或压强。
,氨气的平衡转化率随着条件甲和条件乙的变化曲线如图所示,条件甲和条件乙表示温度或压强。

下列说法正确的是
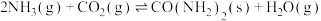
 ,氨气的平衡转化率随着条件甲和条件乙的变化曲线如图所示,条件甲和条件乙表示温度或压强。
,氨气的平衡转化率随着条件甲和条件乙的变化曲线如图所示,条件甲和条件乙表示温度或压强。
下列说法正确的是
| A.条件甲是温度 | B.条件乙1>条件乙2 |
| C.a、b、c三点中,b点反应速率最大 | D.a、c点的平衡常数相等 |
您最近一年使用:0次
名校
解题方法
7 . K、Ka、Kw分别表示化学平衡常数、电离常数和水的离子积常数,下列说法正确的是
| A.某可逆反应达到平衡后,改变某一条件使平衡正向移动,K可能不变 |
| B.氨的催化氧化反应,使用催化剂后K增大 |
| C.室温下Ka(HCN)>Ka(CH3COOH),说明CH3COOH酸性强 |
| D.25℃时,pH均为4的盐酸和NH4I溶液中Kw不相等 |
您最近一年使用:0次
名校
解题方法
8 . 下列关于化学平衡常数K,电离平衡常数 或
或 ,水解平衡常数
,水解平衡常数 ,水的离子积常数
,水的离子积常数 的叙述中正确的是
的叙述中正确的是
 或
或 ,水解平衡常数
,水解平衡常数 ,水的离子积常数
,水的离子积常数 的叙述中正确的是
的叙述中正确的是| A.它们都能反映一定条件下对应变化进行的程度 |
| B.它们的大小都随温度的升高而增大 |
C.常温下, 在水中的 在水中的 大于在饱和 大于在饱和 溶液中的 溶液中的 |
| D.若改变条件使以上平衡正向移动,则达到新的平衡时的相应的平衡常数一定增大 |
您最近一年使用:0次
名校
解题方法
9 . 氢能是最重要的新能源,储氢是氢能利用的关键技术,其中一种储氢的方法为:
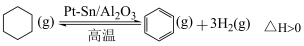
A.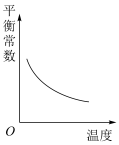 | B.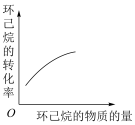 | C.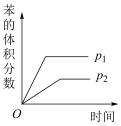 | D.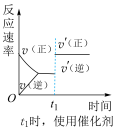 |
您最近一年使用:0次
2023-12-02更新
|
262次组卷
|
6卷引用:2015届安徽省皖北协作区高三3月联考理综化学试卷
名校
10 . 计算。
(1)写出反应 的平衡常数
的平衡常数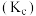 表达式
表达式_________ 。
(2)若某温度时上述反应在 容器内达到平衡,测得容器内有
容器内达到平衡,测得容器内有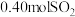 、
、 和
和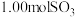 ,计算平衡常数
,计算平衡常数
______ 。
(1)写出反应
 的平衡常数
的平衡常数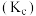 表达式
表达式(2)若某温度时上述反应在
 容器内达到平衡,测得容器内有
容器内达到平衡,测得容器内有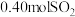 、
、 和
和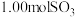 ,计算平衡常数
,计算平衡常数
您最近一年使用:0次
2023-11-13更新
|
108次组卷
|
2卷引用:广东省广州市培英中学2023-2024学年高二上学期10月学情分析化学试题



