CH4、H2、C都是优质的能源物质,它们燃烧的热化学方程式分别为
①CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890.3kJ·mol-1;
②2H2(g)+O2(g)===2H2O(l) ΔH=-571.6kJ·mol-1;
③C(s)+O2(g)===CO2(g) ΔH=-393.5kJ·mol-1。
(1)在深海中存在一种甲烷细菌,它们依靠酶使甲烷与O2作用产生的能量存活。甲烷细菌使1mol甲烷生成CO2气体与液态水,放出的能量_______ (填“>”“<”或“=”)890.3kJ。
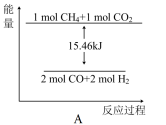
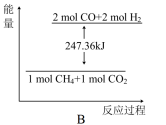
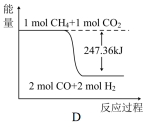
(2)甲烷与CO2可用于合成合成气(主要成分是一氧化碳和氢气):CH4+CO2===2CO+2H2,1gCH4完全反应可释放15.46kJ的热量,能表示该反应过程中能量变化的是________ (填字母)。

(3)C(s)与H2(g)不反应,所以C(s)+2H2(g)===CH4(g)的反应热无法直接测量,但通过上述反应可求出其反应热ΔH=________ 。
①CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890.3kJ·mol-1;
②2H2(g)+O2(g)===2H2O(l) ΔH=-571.6kJ·mol-1;
③C(s)+O2(g)===CO2(g) ΔH=-393.5kJ·mol-1。
(1)在深海中存在一种甲烷细菌,它们依靠酶使甲烷与O2作用产生的能量存活。甲烷细菌使1mol甲烷生成CO2气体与液态水,放出的能量
(2)甲烷与CO2可用于合成合成气(主要成分是一氧化碳和氢气):CH4+CO2===2CO+2H2,1gCH4完全反应可释放15.46kJ的热量,能表示该反应过程中能量变化的是




(3)C(s)与H2(g)不反应,所以C(s)+2H2(g)===CH4(g)的反应热无法直接测量,但通过上述反应可求出其反应热ΔH=
2020高三·全国·专题练习 查看更多[6]
河南省南阳市第六完全学校高级中学2022-2023学年高二上学期9月考试化学试题(已下线)考点17 化学反应的热效应-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)小题27 盖斯定律及应用——备战2021年高考化学经典小题考前必刷(全国通用)(已下线)第19讲 化学能与热能 (精练)-2021年高考化学一轮复习讲练测
更新时间:2020/10/27 17:47:44
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】回答下列问题
(1)氨是重要的化工原料。某工厂用氨制硝酸和铵盐的流程如图所示。

①实验室制备氨气的化学方程式:_______
②设备1中发生反应的化学方程式为:_______
③设备2中通入的物质A是:_______
④ 跟NaClO反应来制得肼(
跟NaClO反应来制得肼( )。该反应的化学方程式为:
)。该反应的化学方程式为:______
(2)利用甲烷催化还原氮氧化物,可以消除氮氧化物的污染。已知:
①

②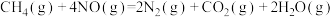

③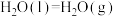

写出 将
将 还原为
还原为 并生成液态水时的热化学方程式:
并生成液态水时的热化学方程式:_______
(3)科研人员设想用如图原电池装置生产硫酸,则负极的电极反应式为_______ 为稳定持续生产,硫酸溶液的浓度应维持不变,则通入 和水的质量比为
和水的质量比为_______

(1)氨是重要的化工原料。某工厂用氨制硝酸和铵盐的流程如图所示。

①实验室制备氨气的化学方程式:
②设备1中发生反应的化学方程式为:
③设备2中通入的物质A是:
④
 跟NaClO反应来制得肼(
跟NaClO反应来制得肼( )。该反应的化学方程式为:
)。该反应的化学方程式为:(2)利用甲烷催化还原氮氧化物,可以消除氮氧化物的污染。已知:
①


②
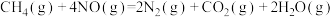

③
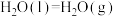

写出
 将
将 还原为
还原为 并生成液态水时的热化学方程式:
并生成液态水时的热化学方程式:(3)科研人员设想用如图原电池装置生产硫酸,则负极的电极反应式为
 和水的质量比为
和水的质量比为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据所学知识,比较下列反应热的大小。
(1)同一反应的生成物状态不同时反应热不同,如2H2(g)+O2(g)=2H2O(g) ΔH1①,2H2(g)+O2(g) =2H2O(l) ΔH2②,则ΔH1____ ΔH2(填“>”、“<”或“=”,下同)。
(2)同一反应的反应物状态不同时,反应热不同,如S(g)+O2(g)=SO2(g) ΔH1① ,S(s)+O2(g) =SO2(g) ΔH2②,则ΔH1_____ ΔH2。
(3)两个相联系的不同反应,其反应热不同。如C(s)+O2(g)=CO2(g) ΔH1①,C(s)+1/2O2(g) =CO(g) ΔH2②,又知CO的燃烧反应为放热反应 ,则ΔH1_______ ΔH2。
(1)同一反应的生成物状态不同时反应热不同,如2H2(g)+O2(g)=2H2O(g) ΔH1①,2H2(g)+O2(g) =2H2O(l) ΔH2②,则ΔH1
(2)同一反应的反应物状态不同时,反应热不同,如S(g)+O2(g)=SO2(g) ΔH1① ,S(s)+O2(g) =SO2(g) ΔH2②,则ΔH1
(3)两个相联系的不同反应,其反应热不同。如C(s)+O2(g)=CO2(g) ΔH1①,C(s)+1/2O2(g) =CO(g) ΔH2②,又知CO的燃烧反应为放热反应 ,则ΔH1
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某温度时,将2 mol CO与5 mol H2的混合气体充入容积为2 L的密闭容器中,在催化剂的作用下发生反应:CO(g)+2H2(g) CH3OH(g)。经过5 min后,反应达到平衡,此时H2的转化率为60%。
CH3OH(g)。经过5 min后,反应达到平衡,此时H2的转化率为60%。
(1)该反应的平衡常数为________ ,v(CH3OH)=________ mol·L-1·min-1。若保持体积不变,再充入2 mol CO和1.5 mol CH3OH,此时v(正)________ v(逆)(填“>”“<”或“=”)。
(2)在一定压强下,容积为VL的容器充入amol CO与2amol H2,在催化剂作用下反应生成甲醇,平衡转化率与温度、压强的关系如图所示。则ΔH___ 0,p1____ p2(填“大于”“小于”或“等于”)。

(3)能使该反应的反应速率增大,且平衡向正反应方向移动的是________ 。
a.及时分离出CH3OH气体 b.适当升高温度 c.增大H2的浓度 d.选择高效催化剂
 CH3OH(g)。经过5 min后,反应达到平衡,此时H2的转化率为60%。
CH3OH(g)。经过5 min后,反应达到平衡,此时H2的转化率为60%。(1)该反应的平衡常数为
(2)在一定压强下,容积为VL的容器充入amol CO与2amol H2,在催化剂作用下反应生成甲醇,平衡转化率与温度、压强的关系如图所示。则ΔH

(3)能使该反应的反应速率增大,且平衡向正反应方向移动的是
a.及时分离出CH3OH气体 b.适当升高温度 c.增大H2的浓度 d.选择高效催化剂
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】碳及其化合物在能源和材料方面具有广泛的用途,回答下列问题:
(1)已知CH4(g)+ O2(g)=CO(g)+2H2O(l)
O2(g)=CO(g)+2H2O(l) 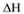 =-607.31kJ/mol
=-607.31kJ/mol
2CO(g)+ O2(g)=2CO2(g)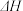 =-566.0kJ/mol
=-566.0kJ/mol
写出表示甲烷燃烧热的热化学方程式____________ 。
(2)天然气的一个重要用途是制取H2,其原理为:CO2(g)+CH4(g) 2CO(g)+2H2(g) 。在密闭容器中通入物质的量浓度均为0.125mol/L的CH4与CO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如下图所示。则:
2CO(g)+2H2(g) 。在密闭容器中通入物质的量浓度均为0.125mol/L的CH4与CO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如下图所示。则:

①压强P1_____ P2(填 “>”或“<”);
②压强为P2时,在Y点:v(正)_______ v(逆)(填“>”、“<”或“=”)。
③求Y点对应温度下的该反应的平衡常数K=_________ 。(计算结果保留两位小数)
(3)CO可以合成二甲醚,2CO(g)+4H2(g) CH3OCH3(g)+H2O(g) △H<0,二甲醚可以作为燃料电池的原料。
CH3OCH3(g)+H2O(g) △H<0,二甲醚可以作为燃料电池的原料。
①写出二甲醚在KOH做电解质条件下的负极电极反应式_____________________ 。
②利用此燃料电池以石墨为电极电解1L,0.5mol/L的CuSO4溶液,导线通过1mol电子时,假设溶液体积不变,则所得溶液pH=_________ ,理论上消耗二甲醚________ g(保留小数点后两位)。
(1)已知CH4(g)+
 O2(g)=CO(g)+2H2O(l)
O2(g)=CO(g)+2H2O(l) 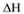 =-607.31kJ/mol
=-607.31kJ/mol2CO(g)+ O2(g)=2CO2(g)
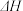 =-566.0kJ/mol
=-566.0kJ/mol写出表示甲烷燃烧热的热化学方程式
(2)天然气的一个重要用途是制取H2,其原理为:CO2(g)+CH4(g)
 2CO(g)+2H2(g) 。在密闭容器中通入物质的量浓度均为0.125mol/L的CH4与CO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如下图所示。则:
2CO(g)+2H2(g) 。在密闭容器中通入物质的量浓度均为0.125mol/L的CH4与CO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如下图所示。则:
①压强P1
②压强为P2时,在Y点:v(正)
③求Y点对应温度下的该反应的平衡常数K=
(3)CO可以合成二甲醚,2CO(g)+4H2(g)
 CH3OCH3(g)+H2O(g) △H<0,二甲醚可以作为燃料电池的原料。
CH3OCH3(g)+H2O(g) △H<0,二甲醚可以作为燃料电池的原料。①写出二甲醚在KOH做电解质条件下的负极电极反应式
②利用此燃料电池以石墨为电极电解1L,0.5mol/L的CuSO4溶液,导线通过1mol电子时,假设溶液体积不变,则所得溶液pH=
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】Cu2O是一种重要的工业原料,广泛川作催化剂。
Ⅰ.制备Cu2O
(1)微乳液—还原法:在100℃的Cu(NO3)2溶液中加入一定体积的NaOH溶液,搅拌均匀,再逐滴加入肼(N2H4)产生红色沉淀,抽滤、洗涤、干燥,得到Cu2O。
已知:N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-akJ·mol-1
Cu(OH)2(s)=CuO(s)+H2O(l)△H=+bkJ·mol-1
4CuO(s)=2Cu2O(s)+O2(g)△H=+ckJ·mol-1
则由N2H4(l)和Cu(OH)2(s)反应制备Cu2O(s)的热化学方程式为__ 。
(2)电解法:纳米级Cu2O由于具有优良的催化性能而受到关注。
采用阴离子交换膜制备纳米级Cu2O的装置如图所示:

阳极的电极反应式为___ 。
Ⅱ.纳米级Cu2O催化剂可用于工业上合成甲醇:CO(g)+2H2(g) CH3OH(g)△H=-90.8kJ·mol-1
CH3OH(g)△H=-90.8kJ·mol-1
(3)能说明反应CO(g)+2H2(g) CH3OH(g)已达平衡状态的是
CH3OH(g)已达平衡状态的是__ (填字母)。
A.CO的消耗速率等于CH3OH的生成速率
B.一定条件,CO的转化率不再变化
C.在绝热恒容的容器中,反应的平衡常数不再变化
(4)t℃时,在体积为2L固定体积的密闭容器中加入2.00molH2(g)和1.00mol的CO(g)的物质的量随时间的变化如表:
根据表中数据回答:
①氢气平衡转化率为___ 。
②2t℃时该反应的平衡常数为___ 。
③保持其它条件不变,向平衡体系中充入1molCO(g)、2molH2(g)、1molCH3OH(g);此时v正__ v逆(填“>”“<”或“=”)。
(5)工业实际合成CH3OH生产中,采用如图M点而不是N点对应的反应条件,运用化学反应速率和化学平衡知识,同时考虑生产实际,说明选择该反应条件的理由:__ 。

Ⅰ.制备Cu2O
(1)微乳液—还原法:在100℃的Cu(NO3)2溶液中加入一定体积的NaOH溶液,搅拌均匀,再逐滴加入肼(N2H4)产生红色沉淀,抽滤、洗涤、干燥,得到Cu2O。
已知:N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-akJ·mol-1
Cu(OH)2(s)=CuO(s)+H2O(l)△H=+bkJ·mol-1
4CuO(s)=2Cu2O(s)+O2(g)△H=+ckJ·mol-1
则由N2H4(l)和Cu(OH)2(s)反应制备Cu2O(s)的热化学方程式为
(2)电解法:纳米级Cu2O由于具有优良的催化性能而受到关注。
采用阴离子交换膜制备纳米级Cu2O的装置如图所示:

阳极的电极反应式为
Ⅱ.纳米级Cu2O催化剂可用于工业上合成甲醇:CO(g)+2H2(g)
 CH3OH(g)△H=-90.8kJ·mol-1
CH3OH(g)△H=-90.8kJ·mol-1(3)能说明反应CO(g)+2H2(g)
 CH3OH(g)已达平衡状态的是
CH3OH(g)已达平衡状态的是A.CO的消耗速率等于CH3OH的生成速率
B.一定条件,CO的转化率不再变化
C.在绝热恒容的容器中,反应的平衡常数不再变化
(4)t℃时,在体积为2L固定体积的密闭容器中加入2.00molH2(g)和1.00mol的CO(g)的物质的量随时间的变化如表:
| 时间(s) | 0 | 2 | 5 | 10 | 20 | 40 | 80 |
| 物质的量(mol) | 1.00 | 0.50 | 0.375 | 0.25 | 0.20 | 0.20 | 0.20 |
①氢气平衡转化率为
②2t℃时该反应的平衡常数为
③保持其它条件不变,向平衡体系中充入1molCO(g)、2molH2(g)、1molCH3OH(g);此时v正
(5)工业实际合成CH3OH生产中,采用如图M点而不是N点对应的反应条件,运用化学反应速率和化学平衡知识,同时考虑生产实际,说明选择该反应条件的理由:

您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】按要求完成下列问题。
(1)某反应过程中的能量变化如图所示:

①该反应的ΔH_______ (填“>”或“<”)0。
②加入催化剂,b_______ (填“增大”“减小”或“不变”,下同),ΔH_______ 。
③该反应的热化学方程式为_______ 。
(2)已知:①2Zn(s)+O2(g)=2ZnO(s) ΔH=-702.2 kJ·mol-1②2Hg(l)+O2(g)=2HgO(s) ΔH=-181.4 kJ·mol-1,则Zn(s)+HgO(s)=ZnO(s)+Hg(l) ΔH=_______ kJ·mol-1。
(3)已知:
①H2O(g)=H2(g)+1/2O2(g) ΔH=+241.8kJ/mol
②C(s)+1/2O2(g)=CO(g) ΔH=-110.5kJ/mol
③C(s)+O2(g)=CO2(g) ΔH=-393.5kJ/mol
则表示CO的燃烧热的热化学方程式为_______ ;10g H2完全燃烧生成水蒸气,放出的热量为_______ kJ。
(1)某反应过程中的能量变化如图所示:

①该反应的ΔH
②加入催化剂,b
③该反应的热化学方程式为
(2)已知:①2Zn(s)+O2(g)=2ZnO(s) ΔH=-702.2 kJ·mol-1②2Hg(l)+O2(g)=2HgO(s) ΔH=-181.4 kJ·mol-1,则Zn(s)+HgO(s)=ZnO(s)+Hg(l) ΔH=
(3)已知:
①H2O(g)=H2(g)+1/2O2(g) ΔH=+241.8kJ/mol
②C(s)+1/2O2(g)=CO(g) ΔH=-110.5kJ/mol
③C(s)+O2(g)=CO2(g) ΔH=-393.5kJ/mol
则表示CO的燃烧热的热化学方程式为
您最近半年使用:0次



