28. 大气污染越来越成为人们关注的问题,烟气中的NO
x必须脱除(即脱硝)之后才能排放。
(1)CO和H
2可作为能源和化工原料,应用十分广泛。 反应CO(g)+H
2O(g)

H
2(g)+CO
2(g)的平衡常数随温度的变化如表所示。
| 温度/℃ | 400 | 500 | 830 | 1 000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
①从上表可以推断:此反应是
__________(填“吸”或“放”)热反应。
②在830 ℃下,若开始时向恒容密闭容器中充入CO与H
2O均为1 mol,则达到平衡后CO的转化率为
________。
(2)在汽车尾气系统中装置催化转化器,可有效降低NO
x和CO的排放。
已知:①2CO(g)+O
2(g)

2CO
2(g) ΔH=−566.0 kJ·mol
−1②N
2(g)+O
2(g) ⇌2NO(g)
ΔH=+180.0 kJ·mol
−1③2NO(g)+O
2(g) ⇌2NO
2(g) ΔH=−116.5 kJ·mol
−1回答下列问题:
①CO的燃烧热为
_________。若1 mol N
2(g)、1 mol O
2(g) 分子中化学键断裂时分别需要吸收946 kJ、498 kJ的能量,则1 mol NO(g) 分子中化学键断裂时需吸收的能量为
_________kJ。
②写出CO将NO
2还原为单质反应的热化学方程式为
____________________(3)汽车排气管上的催化转化器,发生上述的CO将NO
2还原为单质反应。在一定温度下,将一定量的CO和NO
2充入2L固定容积的容器中,回答以下问题:
①能说明该反应达到平衡状态的是
_____________(填字母标号)。
A.2υ
正(NO
2)=υ
逆(N
2)
B. 混合气体的平均相对分子质量保持不变
C.气体总压强不再变化
D. ΔH保持不变
E.混合气体的密度不再变化
②从反应开始到5min,生成了0.08mol N
2,则5min内υ(CO)=
___mol
⋅L
−1⋅min
−1。
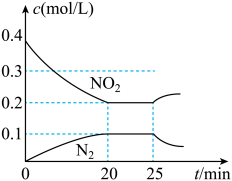
③25min时,物质浓度变化如图所示,则改变的条件可能是
___________(填字母标号)。
A.缩小容器体积
B.增加NO
2的浓度
C.降低温度
D.升高温度