27. 工业上利用电解饱和食盐水可制得重要化工产品,又称为“氯碱工业”。并能以它们为原料生产一系列化工产品。为提高原料的利用率,节能降耗。设计如图所示工艺流程,其中氯碱工业装置中的电极未标出。

(1)电解饱和食盐水的化学方程式为
___________________。
(2)为除去粗盐中的Ca
2+、Mg
2+、SO
42-及泥沙,得到纯净的NaCl,可将粗盐溶于水,正确的操作步骤的顺序是
_______(填序号)。
①过滤②加过量NaOH溶液③加适量盐酸④加过量Na
2CO
3溶液⑤加过量BaCl
2溶液
A.①④①②⑤③B.①②⑤④①③ C.①②④⑤③D.④②⑤
(3)图中NaOH溶液的质量分数a%、b%、c%,由大到小的顺序为
_________。
(4)氯碱工业的产物NaOH与不同物质反应可以生成不同的盐。已知常温下,浓度均为0.1 mol/L的四种钠盐溶液pH如下表,下列说法不正确的是
_______(填序号)。
| 溶质 | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
| pH | 11.6 | 9.7 | 10.3 | 5.2 |
A.向氯水中加入NaHCO
3,可以增大氯水中次氯酸的浓度
B.四种溶液中,水的电离程度最大的是NaClO
C.常温下,相同物质的量浓度的H
2SO
3、H
2CO
3、HClO,pH最大的是HClO
D.四种盐的阴离子结合H
+能力最强的是HCO
3-(5)若利用电解氯化钠溶液所得的气体制36.5%的浓盐酸100t,最少需要消耗食盐
_________t。
(6)氯碱工业产品Cl
2可用于冶炼钛铁矿得到金属钛,流程如图。写出钛铁矿经氯化法得到四氯化钛的化学方程式:
____________________。
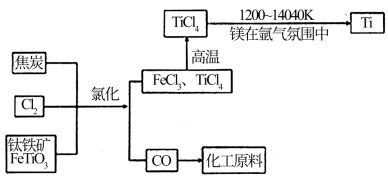
(7)氮气和氩气是两种化学性质相对稳定的气体。镁还原TiCl
4的反应中为防止Mg和Ti被氧化选择稀有气体氩气。试用化学反应方程式解释不选用氮气的原因:
__________________。