22. Ⅰ.碳、氮及其化合物在工农业生产生活中有着重要作用。请回答下列问题:
(1)用CH
4 催化还原NO
x 可以消除氮氧化物的污染。例如:
CH
4(g) + 4NO
2(g) = 4NO(g)+CO
2(g) + 2H
2O(g) ΔH
1=-574 kJ·molˉ
1CH
4(g) + 4NO(g) = 2N
2(g)+CO
2(g) + 2H
2O(g) ΔH
2若2 mol CH
4 还原NO
2 至N
2,整个过程中放出的热量为1734 kJ,则ΔH
2=
______(2)据报道,科学家在一定条件下利用Fe
2O
3与甲烷反应可制取“纳米级”的金属铁。其反应为:Fe
2O
3(s) + 3CH
4(g)

2Fe(s)+3CO(g) + 6H
2(g) ΔH>0
①若反应在5L的密闭容器中进行,1min后达到平衡,测得Fe
2O
3在反应中质量减少3.2g。则该段时间内CO的平均反应速率为
_____②若该反应在恒温恒容容器中进行,能表明该反应达到平衡状态的是
_____A.CH
4的转化率等于CO的产率
B.混合气体的密度不变
C.v(CO)与v(H
2)的比值为1:2
D.固体的总质量不变
③该反应达到平衡时某物理量随温度变化如图所示,当温度由T
1升高到T
2时,平衡常数K
A_____K
B(填“>”、“<”或“=”)。纵坐标可以表示的物理量有哪些
_____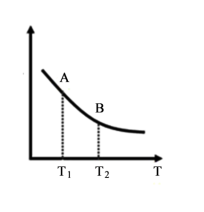
A.H
2的逆反应速率
B.CH
4的的体积分数
C.混合气体的平均相对分子质量
D.CO的体积分数
Ⅱ.已知2A
2(g)+B
2(g)

2C
3(g)
△H=-Q
1 kJ/mol (Q
1>0),在一个有催化剂的容积不变的密闭容器中加入2 mol A
2和1 mol B
2,在500℃时充分反应,达平衡后C
3的浓度为w mol·L
-1,放出热量为Q
2 kJ。
(1)下列措施可以同时提高反应速率和B
2的转化率是
___________(填选项序号)。
A.选择适当的催化剂
B.增大压强
C.及时分离生成的C
3D.升高温度
(2)达到平衡后,向原容器中通入少量的Ar,A
2的转化率将
___________(填“增大“、“减小”或“不变”)
(3)达到平衡时,A
2的转化率为
___________(4)将上述容器改为恒压容器,起始时加入2 mol A
2和1 mol B
2,500℃时充分反应达平衡后,放出热量Q
4 kJ,则Q
2___________Q
4(填“>”、“<”或“=”)。
(5)改变某一条件,得到如图的变化规律(图中T表示温度,n表示物质的量),可得出的结论正确的是
___________;
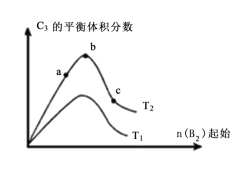
A.反应速率c>b>a
B.达到平衡时A
2的转化率大小为:b>a>c
C.T
2>T
1D.b点A
2和B
2的物质的量之比为2:1