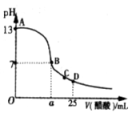
26. I、在25mL的氢氧化钠溶液中逐滴加入0.2 mol/ L醋酸溶液,滴定曲线如图所示。
(1)写出氢氧化钠溶液与醋酸溶液反应的离子方程式:
_____________________。
(2)该氢氧化钠溶液浓度为
________________。
(3)在B点,a
_________12.5 mL(填“<”“>”或“=”)。若由体积相等的氢氧化钠溶液和醋酸溶液混合且恰好呈中性,则混合前c(NaOH)
____________c(CH
3COOH),混合前酸中c(H
+)和碱中的c(OH
-)的关系:c(H
+)
____________c(OH
-)(填“<”“>”或“=”)。
(4)在D点,溶液中离子浓度大小关系为
_______________________________。
II、相同物质的量浓度的NaX、NaY、NaZ三种盐溶液的pH分别为7、8、9,则相同物质的量浓度的HX、HY、HZ的酸性强弱顺序为:
__________________________。III、下列电解质中,①NaCl;②NaOH;③NH
3·H
2O;④CH
3COOH;⑤BaSO
4;⑥AgCl;⑦ H
2O,
________________是强电解质;
______________是弱电解质。
IV、有浓度为0.1 mol•L
-1的盐酸、醋酸二种溶液,试回答:
(1)二种溶液中c(H
+) 依次为a mol•L
-1,b mol•L
-1,其大小顺序为
__________。
(2)等体积的以上二种酸分别与过量的NaOH 溶液反应,生成的盐的物质的量依次为n
1mol,n
2 mol,它们的大小关系为
____________。
(3)与锌反应时产生氢(气)的速率刚开始一段时间分别为v
1、v
2,其大小关系为
_______。
V、25℃时,有0.01 mol•L
-1的醋酸溶液,则醋酸的电离平衡常数表达式为
____________,达平衡时,溶液中氢离子浓度是
____________。(提示:25℃时,醋酸的电离平衡常数为1. 85×10
-5,醋酸的电离常数很小,平衡时C(CH
3COOH)=0.01 mol•L
-1,4.3
2=18.5)