25. 化工行业的发展必须符合国家节能减排的总体要求。请回答下列问题:
(1)已知C(s)+H
2O(g)

CO(g)+H
2(g),则该反应的平衡常数表达式为
_______。
(2)已知在一定温度下,
C(s)+CO
2(g)

2CO(g)
△H
1CO(g)+H
2O(g)

H
2(g)+CO
2(g)
△H
2C(s)+H
2O(g)

CO(g)+H
2(g)
△H
3则
△H
1、
△H
2、
△H
3之间的关系是:
_____________。
(3)通过研究不同温度下平衡常数可以解决某些实际问题。已知等体积的一氧化碳和水蒸气进入反应时,会发生如下反应: CO(g)+H
2O(g)

H
2(g)+CO
2(g),该反应平衡常数随温度的变化如表所示。
则该反应的正反应方向是
_______反应(填“吸热”或“放热”),在500℃时,若设起始时CO和H
2O的起始浓度均为0.020mol/L,则CO的平衡转化率为
_________。
(4)从氨催化氧化可以制硝酸,此过程中涉及氮氧化物,如NO、NO
2、N
2O
4等。对反应N
2O
4(g)

2NO
2(g)
△H>0在温度为T
1、T
2时,平衡体系中NO
2的体积分数随压强变化曲线如图所示。下列说法正确的是
_________:
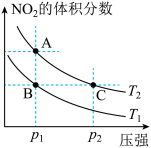
A. A、C两点的反应速率:A>C
B. A、C两点气体的颜色:A深,C浅
C. A、C两点的气体的平均相对分子质量:A<C
D.由状态A到状态B,可以用加热的方法
E.A、C两点的化学平衡常数:A=C
(5)某小组利用H
2C
2O
4溶液和硫酸酸化的KMnO
4溶液反应来探究“外界条件对化学反应速率的影响”。实验时通过测定酸性KMnO
4溶液褪色所需时间来判断反应的快慢。该小组设计了如下方案。已知:
实验
编号 | 0.1mol/L酸性KMnO4溶液的体积/mL | 0.6mol/LH2C2O4溶液的体积/mL | H2O的体积/mL | 实验温度/℃ | 溶液褪色所需时间/min |
| ① | 10 | V1 | 35 | 25 | |
| ② | 10 | 10 | 30 | 25 | |
| ③ | 10 | 10 | V2 | 50 | |
①表中V
1=
______mL
②探究温度对化学反应速率影响的实验编号是
_____(填编号)
③KMnO
4溶液与H
2C
2O
4溶液反应的离子方程式
_________④实验③测得KMnO
4溶液的褪色时间为2min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(H
2C
2O
4)=
___mol·L
-1·min
-1。