21. 以天然气(CH
4)为原料合成甲醇(CH
3OH)。有关热化学方程式如下:
①2CH
4(g)+O
2(g) = 2CO(g)+4H
2(g) ΔH
1=-70.8 kJ·mol
-1②CO(g)+2H
2(g)
⇌CH
3OH(g) ΔH
2③2CH
4(g)+O
2(g)
⇌2CH
3OH(g) ΔH
3=-251.0 kJ·mol
-1(1)ΔH
2=
________kJ·mol
-1。 反应①自发进行的条件是
_________(填序号)。
a.高温
b. 低温
c. 任何环境都自发
d. 任何环境都不自发
(2)在体积可变的密闭容器中投入1 mol CO和2 mol H
2,在不同条件下发生反应:CO(g)+2H
2(g)
⇌CH
3OH(g)。实验测得平衡时CH
3OH的物质的量随温度、压强的变化如图所示。
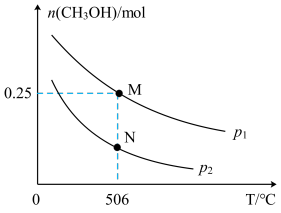
①M点时,H
2的转化率为
__________;压强:p
1_______p
2 (填“>”、“<”或“=”)。
②反应速率:N点ʋ
正(CO)
________M点ʋ
逆(CO)(填“>”、“<”或“=”)。
③温度为506℃时,若压强为p
1、在密闭容器中进行上述反应(起始投料不变),平衡时容器体积为1L,则平衡常数K=
__________(用分数表示)。在不同温度下上述反应的平衡常数的对数(lg K)如图所示,则B、C、D、E四点中能正确表示该反应的lg K与T的关系的点为
_______(填字母)。

④在2 L恒容密闭容器中充入a(a>0) mol H
2、2 mol CO和6 mol CH
3OH(g),在506℃下进行上述反应。为了使该反应逆向进行,a的范围为
____________。