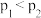工业上可通过甲醇羰基化法制取甲酸甲酯:CH3OH(g)+ CO(g) HCOOCH3(g),在容积固定的密闭容器中,投入等物质的量CH3OH和CO,测得相同时间内CO的转化率随温度变化如图所示。下列说法
HCOOCH3(g),在容积固定的密闭容器中,投入等物质的量CH3OH和CO,测得相同时间内CO的转化率随温度变化如图所示。下列说法不正确 的是
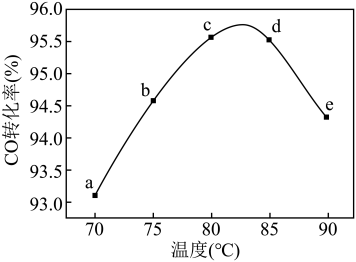
 HCOOCH3(g),在容积固定的密闭容器中,投入等物质的量CH3OH和CO,测得相同时间内CO的转化率随温度变化如图所示。下列说法
HCOOCH3(g),在容积固定的密闭容器中,投入等物质的量CH3OH和CO,测得相同时间内CO的转化率随温度变化如图所示。下列说法
| A.增大压强甲醇转化率减小 |
| B.b点反应速率υ正=υ逆 |
| C.平衡常数K(75℃)>K(85℃),反应速率υb<υd |
| D.生产时反应温度控制在80~85℃为宜 |
更新时间:2020-12-04 08:46:18
|
相似题推荐
多选题
|
适中
(0.65)
名校
【推荐1】在恒容绝热的容器中投入1molA和1molB进行反应:2A(g)+B(g) 3C(g)+D(s) △H=-akJ·mol-1(a>0),下列说法不正确的是
3C(g)+D(s) △H=-akJ·mol-1(a>0),下列说法不正确的是
 3C(g)+D(s) △H=-akJ·mol-1(a>0),下列说法不正确的是
3C(g)+D(s) △H=-akJ·mol-1(a>0),下列说法不正确的是| A.容器中压强不变,表明反应达到平衡状态 |
| B.B的体积分数不变,不能表明反应达到平衡状态 |
| C.增加A的浓度,平衡时B的体积分数减少 |
| D.反应达到平衡状态后增加D的量,容器内的温度会降低 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】在一密闭容器中,反应aA(g) bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,A的浓度变为原来的60%,则
bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,A的浓度变为原来的60%,则
 bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,A的浓度变为原来的60%,则
bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,A的浓度变为原来的60%,则| A.平衡向逆反应方向移动了 | B.物质A的转化率减小了 |
| C.物质B的质量分数增加了 | D.a<b |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐3】在同一温度下,在3个容积均为1.0 L的恒容密闭容器中发生反应:PCl5(g) PCl3(g)+Cl2(g)。下列说法错误的是
PCl3(g)+Cl2(g)。下列说法错误的是
 PCl3(g)+Cl2(g)。下列说法错误的是
PCl3(g)+Cl2(g)。下列说法错误的是| 容器编号 | 物质的起始浓度/(mol/L) | 物质的平衡浓度/(mol/L) | ||
| c(PCl5) | c(PCl3) | c(Cl2) | c(Cl2) | |
| I | 0.4 | 0 | 0 | 0.2 |
| II | 0.6 | 0 | 0.2 | |
| III | 0.8 | 0 | 0 | |
A.反应达到平衡时,容器I中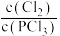 比容器II中的大 比容器II中的大 |
| B.反应达到平衡时,容器I与容器II中的总压强之比为3∶4 |
C.反应达到平衡时,容器III中Cl2的体积分数小于 |
| D.反应达到平衡时,容器III中0.4 mol/L<c(PCl5)<0.8 mol/L |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】臭氧是理想的烟气脱硝试剂,其脱硝反应为2NO2(g)+O3(g) N2O5(g)+O2(g),若反应在恒容密闭容器中进行,反应过程中测得O2(g)的浓度随时间t的变化曲线如图所示。
N2O5(g)+O2(g),若反应在恒容密闭容器中进行,反应过程中测得O2(g)的浓度随时间t的变化曲线如图所示。

下列叙述正确的是
 N2O5(g)+O2(g),若反应在恒容密闭容器中进行,反应过程中测得O2(g)的浓度随时间t的变化曲线如图所示。
N2O5(g)+O2(g),若反应在恒容密闭容器中进行,反应过程中测得O2(g)的浓度随时间t的变化曲线如图所示。
下列叙述正确的是
| A.b点的反应速率比c点快 |
| B.若向容器内充入一定体积的O2,化学反应速率减小 |
| C.0至8minNO2的平均反应速率是0.4mol·L·min-1 |
| D.若向容器内充入一定体积的NO,化学反应速率不变 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】在一体积固定的密闭容器中发生: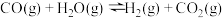 ,如图表示该反应在时刻达到平衡,在
,如图表示该反应在时刻达到平衡,在 时刻分别因改变某个条件而发生变化的情况。图中
时刻分别因改变某个条件而发生变化的情况。图中 时刻发生改变的条件可能是
时刻发生改变的条件可能是
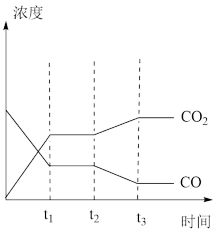
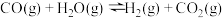 ,如图表示该反应在时刻达到平衡,在
,如图表示该反应在时刻达到平衡,在 时刻分别因改变某个条件而发生变化的情况。图中
时刻分别因改变某个条件而发生变化的情况。图中 时刻发生改变的条件可能是
时刻发生改变的条件可能是
A.加入 | B.加入水蒸气 | C.加入催化剂 | D.分离部分 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】下列有关实验操作、现象和解释或结论都正确的是
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 将NO2球浸泡在冰水、热水中 | 热水中红棕色明显加深 | 2NO2(g)⇌ N2O4(g)ΔH<0,平衡逆向移动 |
| B | 向盛有1mL2mol/L的NaOH溶液中先滴加1~2滴0.1mol/LMgCl2溶液后,继续滴加2滴0.1mol/LFeC13溶液 | 先有白色沉淀,后转化为红褐色沉淀 | Fe(OH)3比Mg(OH)2更难溶 |
| C | 向饱和硼酸溶液中滴加碳酸钠溶液(已知:H3BO3K=5.8×10-10,H2CO3K1=4.4×10-7K2=4.7×10-11) | 无明显现象 | 硼酸不与碳酸钠反应 |
| D | 向盛有饱和硫代硫酸钠溶液的试管中滴加稀盐酸 | 有刺激性气味气体产生,溶液变浑浊 |  +2H+=SO2↑+S↓+H2O +2H+=SO2↑+S↓+H2O |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐2】在恒温条件下,向盛有食盐的2L恒容密闭容器中加入 和
和 ,发生两个反应:
,发生两个反应:
①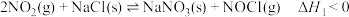 平衡常数
平衡常数
②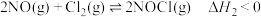 平衡常数
平衡常数
10min时反应达到平衡测得容器内体系的压强减少20%,10min内用NOCl(g)表示的平均反应速率 。下列说法不正确的是
。下列说法不正确的是
 和
和 ,发生两个反应:
,发生两个反应:①
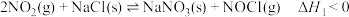 平衡常数
平衡常数
②
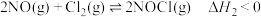 平衡常数
平衡常数
10min时反应达到平衡测得容器内体系的压强减少20%,10min内用NOCl(g)表示的平均反应速率
 。下列说法不正确的是
。下列说法不正确的是A.反应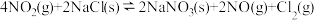 的平衡常数为 的平衡常数为 |
B.平衡后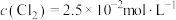 |
C.其他条件保持不变,反应在恒压条件下进行,则平衡常数 增大 增大 |
D.平衡时 的转化率为60% 的转化率为60% |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐3】为了模拟汽车尾气的净化,向密闭容器中投入一定量的CO和O2,在催化剂(I型、II型)和不同温度下发生反应:2CO(g)+O2(g) 2CO2(g),反应进行相同时间t(s),测得CO转化率与温度的关系曲线如图所示。下列说法正确的是
2CO2(g),反应进行相同时间t(s),测得CO转化率与温度的关系曲线如图所示。下列说法正确的是
 2CO2(g),反应进行相同时间t(s),测得CO转化率与温度的关系曲线如图所示。下列说法正确的是
2CO2(g),反应进行相同时间t(s),测得CO转化率与温度的关系曲线如图所示。下列说法正确的是
| A.该反应在a、b两点对应的平衡常数大小关系:Ka>Kb |
| B.b点转化率明显下降最主要原因是温度升高催化剂失活 |
| C.在实验中CO平衡转化率达到阴影部分数值只能采用延长反应时间的方案 |
D.50℃、t s时容器中O2浓度为0.01 mol/L,该温度下反反应平衡常数为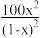 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】化学反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。相关数据如下表:
在反应进料气组成、压强及反应时间相同的情况下,某催化剂表面的积碳量随温度的变化关系如图所示。升高温度时,下列关于积碳反应、消碳反应的平衡常数(K)和速率(v)的叙述正确的是

反应 | 积碳反应 CH4(g)=C(s)+2H2(g) | 消碳反应 CO2(g)+C(s)=2CO(g) | |
△H/kJ∙mol-1 | 75 | 172 | |
活化能/(kJ·mol-1) | 催化剂X | 33 | 91 |
催化剂Y | 43 | 72 | |

| A.K积、K消均增加 | B.v积减小、v消增加 |
| C.催化剂X效果比Y好 | D.v消增加的倍数比v积增加的倍数大 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
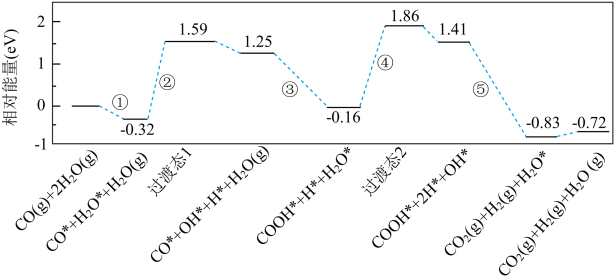
【推荐2】合成氨反应 N2(g)+
N2(g)+ H2(g)⇌NH3(g)是目前最有效工业固氮的方法,解决数亿人口生存问题。科学家研究利用铁触媒催化合成氨的反应历程如图所示,其中吸附在催化剂表面的物种用“ad”表示。
H2(g)⇌NH3(g)是目前最有效工业固氮的方法,解决数亿人口生存问题。科学家研究利用铁触媒催化合成氨的反应历程如图所示,其中吸附在催化剂表面的物种用“ad”表示。
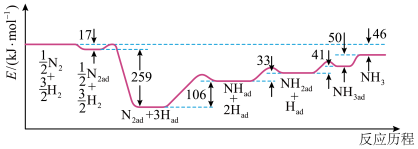
下列说法错误的是
 N2(g)+
N2(g)+ H2(g)⇌NH3(g)是目前最有效工业固氮的方法,解决数亿人口生存问题。科学家研究利用铁触媒催化合成氨的反应历程如图所示,其中吸附在催化剂表面的物种用“ad”表示。
H2(g)⇌NH3(g)是目前最有效工业固氮的方法,解决数亿人口生存问题。科学家研究利用铁触媒催化合成氨的反应历程如图所示,其中吸附在催化剂表面的物种用“ad”表示。
下列说法错误的是
| A.该合成氨反应的△H=+46 kJ/mol |
| B.活化能最大的一步反应的方程式为Nad+Had=NHad |
| C.升高温度、增大压强均能提高原料的平衡转化率 |
| D.加入催化剂能降低反应活化能,加快正反应速率 |
您最近一年使用:0次


 的
的 ,
,