20. 已知:氮气和氢气合成氨反应为:N
2(g)+3H
2(g)

2NH
3(g) ΔH=-92kJ·mol
-1请回答下列问题:
(1)取1 mol N
2(g)和3 molH
2(g)充入一密闭容器中,一定条件下进行反应并达平衡时,测得反应放出的热量
_________92kJ(填“大于”、“等于”或“小于”), 原因是
_____________;若升高温度,上述反应中ΔH
___________ (填“变大”、“变小”或“不变”)。
(2)已知:分别破坏1molN

H键、1mol H

H键需要吸收的能量为:391 kJ、436 kJ,则破坏1mol N

N键需要吸收的能量为
_______________。
(3)一定条件下,向体积为2L的恒容密闭容器中充入1molNH
3(g) 并发生上述反应。半分钟后反应达到平衡,测得v(NH
3)=0.40mol/(L•min),则上述合成氨反应的平衡常数为
____________。
(4)向三个体积均为1L的恒容密闭容器中分别充入1molN
2和3molH
2,当分别只改变其中一个外界条件时使反应达到平衡,测得氨的体积分数随时间的变化如图所示。
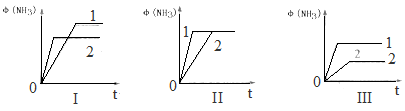
上述图象中,只改变温度的为
__________(填“I”“II”“III”,下同),只改变压强的为
_______,只改变催化剂的为
_________________。
(5)若把标准状况下8.96L氨气通入到100g9.8%的硫酸溶液中并完全吸收,所得溶液中离子浓度从大到小的顺序是
________________________。
(6)常温下,向浓度均为0.1mol/L的MgCl
2、FeCl
3和AlCl
3混合溶液中通入NH
3至过量,最先生成沉淀的化学式为
____________,当pH=
_______时,开始生成Mg(OH)
2沉淀。
(已知:Ksp[Mg(OH)
2] =1.0×10
-13; Ksp[Fe(OH)
3] =1.0×10
-40;Ksp[Al(OH)
3] =1.0×10
-33)