21. 化学反应的能量变化通常表现为热量的变化,因此反应热的研究对于化学学科发展具有重要意义。
Ⅰ.已知反应:①101 kPa时,2C(s)+O
2(g)=2CO(g) ΔH=-221kJ·mol
-1②稀溶液中,H
+(aq)+OH
-(aq)=H
2O(l) ΔH=-57.3kJ·mol
-1下列结论中正确的是
_________。
A.碳的燃烧热等于110.5kJ·mol
-1B.①的反应热为221kJ·mol
-1C.稀硫酸与稀NaOH溶液反应的中和热为114.6kJ·mol
-1D.含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.65kJ的热量
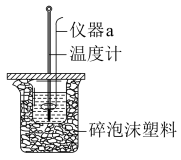
Ⅱ.利用如图所示装置测定中和热的实验步骤如下:
①用量筒量取100mL 0.50mol·L
-1盐酸倒入小烧杯中,测出盐酸温度;
②用另一量筒量取100mL 0.55mol·L
-1 NaOH溶液,并用同一温度计测出其温度;
③将NaOH和盐酸溶液一并倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。
回答下列问题:
(1)仪器a的名称是
_______。烧杯间填满碎泡沫塑料的作用是
________。
(2)配制100mL 0.55mol/L的氢氧化钠溶液,需要用到的仪器有托盘天平、烧杯、钥匙、镊子、玻璃棒、量筒以及
______。
(3)实验中改用80mL0.50mol/L盐酸跟80mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量
_____(填“相等”“不相等”)。反应过程中NaOH溶液的浓度为0.55mol·L
-1不是0.50mol·L
-1 的原因是
_________。用Ba(OH)
2溶液和硫酸代替上述试剂,所测中和热的数值
_________。(填“偏大”、“偏小”或“不变”)
(4)倒入NaOH和盐酸溶液的正确操作是
______(填字母)。
A.沿玻璃棒缓慢倒入
B.分三次倒入
C.一次迅速倒入
D.一边搅拌一边一次滴入
(5)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和1L 1mol·L
-1的稀盐酸恰好完全反应,其反应热分别为ΔH
1、ΔH
2、ΔH
3,则ΔH
1、ΔH
2、ΔH
3的大小关系为
_________。
(6)假设盐酸和氢氧化钠溶液的密度都是1g·cm
-3,又知中和反应后生成溶液的比热容c=4.18J·g
-1·℃
-1。为了计算中和热,某学生实验记录数据如下:
| 实验序号 | 起始温度t1/℃ | 终止温度t2/℃ |
| 盐酸 | 氢氧化钠溶液 | 混合溶液 |
| 1 | 20.0 | 20.2 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.3 | 20.5 | 25.6 |
依据该学生的实验数据计算,该实验测得的中和热ΔH=
__________(结果保留一位小数)。