26. 某同学用0.1000mol/L的标准盐酸来测定某氢氧化钠样品的纯度(杂质不参与反应),试根据实验回答下列问题:
| 滴定次数 | 待测溶液
体积(mL) | 标准酸体积 |
| 滴定前的刻度(mL) | 滴定后的刻度(mL) |
| 第一次 | 10.00 | 0.40 | 10.50 |
| 第二次 | 10.00 | 4.10 | 14.00 |
| 第三次 | 10.00 | 2.50 | 14.00 |
(1)准确称量5.0 g含有少量易溶杂质的样品,配成1L待测溶液。称量时,样品可放在
_______(填字母)称量。
A.小烧杯中
B.洁净纸片上
C.托盘上
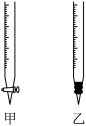
(2)滴定过程中氢氧化钠溶液放在锥形瓶中,则盐酸应该放在
_______(填“甲”或“乙”)中。该同学选用酚酞做指示剂,如何判断达到滴定终点:
_______。
(3)根据表格数据,计算被测烧碱溶液的物质的量浓度是
_______
,烧碱样品的纯度是
_______。
(4)下列实验操作会对滴定结果产生什么后果?(填“偏高”“偏低”或“无影响”)
①观察酸式滴定管液面时,开始平视,滴定终点俯视,则滴定结果
_______。
②滴定前酸式滴定管尖嘴处有气泡,滴定后气泡消失,则滴定结果
_______。
③用蒸馏水洗涤锥形瓶后未干燥,则滴定结果
_______。