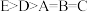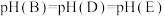水的电离平衡曲线如图所示。下列说法正确的是

| A.图中对应点的温度关系为a>b>c |
| B.纯水仅升高温度,可从a点变到c点 |
| C.水的离子积常数KW数值大小关系为b>c>d |
| D.在b点对应温度下,0.5 mol/L的H2SO4溶液与1 mol/L的KOH溶液等体积混合,充分反应后,所得溶液的pH=7 |
更新时间:2020-01-14 13:23:29
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】室温下,关于等体积、pH 均为4的醋酸和盐酸两种溶液说法正确的是
| A.两溶液的微粒总数相同 |
| B.两溶液中和氢氧化钠的能力相同 |
| C.两溶液中水的电离程度相同 |
| D.将两溶液稀释至pH 均为5所需加入的水的体积相同 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,下列叙述不正确的是
| A.c(H+)>c(OH-)的溶液一定显酸性 |
| B.pH=3 的弱酸溶液与 pH=11 的强碱溶液等体积混合后溶液呈酸性 |
| C.pH=5 的硫酸溶液稀释到原来的 500 倍,稀释后 c(SO42-)与 c(H+)之比约为 1∶10 |
| D.中和 10 mL 0.1 mol/L 醋酸与 100 mL 0.01 mol/L 醋酸所需 NaOH 的物质的量不同 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法错误的是
| A.向醋酸溶液中加水,溶液中所有粒子(不考虑水)的浓度都减小 |
| B.25°C时,pH=8的NaHA的水溶液中: c(Na+)>c(HA-)>c(H2A)>c(A2-) |
| C.等物质的量浓度的K2S和KHS混合溶液中: c(K+)>2c(S2-)+c(HS-) |
| D.25°C时,pH为5的NH4Cl与pH=9的碳酸钠溶液中,水的电离程度相同 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,关于下列两种溶液的说法不正确的是
| ① | ② | |
| pH | 12 | 12 |
| 溶质 | NaOH | NH3·H2O |
A.①中c(Na+)等于②中c(NH ) ) |
| B.两溶液中溶质的物质的量浓度:① < ② |
| C.中和等体积的两溶液所用等浓度盐酸的体积:① < ② |
| D.两溶液中水的电离程度:① < ② |
您最近半年使用:0次

 的电离程度大于其水解程度,NaHSO3溶液呈酸性
的电离程度大于其水解程度,NaHSO3溶液呈酸性
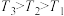
 间的关系:
间的关系: