已知 A(g)+B(g)⇌C(g)+D(g)反应的平衡常数和温度的关系如下:
830℃时,向一个2L的密闭容器中充入0.2mol的A和0.8mol的B,反应初始4s内A的平均反应速率v(A)=0.005mol/(L·s)。下列说法正确的是( )
温度 | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
| A.4s时c(B)为0.76 mol/L |
| B.830℃达平衡时,A的转化率为80% |
| C.反应达平衡后,升高温度,平衡正向移动 |
| D.1200℃时反应C(g)+D(g)⇌A(g)+B(g)的平衡常数的值为0.4 |
2014·北京丰台·一模 查看更多[18]
河北省邯郸市大名县第一中学2022-2023学年高二上学期10月月考化学试题广西梧州市藤县第六中学2021-2022学年高二上学期期中考试化学试题宁夏吴忠中学2021-2022学年高二上学期期末考试化学试题安徽省滁州九校2021-2022学年高二上学期第四次调研考试化学试题新疆乌苏市第一中学2021-2022学年高二上学期期中考试化学试题黑龙江省鸡东二中2020-2021学年高二上学期期末考试化学试题广西南宁市2020-2021学年高二上学期期末考试(原理)化学试题云南省昆明师范专科学校附属中学2020-2021学年高二上学期期中考试化学试题四川省攀枝花市第十五中学2019-2020学年高二上学期期中考试化学试题广东省中山市第一中学2018-2019学年高二上学期第一次段考化学试题【全国百强校】新疆维吾尔自治区生产建设兵团第二中学2018-2019学年高二上学期期中检测化学试题广东省中山市2017-2018学年高二上学期期末考试化学试题2017届北京市丰台区高三上学期期末化学试卷2016-2017学年河北省唐山一中高二上10月月考化学卷2017届内蒙古赤峰二中高三上第一次月考化学试卷2016届陕西省西安铁一中高三上12月模拟化学试卷2015届北京市清华大学附属中学高三3月综合测(三)化学试卷(已下线)2014届北京市丰台区高三下学期统一练习(一)化学试卷
更新时间:2014-05-06 18:16:22
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】向恒容密闭容器中充入HI发生反应2HI(g) H2(g)+I2(g) ΔH>0,T1和T2温度下,
H2(g)+I2(g) ΔH>0,T1和T2温度下, 随时间t的关系如图,下列说法不正确的是
随时间t的关系如图,下列说法不正确的是
 H2(g)+I2(g) ΔH>0,T1和T2温度下,
H2(g)+I2(g) ΔH>0,T1和T2温度下, 随时间t的关系如图,下列说法不正确的是
随时间t的关系如图,下列说法不正确的是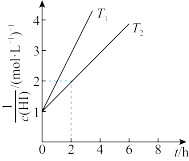
| A.T2温度下0-2h内,生成H2的平均速率为0.125mol·L-1·h-1 |
| B.T1温度下2h末和4h末HI的瞬时速率相同 |
| C.T1>T2 |
| D.若改变条件是催化剂,则T1和T2可以分别代表有、无催化剂时的反应变化示意图 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】700℃时,向容积为2L的密闭容器中充入一定量的 和
和 ,发生反应
,发生反应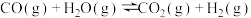 ,反应过程中测定的部分数据见下表(表中
,反应过程中测定的部分数据见下表(表中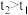 ):
):
下列说法中正确的是
 和
和 ,发生反应
,发生反应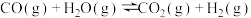 ,反应过程中测定的部分数据见下表(表中
,反应过程中测定的部分数据见下表(表中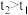 ):
):反应时间/ | 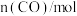 | 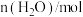 |
| 0 | 1.20 | 0.60 |
 | 0.80 | X |
 | Y | 0.20 |
A.反应在 内的平均速率为: 内的平均速率为: |
| B.加压可以加快反应速率,可以增大反应物的转化率 |
| C.700℃时该反应的平衡常数为1 |
D.保持条件不变,向平衡体系中再通入  和 和  ,则 ,则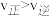 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】HI在一定条件下可发生反应2HI(g) H2(g)+I2(g)ΔH,在2L恒容密闭容器中,充入一定量的HI(g),反应物的物质的量n(mol)随时间t(min)变化的数据如下:
H2(g)+I2(g)ΔH,在2L恒容密闭容器中,充入一定量的HI(g),反应物的物质的量n(mol)随时间t(min)变化的数据如下:
根据表中数据,下列说法正确的是
 H2(g)+I2(g)ΔH,在2L恒容密闭容器中,充入一定量的HI(g),反应物的物质的量n(mol)随时间t(min)变化的数据如下:
H2(g)+I2(g)ΔH,在2L恒容密闭容器中,充入一定量的HI(g),反应物的物质的量n(mol)随时间t(min)变化的数据如下:| 实验序号 | T | 0 | 10 | 20 | 30 | 40 | 50 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 |
| 2 | 800℃ | a | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 |
| A.实验1中,反应在0至10min内,v(HI)=0.02mol·L−1·min−1 |
| B.800℃时,该反应的平衡常数K=0.25 |
| C.根据实验1和实验2可说明:反应物浓度越大,反应速率越快 |
| D.ΔH<0 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知某可逆反应 在密闭容器中进行,如图表示在不同反应时间t时,温度T和压强p与生成物C在混合气体中的体积分数
在密闭容器中进行,如图表示在不同反应时间t时,温度T和压强p与生成物C在混合气体中的体积分数 的关系曲线,由曲线分析,下列判断
的关系曲线,由曲线分析,下列判断正确 的是
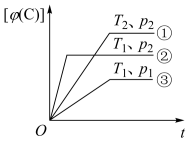
 在密闭容器中进行,如图表示在不同反应时间t时,温度T和压强p与生成物C在混合气体中的体积分数
在密闭容器中进行,如图表示在不同反应时间t时,温度T和压强p与生成物C在混合气体中的体积分数 的关系曲线,由曲线分析,下列判断
的关系曲线,由曲线分析,下列判断
A. | B.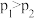 | C. | D.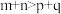 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
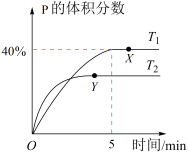
【推荐1】将1molM和2 molN置于体积为2L的恒容密闭容器中,发生反应:M(s)+2N(g) P(g)+Q(g) △H。反应过程中测得P的体积分数在不同温度下随时间的变化如图所示。下列说法正确的是( )
P(g)+Q(g) △H。反应过程中测得P的体积分数在不同温度下随时间的变化如图所示。下列说法正确的是( )
 P(g)+Q(g) △H。反应过程中测得P的体积分数在不同温度下随时间的变化如图所示。下列说法正确的是( )
P(g)+Q(g) △H。反应过程中测得P的体积分数在不同温度下随时间的变化如图所示。下列说法正确的是( )
| A.若X、Y两点的平衡常数分别为K1、K2,则K1>K2 |
| B.温度为T1时,N的平衡转化率为80%,平衡常数K=40 |
| C.无论温度为T1还是T2,当容器中气体密度和压强不变时,反应达平衡状态 |
| D.降低温度、增大压强、及时分离出产物均有利于提高反应物的平衡转化率 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定条件下的密闭容器中发生反应: 。达平衡后升高反应温度,下列叙述
。达平衡后升高反应温度,下列叙述不正确 的是
 。达平衡后升高反应温度,下列叙述
。达平衡后升高反应温度,下列叙述| A.正、逆反应速率都增大 | B.平衡向逆反应方向移动 |
C. 的转化率增大 的转化率增大 | D.化学平衡常数增大 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】羰基硫( )可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将
)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将 和一定量的
和一定量的 混合加热并达到下列平衡:
混合加热并达到下列平衡:
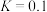 ,平衡后
,平衡后 物质的量为
物质的量为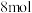 。下列说法不正确的是
。下列说法不正确的是
 )可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将
)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将 和一定量的
和一定量的 混合加热并达到下列平衡:
混合加热并达到下列平衡:
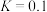 ,平衡后
,平衡后 物质的量为
物质的量为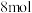 。下列说法不正确的是
。下列说法不正确的是A. 的转化率之比为1:1 的转化率之比为1:1 |
B.达平衡后 的体积分数为 的体积分数为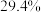 |
| C.加入正催化剂,可以加快反应速率,但不能提高平衡转化率 |
D.恒温下向平衡体系中再加入 各 各 ,平衡会移动 ,平衡会移动 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】可逆反应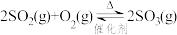 达到平衡状态后,保持温度﹑容器容积不变,向容器中充入一定量的O2,下列说法正确的是(K为平衡常数,Q为浓度商)
达到平衡状态后,保持温度﹑容器容积不变,向容器中充入一定量的O2,下列说法正确的是(K为平衡常数,Q为浓度商)
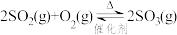 达到平衡状态后,保持温度﹑容器容积不变,向容器中充入一定量的O2,下列说法正确的是(K为平衡常数,Q为浓度商)
达到平衡状态后,保持温度﹑容器容积不变,向容器中充入一定量的O2,下列说法正确的是(K为平衡常数,Q为浓度商)| A.Q不变,K变大,O2的转化率增大 |
| B.Q减小,K不变,O2的转化率减小 |
| C.平衡常数越大表示该反应速率越快 |
| D.化学计量数变为二倍则ΔH值和K值也变为原来的二倍 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下表是有关可逆反应的数据
根据以上信息判断下列结论错误的是
| 编号 | 化学反应方程式 | 平衡常数 | 温度 | |
| 979K | 1173K | |||
| I | Fe(s) +CO2(g)  FeO(s) +CO(g) FeO(s) +CO(g) | K1 | 1.47 | 2.15 |
| II | Fe(s) +H2O(g)  FeO(s) + H2(g) FeO(s) + H2(g) | K2 | 2.38 | 1.67 |
| III | CO(g) +H2O(g)  CO2(g) +H2(g) CO2(g) +H2(g) | K3 | a | b |

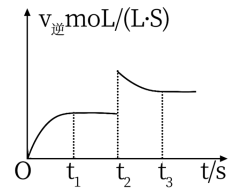
| A.反应III是放热反应 |
| B.a> b a=1.62 |
| C.若要使反应III在一定条件下平衡向逆反应方向移动,可采取措施①升高温度;②充入He气使体积增大 |
| D.反应III逆反应速率如图所示,t2时改变的条件可能是升温 |
您最近半年使用:0次

 2NH3(g)+CO2(g)。该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示,下列说法错误的是
2NH3(g)+CO2(g)。该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示,下列说法错误的是


