9. 硫元素的单质及其化合物在科学研究、工农业生产、农药的制备与使用等方面具有广泛用途。请
根据以下应用回答有关问题:
(1)已知单质硫有
S2、
S4、
S6、
S8、
Sn等多种形式,在
Sn分子内
S原子以
S—
S单键形成“锯齿形”的
n元环。试画出
S8的八元环结构式
___________。
(2)绿色农药“石硫合剂”的有效成分为五硫化钙
(CaS5)和硫代硫酸钙
(CaS2O
3),可由单质硫和熟石灰在加热条件下制得,该反应的化学方程式为(反应中单质硫要求用
S4表示);
____________。
已知多硫化钙为离子化合物,其中
S原子以
S—
S单键连接成多硫链而形成—2价的原子团,试画出五硫化钙的电子式
_________________。
(3)科学家探测出火星大气中含有一种称为硫化羰的物成,其化学式为
COS,结构与二氧化碳分子相似。硫化羰可作为一种熏蒸剂,能防止某些昆虫、线虫的危害。请你利用下表中相关共价键的键能数据:
| 共价键 | C=O | C=S | H—O | H—S |
| 键能/kJ.mol-1 | 745 | 536 | 464 | 339 |
根据有关反应原理写出硫化羰气体与水蒸气反应生成
CO
2和
H2S的热化学方程式:
______________.
(4)S
4广泛用于杀菌剂和抗真菌剂中,可由
H2S
2的燃料电池获得,其装置如下图所示。
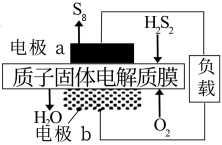
①
H2S2的名称是
________。
②电极
b为
________(选填“正极”、 “负极”)。
③电极
a上发生的电极反应为:
_______________。
(5)一氧化二硫
(S2O)常温下是一种无色、不稳定的气体,实验室可由
S8和氧化铜共热制得,同时生成硫化铜和
SO
2(注:生成物中气体产物等物质的量:升价与降价的硫也是等物质的量)。
该制备反应的化学方程式为
________;
已知
S2O常温时分解生成两种含硫的常见物质,请依据
S2O中硫元素的价态分析并写出该分解反应的化学方程式
_____________________。