室温条件下,用0.100 0 mol/L的NaOH溶液分别滴定HX、HY、HZ的溶液,三种酸溶液的体积均为20.00 mL,浓度均为0.100 0 mol/L,滴定曲线如图所示。下列叙述正确的是( )
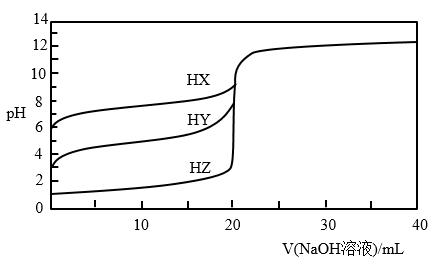

| A.酸性强弱:HX>HY>HZ |
| B.滴定这三种酸时,均可选择石蕊做指示剂 |
| C.电离常数Ka(HY)=10‒5 |
D.HZ的电离方程式为HZ H++Z‒ H++Z‒ |
更新时间:2020-11-20 10:50:35
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】向20 mL NaOH溶液中逐滴加入0.1 mol/L的醋酸溶液,滴定曲线如图所示。下列判断中,正确的是


| A.在M点,两者恰好反应完全 |
| B.确定滴定终点的指示剂可以选用甲基橙 |
| C.NaOH溶液的物质的量浓度为0.1 mol/L |
| D.在N点,c(CH3COO->c(Na+>c(H+>c(CH3COOH |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
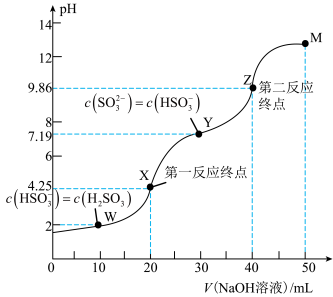
【推荐2】用 溶液滴定
溶液滴定 溶液,所得滴定曲线如图所示
溶液,所得滴定曲线如图所示 忽略混合时溶液体积的变化
忽略混合时溶液体积的变化 。下列叙述正确的是( )
。下列叙述正确的是( )
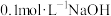 溶液滴定
溶液滴定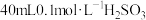 溶液,所得滴定曲线如图所示
溶液,所得滴定曲线如图所示 忽略混合时溶液体积的变化
忽略混合时溶液体积的变化 。下列叙述正确的是( )
。下列叙述正确的是( )
A.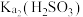 的数量级为 的数量级为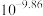 |
| B.若滴定到第二反应终点,最好选用甲基橙作指示剂 |
| C.图中各点水的电离程度:Z点最大,X点最小 |
D.图中Y点对应的溶液中: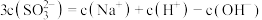 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】甲胺(CH3NH2)是一种应用广泛的一元弱碱。常温下,向20.00 mL0. 10 mol∙L-1的甲胺溶液中滴加V mL 0.10 mol·L-1盐酸,混合溶液的pH与 的关系曲线如图所示。
的关系曲线如图所示。

下列说法错误的是
 的关系曲线如图所示。
的关系曲线如图所示。
下列说法错误的是
| A.该滴定过程可选用甲基橙作指示剂 |
| B.常温下,甲胺的电离常数为Kb,则pKb=-lgKb=3.4 |
C.c点对应溶液可能存在关系:2c(H+)+c(CH3NH )=c(CH3NH2)+2c(OH-)+c(Cl-) )=c(CH3NH2)+2c(OH-)+c(Cl-) |
| D.b点对应溶液中加入盐酸的体积为20.00 mL |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】室温下, 的
的 ,向
,向 溶液中逐滴加入
溶液中逐滴加入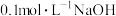 溶液,点K时达到终点。溶液的
溶液,点K时达到终点。溶液的 随
随 溶液体积的变化曲线如图所示。下列说法正确的是
溶液体积的变化曲线如图所示。下列说法正确的是

 的
的 ,向
,向 溶液中逐滴加入
溶液中逐滴加入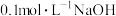 溶液,点K时达到终点。溶液的
溶液,点K时达到终点。溶液的 随
随 溶液体积的变化曲线如图所示。下列说法正确的是
溶液体积的变化曲线如图所示。下列说法正确的是
A. 溶液的浓度为 溶液的浓度为 |
B.点M时溶液中存在: |
C.点N时溶液中存在: |
D.随着 的滴入, 的滴入, 不断增大 不断增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某实验小组用稀盐酸标准液滴定未知浓度的NaOH溶液,下列操作符合实验规范的是
| A.用碱式滴定管盛装标准液 | B.用量筒准确量取NaOH溶液后注入锥形瓶中 |
| C.选用紫色石蕊溶液作指示剂 | D.滴定过程中时刻注视锥形瓶中溶液的变化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】25℃时,在20mL0.1mol•L-1一元弱酸HA溶液中滴加0.1mol•L﹣1NaOH溶液,溶液中1g[ ]与pH关系如图所示。下列说法正确的是
]与pH关系如图所示。下列说法正确的是
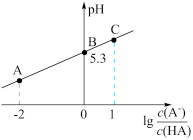
 ]与pH关系如图所示。下列说法正确的是
]与pH关系如图所示。下列说法正确的是
| A.B点对应溶液中:c(HA)>c(Na+)>c(H+)>c(OH﹣) |
| B.25℃时,HA酸的电离常数的数量级为10-5 |
C.对C点溶液加热(不考虑挥发),则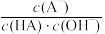 增大 增大 |
| D.B点对应的NaOH溶液体积为10mL |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法不正确的是( )
| A.已知冰的熔化热为6.0 kJ • mol-1,冰中氢键键能为20 kJ • mol-1,假设1 mol 冰中有2 mol氢键,且熔化热完全用于破坏冰的氢键,则最多只能破坏冰中15 %的氢键 |
B.已知一定温度下,醋酸溶液的物质的量浓度为c,电离度为a, 电离常数 。若加水稀释,则CH3COOH 。若加水稀释,则CH3COOH CH3COO-+H+向右移动,a增大, Ka不变 CH3COO-+H+向右移动,a增大, Ka不变 |
| C.甲烷的标准燃烧热为-890.3 kJ• mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3 kJ • mol-1 |
D.500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g) 2NH3(g)△H=-38.6kJ/mol 2NH3(g)△H=-38.6kJ/mol |
您最近一年使用:0次

 时,用
时,用 盐酸滴定
盐酸滴定 一元弱碱
一元弱碱 溶液,所得溶液的
溶液,所得溶液的
 时
时 )如图2所示。(已知:
)如图2所示。(已知: )
)
 的数量级为
的数量级为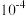
 约为
约为



