某实验小组用稀盐酸标准液滴定未知浓度的NaOH溶液,下列操作符合实验规范的是
| A.用碱式滴定管盛装标准液 | B.用量筒准确量取NaOH溶液后注入锥形瓶中 |
| C.选用紫色石蕊溶液作指示剂 | D.滴定过程中时刻注视锥形瓶中溶液的变化 |
21-22高二下·广西桂林·期末 查看更多[5]
广西桂林市2021-2022学年高二下学期期末质量检测化学试题(已下线)3.2.3 酸碱中和滴定-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)河南省鹤壁市高中2022-2023学年高二上学期10月居家测试化学(宏奥班)试题(已下线)考点巩固卷09 水溶液中的离子反应与平衡(4大考点62题)-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)实验04 强酸和强碱的中和滴定-【同步实验课】2023-2024学年高二化学教材实验大盘点(人教版2019选择性必修1)
更新时间:2022-07-15 16:28:37
|
【知识点】 酸碱中和滴定的综合考查解读
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下图曲线a和b是常温下盐酸与氢氧化钠溶液相互滴定的滴定曲线,下列叙述不正确的是
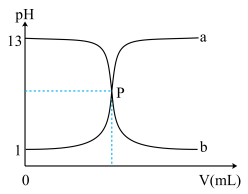

A.盐酸的物质的量浓度为0.1 | B.P点时恰好完全中和,溶液呈中性 |
| C.曲线a是盐酸滴定氢氧化钠溶液的滴定曲线 | D.甲基橙能用作本实验的指示剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,用0.10mol/LNaOH标准液滴定未知浓度的盐酸,滴定曲线如图1实线。下列说法正确的是
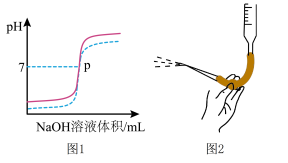

| A.滴定过程中,眼睛注视滴定管内液面变化 |
| B.若用酚酞做指示剂,滴入最后半滴NaOH标准液,溶液恰好变红,一定达到滴定终点 |
| C.装NaOH标准液时,用图2所示方法排除滴定管内的气泡 |
| D.若用该NaOH溶液滴定与盐酸相同浓度的醋酸,可用虚线表示滴定曲线,滴定终点是p点 |
您最近一年使用:0次





