某化学实验小组用0.2000 mol/L的酸性KMnO4溶液测定草酸晶体的纯度(草酸晶体化学式为H2C2O4•2H2O,杂质不与KMnO4反应).实验步骤如下:
(1)称取13.0 g草酸晶体,配成250.00 mL水溶液.此操作过程必须用到的2种定量仪器是______ 和 ______ .
(2)量取草酸溶液25.00 mL放入锥形瓶中,用0.2000 mol/L的酸性KMnO4溶液滴定.
①量取25.00 mL草酸溶液
②酸化KMnO4溶液的酸应为______ .(选填“盐酸”或“稀硫酸”或“稀硝酸”)
③配平离子方程式:_______________________ □MnO4-+□H2C2O4+□H+→□Mn2++□CO2↑+□H2O
④滴定达到终点的标志是______ .
(3)在上述实验中,下列操作一定会造成测定结果偏低的是______ .
A.称取13.0 g草酸晶体时,将草酸晶体放在托盘天平右盘
B.锥形瓶水洗后未用草酸溶液润洗
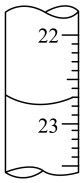
C.读取KMnO4溶液体积时,开始仰视读数,滴定结束时俯视读数
D.盛KMnO4溶液的酸式滴定管尖嘴部分有气泡,滴定后气泡消失.
(1)称取13.0 g草酸晶体,配成250.00 mL水溶液.此操作过程必须用到的2种定量仪器是
(2)量取草酸溶液25.00 mL放入锥形瓶中,用0.2000 mol/L的酸性KMnO4溶液滴定.
①量取25.00 mL草酸溶液
②酸化KMnO4溶液的酸应为
③配平离子方程式:
④滴定达到终点的标志是

(3)在上述实验中,下列操作一定会造成测定结果偏低的是
A.称取13.0 g草酸晶体时,将草酸晶体放在托盘天平右盘
B.锥形瓶水洗后未用草酸溶液润洗
C.读取KMnO4溶液体积时,开始仰视读数,滴定结束时俯视读数
D.盛KMnO4溶液的酸式滴定管尖嘴部分有气泡,滴定后气泡消失.
更新时间:2019-03-11 15:18:32
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】亚硝酸钠(NaNO2)是重要的防腐剂。某化学兴趣小组尝试制备亚硝酸钠,查阅资料:HNO2为弱酸,在酸性溶液中, 可将
可将 还原为Mn2+且无气体生成。
还原为Mn2+且无气体生成。
(一)亚硝酸钠固体含量的测定:
称取NaNO2固体样品(杂质不与酸性KMnO4溶液反应)4.000 g溶于水配成250 mL溶液,取25.00 mL溶液于锥形瓶中,用0.1000 mol/L酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
(1)第一组实验数据出现异常,造成这种异常的原因可能是______________ ( (填字母)。
A.酸式滴定管用蒸馏水洗净后未用标准液润洗
B.锥形瓶洗净后未干燥
C.滴定结束后仰视读数
(2)滴定时,将高锰酸钾标准溶液注入______________ (填“酸”或“碱”)式滴定管中。
(3)该实验滴定终点现象是________________ 。
(4)根据表中数据,计算所得固体中亚硝酸钠(M=69 g/mol)的质量分数是___________ 。
(二)反应废液的处理:
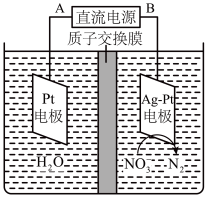
反应后溶液中存在的硝酸根,可以采用电化学降解法进行处理。25℃时,反应进行10 min,溶液的pH由7变为12,电化学降解 的原理如图所示。
的原理如图所示。
(5)电源正极为______________ (填A或B),阴极反应式为_______________ 。
 可将
可将 还原为Mn2+且无气体生成。
还原为Mn2+且无气体生成。(一)亚硝酸钠固体含量的测定:
称取NaNO2固体样品(杂质不与酸性KMnO4溶液反应)4.000 g溶于水配成250 mL溶液,取25.00 mL溶液于锥形瓶中,用0.1000 mol/L酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
| 滴定次数 | 1 | 2 | 3 | 4 |
| KMnO4溶液体积/mL | 20.60 | 20.02 | 20.00 | 19.98 |
A.酸式滴定管用蒸馏水洗净后未用标准液润洗
B.锥形瓶洗净后未干燥
C.滴定结束后仰视读数
(2)滴定时,将高锰酸钾标准溶液注入
(3)该实验滴定终点现象是
(4)根据表中数据,计算所得固体中亚硝酸钠(M=69 g/mol)的质量分数是
(二)反应废液的处理:
反应后溶液中存在的硝酸根,可以采用电化学降解法进行处理。25℃时,反应进行10 min,溶液的pH由7变为12,电化学降解
 的原理如图所示。
的原理如图所示。(5)电源正极为

您最近一年使用:0次
【推荐2】化学反应常伴随热效应.某些反应(如中和反应)的热量变化,其数值 可通过量热装置测量反应前后体系温度变化,用公式
可通过量热装置测量反应前后体系温度变化,用公式 计算获得.
计算获得.

(1)盐酸浓度的测定:移取 待测液,加入指示剂,用
待测液,加入指示剂,用
 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 (读数如图所示).
(读数如图所示).
①
______________ .
②如果滴定前俯视,终点时仰视,会导致盐酸浓度______________ (“偏高”“偏低”或“不影响”).
(2)热量的测定:取上述 溶液和盐酸各
溶液和盐酸各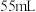 进行反应,测得反应前后体系的温度值
进行反应,测得反应前后体系的温度值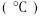 分别为
分别为 ,则该过程放出的热量为
,则该过程放出的热量为______________  (
( 和
和 分别取
分别取 和
和 ,忽略水以外各物质吸收的热量,下同).
,忽略水以外各物质吸收的热量,下同).
(3)借鉴 的方法,甲同学测量放热反应
的方法,甲同学测量放热反应 的焓变
的焓变 (忽略温度对焓变的影响,下同).实验结果见下表.
(忽略温度对焓变的影响,下同).实验结果见下表.

______________ 结果表明,该方法可行.
(4)乙同学也借鉴 的方法,测量反应
的方法,测量反应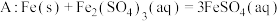 的焓变.
的焓变.
查阅资料:配制 溶液时需加入酸.加酸的目的是
溶液时需加入酸.加酸的目的是______________ .
提出猜想: 粉与
粉与 溶液混合,在反应
溶液混合,在反应 进行的过程中,可能存在
进行的过程中,可能存在 粉和酸的反应.
粉和酸的反应.
验证猜想:用 试纸测得
试纸测得 溶液的
溶液的 不大于1;向少量
不大于1;向少量 溶液中加入
溶液中加入 粉,溶液颜色变浅的同时有气泡冒出,说明存在反应
粉,溶液颜色变浅的同时有气泡冒出,说明存在反应 和
和______________ (用离子方程式表示).
实验小结:猜想成立,不能直接测反应 的焓变.
的焓变.
教师指导:鉴于以上问题,特别是气体生成带来的干扰,需要设计出实验过程中无气体生成的实验方案.
优化设计:乙同学根据盖斯定律,借助 的焓变
的焓变 与反应
与反应______________ 的焓变 获得了反应
获得了反应 的焓变.
的焓变.
 可通过量热装置测量反应前后体系温度变化,用公式
可通过量热装置测量反应前后体系温度变化,用公式 计算获得.
计算获得.
(1)盐酸浓度的测定:移取
 待测液,加入指示剂,用
待测液,加入指示剂,用
 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 (读数如图所示).
(读数如图所示).①

②如果滴定前俯视,终点时仰视,会导致盐酸浓度
(2)热量的测定:取上述
 溶液和盐酸各
溶液和盐酸各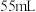 进行反应,测得反应前后体系的温度值
进行反应,测得反应前后体系的温度值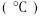 分别为
分别为 ,则该过程放出的热量为
,则该过程放出的热量为 (
( 和
和 分别取
分别取 和
和 ,忽略水以外各物质吸收的热量,下同).
,忽略水以外各物质吸收的热量,下同).(3)借鉴
 的方法,甲同学测量放热反应
的方法,甲同学测量放热反应 的焓变
的焓变 (忽略温度对焓变的影响,下同).实验结果见下表.
(忽略温度对焓变的影响,下同).实验结果见下表.| 反应试剂 | 体系温度/ | ||
| 反应前 | 反应后 | ||
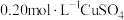 溶液 溶液 |  粉 粉 |  |  |

(4)乙同学也借鉴
 的方法,测量反应
的方法,测量反应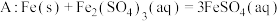 的焓变.
的焓变.查阅资料:配制
 溶液时需加入酸.加酸的目的是
溶液时需加入酸.加酸的目的是提出猜想:
 粉与
粉与 溶液混合,在反应
溶液混合,在反应 进行的过程中,可能存在
进行的过程中,可能存在 粉和酸的反应.
粉和酸的反应.验证猜想:用
 试纸测得
试纸测得 溶液的
溶液的 不大于1;向少量
不大于1;向少量 溶液中加入
溶液中加入 粉,溶液颜色变浅的同时有气泡冒出,说明存在反应
粉,溶液颜色变浅的同时有气泡冒出,说明存在反应 和
和实验小结:猜想成立,不能直接测反应
 的焓变.
的焓变.教师指导:鉴于以上问题,特别是气体生成带来的干扰,需要设计出实验过程中无气体生成的实验方案.
优化设计:乙同学根据盖斯定律,借助
 的焓变
的焓变 与反应
与反应 获得了反应
获得了反应 的焓变.
的焓变.
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】铬及其化合物在工业上用途广泛,工业废水中含有毒的铬(VI),可以利用化学方法处理。
(1)还原法处理
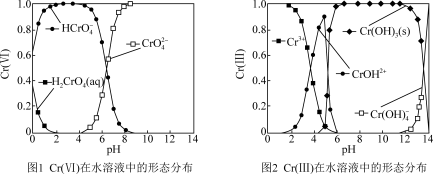
①Cr(VI)在水溶液中的形态分布如图1所示。向pH=2的含Cr(VI)污水中加入NaHSO3,发生的主要反应的离子方程式为_______ 。
②向水体中加入还原剂,将高毒性Cr(VI)还原为低毒性Cr(III),再调节溶液pH范围为_______ Cr(III)生成Cr(OH)3沉淀除去。
(2)电化学法处理
甲醇酸性燃料电池处理酸性含铬废水(主要含有 )的原理如图所示。
)的原理如图所示。
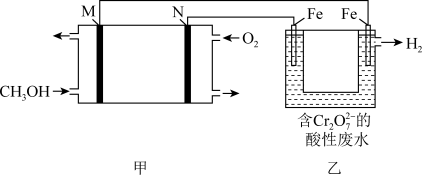
①下列说法正确的是_______ (填标号)
A.M为负极,电极反应为CH3OH+6e-+H2O=6H++CO2↑
B.甲中阴离子向N极移动
C.乙中电极均不参与电极反应
D.乙中阳极区 发生的反应为
发生的反应为 +6Fe2++14H+=2Cr3++6Fe3++7H2O
+6Fe2++14H+=2Cr3++6Fe3++7H2O
②若甲中消耗44.8L氧气(标准状况),则乙中产生_______ molH2(假设阴极只有氢离子放电)。
(3)废水中铬元素含量的测定:准确移取20.00mL含 的酸性废水,向其中加入过量的KI溶液(
的酸性废水,向其中加入过量的KI溶液( +6I-+14H+=2Cr3++3I2+7H2O),充分反应后,以
+6I-+14H+=2Cr3++3I2+7H2O),充分反应后,以_______ 为指示剂,向其中滴加0.0150mol·L-1的Na2S2O3标准溶液(I2+2 =2I-+
=2I-+ ),达到滴定终点时的现象为
),达到滴定终点时的现象为_______ ,重复实验两次,消耗Na2S2O3溶液体积的平均值为VmL。废水中铬元素的浓度为_______ mg·L-1。
(1)还原法处理

①Cr(VI)在水溶液中的形态分布如图1所示。向pH=2的含Cr(VI)污水中加入NaHSO3,发生的主要反应的离子方程式为
②向水体中加入还原剂,将高毒性Cr(VI)还原为低毒性Cr(III),再调节溶液pH范围为
(2)电化学法处理
甲醇酸性燃料电池处理酸性含铬废水(主要含有
 )的原理如图所示。
)的原理如图所示。
①下列说法正确的是
A.M为负极,电极反应为CH3OH+6e-+H2O=6H++CO2↑
B.甲中阴离子向N极移动
C.乙中电极均不参与电极反应
D.乙中阳极区
 发生的反应为
发生的反应为 +6Fe2++14H+=2Cr3++6Fe3++7H2O
+6Fe2++14H+=2Cr3++6Fe3++7H2O②若甲中消耗44.8L氧气(标准状况),则乙中产生
(3)废水中铬元素含量的测定:准确移取20.00mL含
 的酸性废水,向其中加入过量的KI溶液(
的酸性废水,向其中加入过量的KI溶液( +6I-+14H+=2Cr3++3I2+7H2O),充分反应后,以
+6I-+14H+=2Cr3++3I2+7H2O),充分反应后,以 =2I-+
=2I-+ ),达到滴定终点时的现象为
),达到滴定终点时的现象为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某学生用已知物质的量浓度的 标准溶液来测定未知物质的量浓度的盐酸时,选择酚酞作指示剂。请回答下列问题:
标准溶液来测定未知物质的量浓度的盐酸时,选择酚酞作指示剂。请回答下列问题:
(1)配制 标准溶液。配制所需的玻璃仪器有:烧杯、量筒,玻璃棒、
标准溶液。配制所需的玻璃仪器有:烧杯、量筒,玻璃棒、___________ 。
(2)滴定操作可分解为如下几步:
①检查滴定管是否漏水;
②取一定体积的待测液于锥形瓶中;
③装标准溶液和待测液并调整液面(记录初始读数);
④用标准溶液润洗盛标准溶液的滴定管,用待测液润洗盛待测液的滴定管;
⑤用蒸馏水洗涤玻璃仪器;
⑥滴定操作
正确的操作顺序为:___________ 。
(3)盛装NaOH标准溶液的仪器名称为___________ ,若滴定开始和结束时,该仪器中溶液读数如图所示,所用NaOH标准溶液的体积为___________  。
。

(4)滴定过程中边滴加边摇动锥形瓶,直到加入最后一滴 溶液后,
溶液后,___________ ,表明已经到达滴定终点。
(5)某学生根据3次实验分别记录有关数据如表所示:
依据表中数据计算该盐酸的物质的量浓度为___________  。
。
(6)在上述实验中,下列操作会造成测定结果:(填 “偏高”、“ 偏低”、 “无影响”)。
a.滴定结束后盛装标准液的滴定管有气泡___________ ;
b.碱式滴定管水洗后末用标准溶液润洗___________ ;
c.若锥形瓶盛装标准溶液,滴定管内为待测溶液,并滴定终点时俯视读数___________ 。
 标准溶液来测定未知物质的量浓度的盐酸时,选择酚酞作指示剂。请回答下列问题:
标准溶液来测定未知物质的量浓度的盐酸时,选择酚酞作指示剂。请回答下列问题:(1)配制
 标准溶液。配制所需的玻璃仪器有:烧杯、量筒,玻璃棒、
标准溶液。配制所需的玻璃仪器有:烧杯、量筒,玻璃棒、(2)滴定操作可分解为如下几步:
①检查滴定管是否漏水;
②取一定体积的待测液于锥形瓶中;
③装标准溶液和待测液并调整液面(记录初始读数);
④用标准溶液润洗盛标准溶液的滴定管,用待测液润洗盛待测液的滴定管;
⑤用蒸馏水洗涤玻璃仪器;
⑥滴定操作
正确的操作顺序为:
(3)盛装NaOH标准溶液的仪器名称为
 。
。
(4)滴定过程中边滴加边摇动锥形瓶,直到加入最后一滴
 溶液后,
溶液后,(5)某学生根据3次实验分别记录有关数据如表所示:
| 滴定次数 | 待测盐酸的体积 | 标准 溶液体积 溶液体积 | |
| 滴定前的刻度/mL | 滴定后的刻度 | ||
| 第一次 | 25.00 | 0.00 | 26.01 |
| 第二次 | 25.00 | 1.40 | 29.85 |
| 第三次 | 25.00 | 0.46 | 26.45 |
 。
。(6)在上述实验中,下列操作会造成测定结果:(填 “偏高”、“ 偏低”、 “无影响”)。
a.滴定结束后盛装标准液的滴定管有气泡
b.碱式滴定管水洗后末用标准溶液润洗
c.若锥形瓶盛装标准溶液,滴定管内为待测溶液,并滴定终点时俯视读数
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】欲测定某NaOH溶液的物质的量浓度,可用0.1000 mol/L的盐酸标准溶液进行中和滴定(用甲基橙作指示剂,相应颜色:HIn红色,过渡为橙色,In黄色)。请回答下列问题:
(1)滴定时,在其中发生中和反应的仪器名称为__________ 。
(2)盛装标准盐酸的仪器名称为____________ 。
(3)滴定终点的判定为____________ 。
(4)若甲学生在实验过程中,记录滴定前滴定管内液面读数为0.50 mL,滴定后液面如图,则此时消耗标准溶液的体积为______________ 。

(5)乙学生做了三组平行实验,数据记录如下:
选取上述合理数据,计算出待别NaOH溶液的物质的量浓度为___ (保留四位有效数字)。
(6)下列哪些操作会使测定结果偏高________ (填字母)。
A.锥形瓶用蒸馏水洗净后再用待测液润洗
B.酸式滴定管用蒸馏水洗净后再用标准液润洗
C.测定前酸式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前读数正确,滴定后俯视滴定管读数
(1)滴定时,在其中发生中和反应的仪器名称为
(2)盛装标准盐酸的仪器名称为
(3)滴定终点的判定为
(4)若甲学生在实验过程中,记录滴定前滴定管内液面读数为0.50 mL,滴定后液面如图,则此时消耗标准溶液的体积为

(5)乙学生做了三组平行实验,数据记录如下:
| 实验序号 | 待测NaOH溶液的体积/mL | 0.100 0 mol/LHCl溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25. 00 | 0.00 | 26. 29 |
| 2 | 25. 00 | 1.00 | 31.00 |
| 3 | 25.00 | 1.00 | 27.31 |
(6)下列哪些操作会使测定结果偏高
A.锥形瓶用蒸馏水洗净后再用待测液润洗
B.酸式滴定管用蒸馏水洗净后再用标准液润洗
C.测定前酸式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前读数正确,滴定后俯视滴定管读数
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】硫化亚锡( )可用作太阳能电池材料,实验室利用
)可用作太阳能电池材料,实验室利用 和
和 反应制备
反应制备 ,装置如图所示(夹持装置已省略)。
,装置如图所示(夹持装置已省略)。
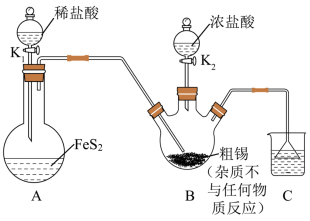
已知:还原性
回答下列问题:
(1)A中发生反应的化学方程式为_______ 。
(2) 溶液现用现制的主要原因是
溶液现用现制的主要原因是_______ 。
(3)浓盐酸的作用:一是作为反应物加快 的生成速率,二是
的生成速率,二是_______ 。
(4)为测定 纯度,进行如下操作:
纯度,进行如下操作:
①向 产品中加入
产品中加入 溶液。
溶液。
②将①中悬浊液离心过滤后,向滤液中加入 溶液,充分反应后,用淀粉溶液作指示剂,用
溶液,充分反应后,用淀粉溶液作指示剂,用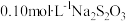 溶液进行滴定
溶液进行滴定 ,达到滴定终点时消耗
,达到滴定终点时消耗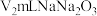 溶液,
溶液, 的纯度为
的纯度为_______  ;下列操作会使
;下列操作会使 纯度偏高的是
纯度偏高的是_______ (填标号)。
A.①中盛 溶液的滴定管未润洗
溶液的滴定管未润洗
B.②中滴定结束后滴定管中有气泡产生
C.②中离心不完全,滤液中还含有少量淡黄色沉淀
 )可用作太阳能电池材料,实验室利用
)可用作太阳能电池材料,实验室利用 和
和 反应制备
反应制备 ,装置如图所示(夹持装置已省略)。
,装置如图所示(夹持装置已省略)。
已知:还原性

回答下列问题:
(1)A中发生反应的化学方程式为
(2)
 溶液现用现制的主要原因是
溶液现用现制的主要原因是(3)浓盐酸的作用:一是作为反应物加快
 的生成速率,二是
的生成速率,二是(4)为测定
 纯度,进行如下操作:
纯度,进行如下操作:①向
 产品中加入
产品中加入 溶液。
溶液。②将①中悬浊液离心过滤后,向滤液中加入
 溶液,充分反应后,用淀粉溶液作指示剂,用
溶液,充分反应后,用淀粉溶液作指示剂,用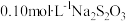 溶液进行滴定
溶液进行滴定 ,达到滴定终点时消耗
,达到滴定终点时消耗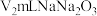 溶液,
溶液, 的纯度为
的纯度为 ;下列操作会使
;下列操作会使 纯度偏高的是
纯度偏高的是A.①中盛
 溶液的滴定管未润洗
溶液的滴定管未润洗B.②中滴定结束后滴定管中有气泡产生
C.②中离心不完全,滤液中还含有少量淡黄色沉淀
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】为验证不同化合价铁的氧化还原能力,利用下列电池装置进行实验。

回答下列问题:
(1)由FeSO4·7H2O固体配制0.10mol·L-1FeSO4溶液,需要的仪器有药匙、玻璃棒、______ (从下列图中选择,写出名称)。

(2)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入_____ 电极溶液中。
(3)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02mol·L-1。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=_______ 。
(4)根据(3)、(4)实验结果,铁电极的电极反应式为______ 。
(5)根据(3)、(4)实验结果,Fe、Fe3+、Fe2+三种微粒氧化性由强到弱的顺序是______ 。
(6)实验前需要对铁电极表面活化。在FeSO4溶液中加入几滴Fe2(SO4)3溶液,将铁电极浸泡一段时间,铁电极表面被刻蚀活化。检验活化反应完成的方法是______ 。

回答下列问题:
(1)由FeSO4·7H2O固体配制0.10mol·L-1FeSO4溶液,需要的仪器有药匙、玻璃棒、

(2)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入
(3)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02mol·L-1。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=
(4)根据(3)、(4)实验结果,铁电极的电极反应式为
(5)根据(3)、(4)实验结果,Fe、Fe3+、Fe2+三种微粒氧化性由强到弱的顺序是
(6)实验前需要对铁电极表面活化。在FeSO4溶液中加入几滴Fe2(SO4)3溶液,将铁电极浸泡一段时间,铁电极表面被刻蚀活化。检验活化反应完成的方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命。下表是1L“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
(1)“鲜花保鲜剂”中蔗糖的物质的量浓度为___________________ 。
(2)在用托盘天平称量蔗糖时,若将蔗糖放在了右盘,50g砝码放在了左盘,调节游码1.3g,则实际称量所得蔗糖质量为___________ 。
(3)配制该1L“鲜花保鲜剂”所需的玻璃仪器除了烧杯、玻璃棒、量筒外还有______________________________ 。(在横线上填写所缺仪器的名称)
(4)在配制溶液时,玻璃棒有两种不同的用途,分别是____________ 、___________ 。
| 成分 | 质量(g) | 摩尔质量(g ·mol-1) |
| 蔗糖 | 51.3 | 342 |
| 硫酸钾 | 0.50 | 174 |
| 阿司匹林 | 0.35 | 180 |
| 高锰酸钾 | 0.50 | 158 |
| 硝酸银 | 0.04 | 170 |
(2)在用托盘天平称量蔗糖时,若将蔗糖放在了右盘,50g砝码放在了左盘,调节游码1.3g,则实际称量所得蔗糖质量为
(3)配制该1L“鲜花保鲜剂”所需的玻璃仪器除了烧杯、玻璃棒、量筒外还有
(4)在配制溶液时,玻璃棒有两种不同的用途,分别是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】实验室需要480mL1mol·L-1NaOH溶液,根据溶液配制情况回答下列问题:
(1)实验中除了托盘天平(砝码)、药匙、量筒、烧杯、玻璃棒外还需要的其他仪器有___ 。
(2)如图是某同学在实验室配制该NaOH溶液的过程示意图,其中有错误的是___ (填操作序号)。

(3)下列操作会导致所配溶液的物质的量浓度偏高的是___ 。
A.配制NaOH溶液时,NaOH固体中含有Na2O杂质
B.用蒸馏水溶解NaOH固体后,立即转入容量瓶中定容
C.定容后发现液面高于刻线,可用胶头滴管将多余的水吸出
D.定容时仰视刻度线
E.用托盘天平称量 NaOH 固体时,砝码生锈
F.配制前容量瓶中有少量蒸馏水
(4)若某同学用密度为1.2g/cm3,质量分数为36.5%的浓盐酸配制100mL3mol/L的稀盐酸,需要用量筒量取浓盐酸的体积为___ mL。
(1)实验中除了托盘天平(砝码)、药匙、量筒、烧杯、玻璃棒外还需要的其他仪器有
(2)如图是某同学在实验室配制该NaOH溶液的过程示意图,其中有错误的是

(3)下列操作会导致所配溶液的物质的量浓度偏高的是
A.配制NaOH溶液时,NaOH固体中含有Na2O杂质
B.用蒸馏水溶解NaOH固体后,立即转入容量瓶中定容
C.定容后发现液面高于刻线,可用胶头滴管将多余的水吸出
D.定容时仰视刻度线
E.用托盘天平称量 NaOH 固体时,砝码生锈
F.配制前容量瓶中有少量蒸馏水
(4)若某同学用密度为1.2g/cm3,质量分数为36.5%的浓盐酸配制100mL3mol/L的稀盐酸,需要用量筒量取浓盐酸的体积为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】碱金属元素和卤族元素广泛存在,用化学用语回答下列问题。
(1)氢氟酸可以用来雕刻玻璃。请写出氟化氢的电子式:___________ 。
(2)次氯酸钠溶液(pH> 7)和溴化钠溶液混合,可以作为角膜塑形镜的除蛋白液。二者混合后,溶液变成淡黄色,该反应的离子方程式是___________ 。
(3)Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4 -SOCl2。电池的总反应可表示为4Li+ 2SOCl2 =4LiCl+S+SO2↑。组装该电池必须在无水条件下进行,原因是___________ 。
(4)利用碱金属与水的反应可测定某碱金属的相对原子质量。如图所示,仪器本身连同水和干燥管以及其内的无水氯化钙的总质量为500.0g。现将4.6g某碱金属单质投入水中,立即用带有干燥管的塞子塞紧瓶口,反应完毕后,测得整套仪器的总质量为504.4 g。
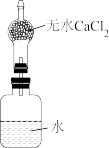
①该元素可能是___________ 。
②若不用干燥管,测得的相对原子质量比实际相对原子质量___________ (填“偏大”“偏小”或“相等”),理由是___________ 。
(5)常温下,KMnO4固体和浓盐酸反应产生氯气。为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,装置气密性已检验)。

实验过程:
I.打开弹簧夹,打开活塞a,滴加浓盐酸。
II.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
III.当B中溶液由黄色变为红棕色时,关闭活塞a。
IV. ……
①验证氯气的氧化性强于碘单质的实验现象是___________ 。
②为验证溴的氧化性强于碘,过程IV的操作和现象是_______ 。
(1)氢氟酸可以用来雕刻玻璃。请写出氟化氢的电子式:
(2)次氯酸钠溶液(pH> 7)和溴化钠溶液混合,可以作为角膜塑形镜的除蛋白液。二者混合后,溶液变成淡黄色,该反应的离子方程式是
(3)Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4 -SOCl2。电池的总反应可表示为4Li+ 2SOCl2 =4LiCl+S+SO2↑。组装该电池必须在无水条件下进行,原因是
(4)利用碱金属与水的反应可测定某碱金属的相对原子质量。如图所示,仪器本身连同水和干燥管以及其内的无水氯化钙的总质量为500.0g。现将4.6g某碱金属单质投入水中,立即用带有干燥管的塞子塞紧瓶口,反应完毕后,测得整套仪器的总质量为504.4 g。
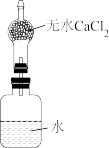
①该元素可能是
②若不用干燥管,测得的相对原子质量比实际相对原子质量
(5)常温下,KMnO4固体和浓盐酸反应产生氯气。为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,装置气密性已检验)。

实验过程:
I.打开弹簧夹,打开活塞a,滴加浓盐酸。
II.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
III.当B中溶液由黄色变为红棕色时,关闭活塞a。
IV. ……
①验证氯气的氧化性强于碘单质的实验现象是
②为验证溴的氧化性强于碘,过程IV的操作和现象是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】某盐X含有三种元素,其摩尔质量为134g/mol,常用于焰火的黄色发光剂。气体A在标准状况下的密度为1.25g/L,盐D与X组成元素完全相同。在一定条件下有如下转化关系:

请回答:
(1)盐X所含元素为_____ (请填写元素符号),盐X的化学式为_____ 。
(2)写出B转化为C的离子方程式_____ 。
(3)盐X隔绝空气加热分解生成A和D的化学方程式为_____ 。

请回答:
(1)盐X所含元素为
(2)写出B转化为C的离子方程式
(3)盐X隔绝空气加热分解生成A和D的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】节日期间因燃放鞭炮会引起空气中SO2含量增大,造成大气污染。某实验小组同学欲探究SO2的性质并测定空气中SO2的含量。
(1)他们设计如下实验装置,请你参与探究,并回答下列问题:
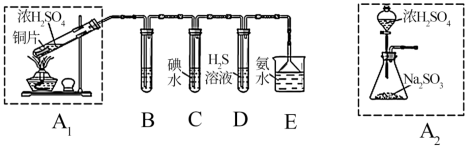
①装置A1中发生反应的化学方程式为_______ ;
②装置B用于SO2检验的漂白性,其中所盛试剂为_______ ,装置D中发生反应的化学方程式为_______ ,说明SO2具有_______ 性;
③C中发生的离子方程式为:_______ ;
④为了实现绿色环保的目标,甲同学欲用装置A2代替装置A1你认为装置A2的优点是_______ 。
(2)拟用以下两装置测定空气中SO2含量(忽略空气中其他还原性气体的干扰)。

①通过讨论,不能采用装置b,其原因是_____________ ;
②若通入V L(标准状况下)空气(M=29g/mol),恰好与145 mL0.25 mol/L酸性高锰酸钾溶液完全反应,则空气中SO2的质量分数为_______ %。(写出含V的表达式)
(1)他们设计如下实验装置,请你参与探究,并回答下列问题:

①装置A1中发生反应的化学方程式为
②装置B用于SO2检验的漂白性,其中所盛试剂为
③C中发生的离子方程式为:
④为了实现绿色环保的目标,甲同学欲用装置A2代替装置A1你认为装置A2的优点是
(2)拟用以下两装置测定空气中SO2含量(忽略空气中其他还原性气体的干扰)。

①通过讨论,不能采用装置b,其原因是
②若通入V L(标准状况下)空气(M=29g/mol),恰好与145 mL0.25 mol/L酸性高锰酸钾溶液完全反应,则空气中SO2的质量分数为
您最近一年使用:0次



