在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命。下表是1L“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
(1)“鲜花保鲜剂”中蔗糖的物质的量浓度为___________________ 。
(2)在用托盘天平称量蔗糖时,若将蔗糖放在了右盘,50g砝码放在了左盘,调节游码1.3g,则实际称量所得蔗糖质量为___________ 。
(3)配制该1L“鲜花保鲜剂”所需的玻璃仪器除了烧杯、玻璃棒、量筒外还有______________________________ 。(在横线上填写所缺仪器的名称)
(4)在配制溶液时,玻璃棒有两种不同的用途,分别是____________ 、___________ 。
| 成分 | 质量(g) | 摩尔质量(g ·mol-1) |
| 蔗糖 | 51.3 | 342 |
| 硫酸钾 | 0.50 | 174 |
| 阿司匹林 | 0.35 | 180 |
| 高锰酸钾 | 0.50 | 158 |
| 硝酸银 | 0.04 | 170 |
(2)在用托盘天平称量蔗糖时,若将蔗糖放在了右盘,50g砝码放在了左盘,调节游码1.3g,则实际称量所得蔗糖质量为
(3)配制该1L“鲜花保鲜剂”所需的玻璃仪器除了烧杯、玻璃棒、量筒外还有
(4)在配制溶液时,玻璃棒有两种不同的用途,分别是
11-12高一上·江苏南通·阶段练习 查看更多[1]
(已下线)2011-2012学年江苏省如皋中学高一上学期质量检测化学试卷
更新时间:2016-12-09 02:09:27
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】某化学实验小组需用480mL0.5mol/L的硫酸铜溶液,请回答下列问题:
(1)如果用胆矾(CuSO4·5H2O)来配制,需用胆矾的质量为__ g。
(2)下面是配制硫酸铜溶液过程中的5个操作步骤:①向盛有胆矾的烧杯中加入20mL蒸馏水使其溶解;②继续往容量瓶中加蒸馏水,至液面距刻度线1~2cm处;③将烧杯中的溶液沿玻璃棒注入500mL容量瓶中;④向烧杯中加入少量的蒸馏水,洗涤烧杯内壁和玻璃棒2~3次后移入容量瓶中,轻轻摇动容量瓶,使溶液混合均匀;⑤改用胶头滴管加蒸馏水至刻度线,盖好瓶塞,反复上下颠倒,摇匀。正确的操作顺序为___ (填序号)。
(3)上述操作中,①、③都用到玻璃棒,其作用分别为__ 、__ 。
(4)下列操作会导致所配硫酸铜溶液物质的量浓度偏低的是__ (填序号,下同);对所配溶液物质的量浓度无影响的是__ 。
①在烧杯中搅拌溶液时,有少量液体溅出
②定容摇匀后,发现溶液液面低于刻度线,又滴加蒸馏水至刻度线
③容量瓶使用前未进行干燥
④所使用的容量瓶刚用某种浓度的硫酸铜溶液润洗过
⑤定容俯视刻度线
⑥没有洗涤溶解时所用的烧杯和玻璃棒
(1)如果用胆矾(CuSO4·5H2O)来配制,需用胆矾的质量为
(2)下面是配制硫酸铜溶液过程中的5个操作步骤:①向盛有胆矾的烧杯中加入20mL蒸馏水使其溶解;②继续往容量瓶中加蒸馏水,至液面距刻度线1~2cm处;③将烧杯中的溶液沿玻璃棒注入500mL容量瓶中;④向烧杯中加入少量的蒸馏水,洗涤烧杯内壁和玻璃棒2~3次后移入容量瓶中,轻轻摇动容量瓶,使溶液混合均匀;⑤改用胶头滴管加蒸馏水至刻度线,盖好瓶塞,反复上下颠倒,摇匀。正确的操作顺序为
(3)上述操作中,①、③都用到玻璃棒,其作用分别为
(4)下列操作会导致所配硫酸铜溶液物质的量浓度偏低的是
①在烧杯中搅拌溶液时,有少量液体溅出
②定容摇匀后,发现溶液液面低于刻度线,又滴加蒸馏水至刻度线
③容量瓶使用前未进行干燥
④所使用的容量瓶刚用某种浓度的硫酸铜溶液润洗过
⑤定容俯视刻度线
⑥没有洗涤溶解时所用的烧杯和玻璃棒
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某学生准备用18.4mol/L的浓硫酸配制0.4mol/L的稀硫酸250mL,试回答下列问题:
(1)通过计算求出浓硫酸所需体积并用量筒量取,读取的数值为V=______ mL。(计算结果保留小数点后一位)
(2)下列配制溶液的操作中,正确的顺序是________ 。(填序号)
①将浓硫酸转移至含有少量蒸馏水的烧杯中,并用玻璃棒搅拌
②冷却后,将稀释好的溶液转入250mL容量瓶中
③用量筒量取V mL浓硫酸
④盖好瓶塞,反复上下颠倒,摇匀
⑤小心地往250mL容量瓶中加蒸馏水至距离刻度线1-2cm处
⑥用胶头滴管滴加蒸馏水至液面与刻度线相切
⑦用少量蒸馏水洗涤烧杯2-3次,将洗涤液转移至250mL容量瓶中,轻轻摇动容量瓶,使溶液混合均匀
(1)通过计算求出浓硫酸所需体积并用量筒量取,读取的数值为V=
(2)下列配制溶液的操作中,正确的顺序是
①将浓硫酸转移至含有少量蒸馏水的烧杯中,并用玻璃棒搅拌
②冷却后,将稀释好的溶液转入250mL容量瓶中
③用量筒量取V mL浓硫酸
④盖好瓶塞,反复上下颠倒,摇匀
⑤小心地往250mL容量瓶中加蒸馏水至距离刻度线1-2cm处
⑥用胶头滴管滴加蒸馏水至液面与刻度线相切
⑦用少量蒸馏水洗涤烧杯2-3次,将洗涤液转移至250mL容量瓶中,轻轻摇动容量瓶,使溶液混合均匀
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
真题
名校
【推荐3】实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:4NH4++6HCHO=3H++6H2O+(CH2)6N4H+[滴定时,1mol(CH2)6N4H+与1molH+相当],然后用NaOH标准溶液滴定反应生成的酸.某兴趣小组用甲醛法进行了如下实验:
步骤I:称取样品1.500g。
步骤Ⅱ:将样品溶解后,完全转移到250mL容量瓶中,定容,充分摇匀。
步骤Ⅲ:移取25.00mL样品溶液于250mL锥形瓶中,加入10mL 20%的中性甲醛溶液,摇匀、静置5min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点.按上述操作方法再重复2次。
(1)根据步骤Ⅲ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数______ (填“偏高”、“偏低”或“无影响”)。
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积______ (填“偏大”、“偏小”或“无影响”)。
③滴定时边滴边摇动锥形瓶,眼睛应观察______ 。
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由______ 色变成______ 色。
(2)滴定结果如下表所示:
若NaOH标准溶液的浓度为0.1010mol•L-1,则该样品中氮的质量分数为______ 。
步骤I:称取样品1.500g。
步骤Ⅱ:将样品溶解后,完全转移到250mL容量瓶中,定容,充分摇匀。
步骤Ⅲ:移取25.00mL样品溶液于250mL锥形瓶中,加入10mL 20%的中性甲醛溶液,摇匀、静置5min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点.按上述操作方法再重复2次。
(1)根据步骤Ⅲ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积
③滴定时边滴边摇动锥形瓶,眼睛应观察
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由
(2)滴定结果如下表所示:
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
若NaOH标准溶液的浓度为0.1010mol•L-1,则该样品中氮的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
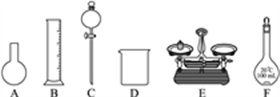
【推荐1】(1)用5.0 mol·L-1的NaOH溶液配制0.1 mol·L-1的NaOH溶液时,如下图所示的仪器中,肯定不需要的是________ (填字母),配制上述溶液还需要的玻璃仪器是________ (填仪器名称)。
(2)在容量瓶的使用方法中,下列操作不正确的是________ (填字母)。
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,不经干燥直接用于配制溶液
C.配制溶液时,将所取液体或固体直接倒入容量瓶中,缓慢加入蒸馏水到液面距容量瓶刻度线1~2 cm处时,改用胶头滴管滴加蒸馏水至溶液的凹液面最低点正好与刻度线相切
D.将容量瓶倾斜,将溶液直接沿容量瓶内壁注入容量瓶中
E.当液面达刻度线后,盖好容量瓶的瓶塞,将容量瓶反复颠倒摇匀
(3)配制溶液用的烧碱中若含有下列杂质,用此溶液测定盐酸的物质的量浓度,则所测浓度比实际浓度偏高、偏低,还是无影响?
①烧碱中含有少量KOH________ 。
②烧碱中含有少量Na2CO3________ 。
③烧碱中含有少量NaCl________ 。

(2)在容量瓶的使用方法中,下列操作不正确的是
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,不经干燥直接用于配制溶液
C.配制溶液时,将所取液体或固体直接倒入容量瓶中,缓慢加入蒸馏水到液面距容量瓶刻度线1~2 cm处时,改用胶头滴管滴加蒸馏水至溶液的凹液面最低点正好与刻度线相切
D.将容量瓶倾斜,将溶液直接沿容量瓶内壁注入容量瓶中
E.当液面达刻度线后,盖好容量瓶的瓶塞,将容量瓶反复颠倒摇匀
(3)配制溶液用的烧碱中若含有下列杂质,用此溶液测定盐酸的物质的量浓度,则所测浓度比实际浓度偏高、偏低,还是无影响?
①烧碱中含有少量KOH
②烧碱中含有少量Na2CO3
③烧碱中含有少量NaCl
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】新冠肺炎疫情期间,环境消毒是极其关键的,常常喷洒“84”消毒液,其有效成分为NaClO。已知某“84”消毒液瓶体部分标签如图所示,该“84”消毒液通常稀释100倍(体积之比)后使用,请回答下列问题:
(1)某实验需用480mL0.2mol•L-1NaClO的消毒液,现用NaClO固体配制,配制时应选用容量瓶的规格和称取NaClO的质量分别是____ 。
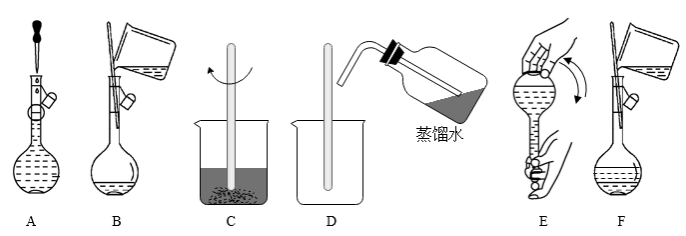
(2)如图所示配制溶液,将以下实验步骤A~F按实验过程先后次序排列_____ 。
(3)下列情况会导致溶液浓度偏低的是_____ (多选)。
A.容量瓶用蒸馏水洗净后,没烘干就直接使用
B.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒
C.溶解后未经冷却就移液
D.移液时,有少量液体溅出
E.定容时,俯视观察刻度线
(4)曾有报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分是盐酸)与“84”消毒液而发生氯气中毒事件.其离子方程式为:ClO-+Cl-+2H+=Cl2↑+H2O,其中氧化剂是:_____ ;还原性:_____>_____。_____
| 净含量:500mL 密度:1.19g•cm-3 主要成分:25%NaClO(NaClO的摩尔质量74.5g•mol-1) 注意事项:密封保存 |
| A.480mL,7.2g | B.500mL,7.2g | C.500mL,7.5g | D.任意规格,7.5g |

(3)下列情况会导致溶液浓度偏低的是
A.容量瓶用蒸馏水洗净后,没烘干就直接使用
B.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒
C.溶解后未经冷却就移液
D.移液时,有少量液体溅出
E.定容时,俯视观察刻度线
(4)曾有报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分是盐酸)与“84”消毒液而发生氯气中毒事件.其离子方程式为:ClO-+Cl-+2H+=Cl2↑+H2O,其中氧化剂是:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】用重铬酸钾法(一种氧化还原滴定法)可测定产物Fe3O4中的二价铁含量。若需配制浓度为0.1000mol·L-1的K2Cr2O7标准溶液250mL,应用电子分析天平准确称取一定质量的K2Cr2O7(已知M(K2Cr2O7)=294.0g·mol-1)
(1)计算配制250mL0.1000mol/LK2Cr2O7溶液时需要用电子分析天平准确称量K2Cr2O7的质量是___ g(保留4位有效数字)。
(2)配制溶液时,一般可以分为以下几个步骤:
①称量②计算③溶解④颠倒摇匀⑤转移⑥洗涤⑦定容⑧冷却
完成该溶液配制,将其正确的操作顺序为____ 。本实验必须用到的仪器有天平、药匙、烧杯、量筒,还有____ 。
(3)使用容量瓶前必须进行的一步操作是____ 。
(4)配制0.1000mol/LK2Cr2O7溶液时,下列操作会引起所配溶液浓度偏高的是____ 。
①向容量瓶中转移液体时,玻璃棒的末端位于容量瓶刻度线以上
②没有洗涤烧杯和玻璃棒且未将洗涤液注入容量瓶
③转移溶液时不慎有少量溶液洒到容量瓶外面
④容量瓶不干燥,含有少量蒸馏水
⑤定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线
⑥定容时俯视刻度线
⑦称量一定质量的K2Cr2O7中含有KCl杂质
(5)配制0.1000mol/LK2Cr2O7溶液,定容时不慎加水超过了刻度线,应如何处理:_____ 。
(1)计算配制250mL0.1000mol/LK2Cr2O7溶液时需要用电子分析天平准确称量K2Cr2O7的质量是
(2)配制溶液时,一般可以分为以下几个步骤:
①称量②计算③溶解④颠倒摇匀⑤转移⑥洗涤⑦定容⑧冷却
完成该溶液配制,将其正确的操作顺序为
(3)使用容量瓶前必须进行的一步操作是
(4)配制0.1000mol/LK2Cr2O7溶液时,下列操作会引起所配溶液浓度偏高的是
①向容量瓶中转移液体时,玻璃棒的末端位于容量瓶刻度线以上
②没有洗涤烧杯和玻璃棒且未将洗涤液注入容量瓶
③转移溶液时不慎有少量溶液洒到容量瓶外面
④容量瓶不干燥,含有少量蒸馏水
⑤定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线
⑥定容时俯视刻度线
⑦称量一定质量的K2Cr2O7中含有KCl杂质
(5)配制0.1000mol/LK2Cr2O7溶液,定容时不慎加水超过了刻度线,应如何处理:
您最近一年使用:0次



