18. I.由于温室效应和资源短缺等问题,如何降低大气中的CO
2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO
2生产燃料甲醇。一定条件下发生反应:CO
2(g)+3H
2(g)

CH
3OH(g)+H
2O(g),如图表示该反应进行过程中能量(单位为kJ·mol
-1)的变化。
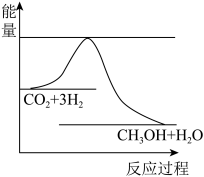
(1)关于该反应的下列说法中,正确的是_______。(填字母)
| A.△H>0,△S>0 | B.△H>0,△S<0 | C.△H<0,△S<0 | D.△H<0,△S>0 |
(2)该反应平衡常数K的表达式为K=
_______。
(3)温度降低,平衡常数K
_______(填“增大”、“不变”或“减小”)。
(4)为探究反应原理,现进行如下实验:在体积为1L的恒容密闭容器中,充入1molCO
2和3molH
2,测得CO
2和CH
3OH(g)的浓度随时间变化如下图所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率v(H
2)为
_______ mol·L
-1·min
-1。
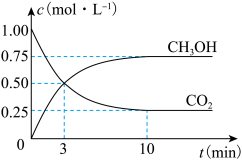
(5)下列措施中能使(4)中n(CH
3OH)/n(CO
2)增大的有
_______。(填字母)
A.升高温度
B.加入催化剂
C.将H
2O(g)从体系中分离
D.再充入1molCO
2和3molH
2E.充入He(g),使体系总压强增大
II.在一恒容的密闭容器中,进行如下化学反应:CO
2(g)+H
2(g)

CO(g)+H
2O(g),其化学平衡常数K和温度T的关系如下表:
| T(℃) | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(6)该反应为
_______反应(选填“吸热”、“放热”)。
(7)能判断该反应达到化学平衡状态的依据是
_______(多选扣分)。
a.容器中压强不变 b.c(CO
2)=c(CO)
c.V
正(H
2)=V
逆(H
2O) d.混合气体中 c(CO)不变
(8)830K时,各物质浓度符合下式:c(CO
2)·c(H
2)=2c(CO)·c(H
2O),此时该反应
_______(填“正反应方向进行”、“逆反应方向进行”或“处于平衡状态”)。