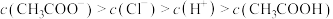常温下,将KOH溶液滴加到某二元弱酸(H2R )中,混合溶pH与 或
或 的变化关系如图所示,下列叙述正确的是。
的变化关系如图所示,下列叙述正确的是。
 或
或 的变化关系如图所示,下列叙述正确的是。
的变化关系如图所示,下列叙述正确的是。
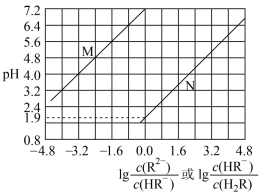
| A.Ka2 (H2R)的数量级为10-7 |
| B.常温时,NaHR溶液显酸性 |
C.曲线N表示pH与 的变化关系 的变化关系 |
| D.当混合溶液呈中性时,c(K+ )>c(R2- )>(HR- )>(OH- )=(H+) |
2022·黑龙江哈尔滨·二模 查看更多[3]
浙江省浙江大学附属中学(玉泉校区)2022-2023学年高二上学期期中考试 高二化学试卷(已下线)第14练 用“五点”法突破盐类水解及酸碱混合相关图像-2022年【暑假分层作业】高二化学(2023届一轮复习通用)黑龙江省哈尔滨市第三中学2022届高三下学期第二次模拟考试理科综合化学试题
更新时间:2022-06-15 11:37:23
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】一定温度下,水溶液中 和
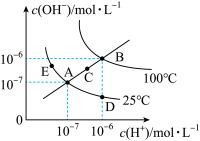
和 的浓度变化曲线如下图所示,下列说法不正确的是
的浓度变化曲线如下图所示,下列说法不正确的是
 和
和 的浓度变化曲线如下图所示,下列说法不正确的是
的浓度变化曲线如下图所示,下列说法不正确的是
A.图中五点对应的 间的关系: 间的关系: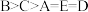 |
B.从A点到E点,可采用在水中加入少量NaOH或 的方法 的方法 |
C.从A点到D点,所得D点溶液中水电离产生的 浓度不可能为 浓度不可能为 |
D.在B点温度下,将 的硫酸溶液与 的硫酸溶液与 的KOH溶液混合(忽略混合后溶液体积的变化)后溶液 的KOH溶液混合(忽略混合后溶液体积的变化)后溶液 ,则硫酸溶液与KOH溶液的体积比为9:11 ,则硫酸溶液与KOH溶液的体积比为9:11 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】常温下,Ca(OH)2的溶解度为0.16克/100克水。向盛有50毫升水的烧杯中加入2克生石灰,搅拌后恢复到原温。下列说法正确的是
| A.在此过程中,水的Kw值始终保持不变 |
| B.在此过程中,Ca(OH)2的电离程度先变大后变小,最后不变 |
| C.反应结束后,溶液中水的电离程度比纯水小 |
| D.最后所得体系中的平衡状态只有水的电离平衡 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下列说法正确的是
| A.常温下,将pH=3的醋酸溶液稀释到原体积的10倍后,溶液的pH=4 |
| B.为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH。若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸 |
| C.用0.2000 mol•L-1 NaOH标准溶液滴定HCl与CH3COOH的混合液(混合液中两种酸的浓度均约为0.1 mol•L-1),当pH=7时,溶液中的酸恰好完全中和 |
| D.相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1 mol•L-1盐酸、③0.1 mol•L-1氯化镁溶液、④0.1 mol•L-1硝酸银溶液中,Ag+浓度:④>①>②>③ |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】常温下,RNH2+H2O⇌OH-+ 的平衡常数K=4×10-4,在某体系中,
的平衡常数K=4×10-4,在某体系中, 与OH-等离子不能穿过隔膜,RNH2可自由穿过该膜。设溶液中的c(R)=c(RNH2)+c(
与OH-等离子不能穿过隔膜,RNH2可自由穿过该膜。设溶液中的c(R)=c(RNH2)+c( ),当达到平衡时,两侧溶液的pH如图所示。
),当达到平衡时,两侧溶液的pH如图所示。
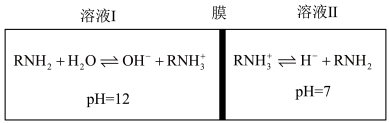
下列叙述错误的是
 的平衡常数K=4×10-4,在某体系中,
的平衡常数K=4×10-4,在某体系中, 与OH-等离子不能穿过隔膜,RNH2可自由穿过该膜。设溶液中的c(R)=c(RNH2)+c(
与OH-等离子不能穿过隔膜,RNH2可自由穿过该膜。设溶液中的c(R)=c(RNH2)+c( ),当达到平衡时,两侧溶液的pH如图所示。
),当达到平衡时,两侧溶液的pH如图所示。
下列叙述错误的是
| A.溶液I、II中的c(RNH2)相等 |
B.溶液II中c(H+)=c(OH-)-c( ) ) |
C.溶液I中c(RNH2):c( )=25:1 )=25:1 |
D.溶液I中c( )小于溶液II中c( )小于溶液II中c( ) ) |
您最近一年使用:0次
单选题
|
较难
(0.4)
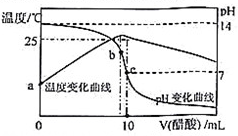
【推荐1】常温下,用 的盐酸滴定20mL相同浓度的某一元碱BOH溶液,滴定过程中pH及电导率变化曲线如图所示:
的盐酸滴定20mL相同浓度的某一元碱BOH溶液,滴定过程中pH及电导率变化曲线如图所示:
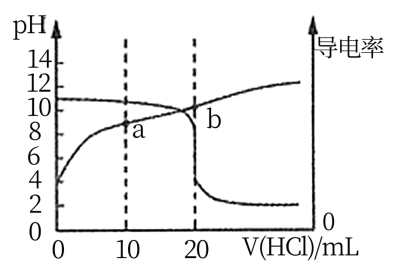
下列说法正确的是
 的盐酸滴定20mL相同浓度的某一元碱BOH溶液,滴定过程中pH及电导率变化曲线如图所示:
的盐酸滴定20mL相同浓度的某一元碱BOH溶液,滴定过程中pH及电导率变化曲线如图所示:
下列说法正确的是
| A.BOH的Kb约为1×10-3 |
| B.a点的c(B+)大于b点 |
| C.a点溶液中:c(B+)+c(H+)=2c(OH-)+c(BOH) |
| D.滴定至pH=7时,c(B+)=c(Cl-)<0.1mol•L-1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
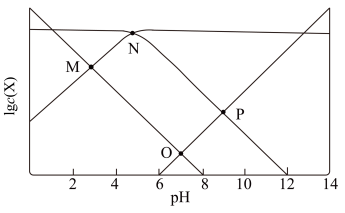
【推荐2】 时,某混合溶液中c(CH3COOH)+c(CH3COO-)=0.1mol/L,
时,某混合溶液中c(CH3COOH)+c(CH3COO-)=0.1mol/L, 、
、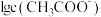 、
、 和
和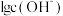 随
随 变化的关系如图所示。
变化的关系如图所示。 为
为 的电离常数,下列说法正确的是
的电离常数,下列说法正确的是
 时,某混合溶液中c(CH3COOH)+c(CH3COO-)=0.1mol/L,
时,某混合溶液中c(CH3COOH)+c(CH3COO-)=0.1mol/L, 、
、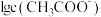 、
、 和
和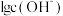 随
随 变化的关系如图所示。
变化的关系如图所示。 为
为 的电离常数,下列说法正确的是
的电离常数,下列说法正确的是
A.O点时, |
B.N点时, |
C.该体系中,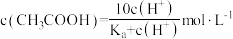 |
D. 由7到14的变化过程中, 由7到14的变化过程中, 的水解程度始终增大 的水解程度始终增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】下列说法正确的是
 常温下,强酸溶液的
常温下,强酸溶液的 ,将溶液的体积稀释到原来的
,将溶液的体积稀释到原来的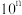 倍,则
倍,则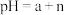
 已知
已知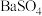 的
的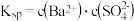 ,所以在
,所以在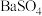 溶液中有
溶液中有
 将
将 的NaHS和
的NaHS和 的
的 溶液等体积混合,所得溶液中有
溶液等体积混合,所得溶液中有
 在
在 氨水中滴加
氨水中滴加 盐酸,刚好完全中和时
盐酸,刚好完全中和时 ,由水电离产生的
,由水电离产生的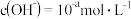 .
.

 常温下,强酸溶液的
常温下,强酸溶液的 ,将溶液的体积稀释到原来的
,将溶液的体积稀释到原来的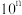 倍,则
倍,则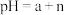
 已知
已知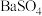 的
的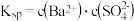 ,所以在
,所以在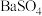 溶液中有
溶液中有
 将
将 的NaHS和
的NaHS和 的
的 溶液等体积混合,所得溶液中有
溶液等体积混合,所得溶液中有
 在
在 氨水中滴加
氨水中滴加 盐酸,刚好完全中和时
盐酸,刚好完全中和时 ,由水电离产生的
,由水电离产生的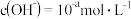 .
.A. | B. | C. | D. |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】某废水处理过程中始终保持H2S饱和,即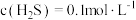 通过调节pH使
通过调节pH使 和
和 形成硫化物而分离,体系中pH与-lg c的关系如图所示,c为
形成硫化物而分离,体系中pH与-lg c的关系如图所示,c为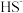 、
、 、
、 和
和 的浓度,单位为
的浓度,单位为 。已知
。已知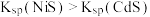 ,下列说法错误的是
,下列说法错误的是
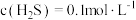 通过调节pH使
通过调节pH使 和
和 形成硫化物而分离,体系中pH与-lg c的关系如图所示,c为
形成硫化物而分离,体系中pH与-lg c的关系如图所示,c为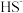 、
、 、
、 和
和 的浓度,单位为
的浓度,单位为 。已知
。已知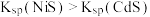 ,下列说法错误的是
,下列说法错误的是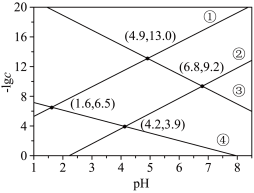
A.①为pH与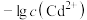 的关系曲线 的关系曲线 |
B.反应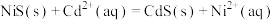 的平衡常数K为107.6 的平衡常数K为107.6 |
C.调节pH的过程中,始终有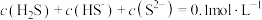 |
D.pH=10.7时,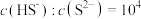 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】H3PO3是制造塑料稳定剂的原料。常温下,向100mL0.5mol·L-1H3PO3溶液中滴加等浓度的NaOH溶液,混合溶液中所有含磷微粒的物质的量分数(δ)与溶液pOH[pOH=-lgc(OH-)]的关系如图所示。下列说法错误的是
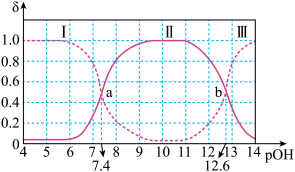

A.H3PO3的结构简式为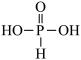 |
| B.a点水电离出的c(OH-)=1×10-7.4mol·L-1 |
C.当pH=4时,c(HPO )=c(H3PO3) )=c(H3PO3) |
| D.b点时加入NaOH溶液的体积为50mL |
您最近一年使用:0次

 的
的 溶液与
溶液与 的
的 等体积混合,溶液
等体积混合,溶液 ,则
,则 溶液和氨水,氨水的导电能力明显强于
溶液和氨水,氨水的导电能力明显强于 呈酸性,
呈酸性, 溶液呈中性,可推知
溶液呈中性,可推知 是强酸还是弱酸,可测
是强酸还是弱酸,可测 溶液的
溶液的 溶液和
溶液和 的水解程度一样
的水解程度一样 的比值和
的比值和 的比值均增大
的比值均增大 的
的 、
、 混合溶液中:
混合溶液中: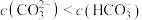 ,且
,且
 的醋酸钠溶液10mL与
的醋酸钠溶液10mL与