乙酸甲酯转化为乙醇的反应原理为CH3COOCH3(g)+2H2(g)⇌C2H5OH(g)+CH3OH(g) ΔH<0。该反应中反应速率随时间变化的关系如图所示,t1、t3、t4时刻分别改变某一外界条件。下列说法错误的是
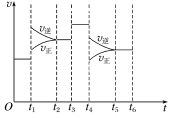

| A.t1时升高温度 |
| B.t3时加入催化剂 |
| C.t4时增大反应容器的容积,使体系压强减小 |
| D.在反应保持化学平衡的时间段中,C2H5OH的体积分数最小的时间段是t2~t3 |
更新时间:2022/10/13 15:05:34
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列关于可逆反应的叙述正确的是
| A.可逆反应是指既能向正反应方向进行,同时又能向逆反应方向进行的反应 |
B.2H2O 2H2+O2与2H2+O2 2H2+O2与2H2+O2 2H2O互为可逆反应 2H2O互为可逆反应 |
| C.对于可逆反应,当正反应速率增大时,逆反应速率就会减小 |
| D.外界条件对可逆反应的正、逆反应速率影响的程度不一定相同 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列由实验现象得出的结论不正确 的是
| 操作 | 现象及结论 | |
| A | 铁钉连接电源负极、铜片连接电源正极,加入CuSO4作为电解质溶液,接通电源 | 一段时间后,铁钉上产生一层红色物质,说明Cu2+得电子生成了Cu单质 |
| B | 将充满NO2的密闭玻璃球浸泡在热水中 | 玻璃球中红棕色加深,说明反应2NO2(g)  N2O4(g) ΔH<0 N2O4(g) ΔH<0 |
| C | FeCl3溶液加入到略有浑浊的天然淡水中 | 静置后水变澄清,说明Fe3+具有吸附性 |
| D | 测定0.1mol/LNa2CO3溶液的pH=8 | 说明 离子水解: 离子水解: +H2O +H2O HCO HCO +OH- +OH- |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】反应aA(g)+bB(g)⇌cC(g) ΔH<0在等容条件下进行。改变其它反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如图所示,下列说法不正确的是


| A.反应的化学方程式中,a:b:c=1:3:2 |
| B.第II阶段反应温度小于第III阶段反应温度 |
| C.A的平均反应速率vⅠ(A)、vⅡ(A)、vⅢ(A),最大的是vⅠ(A) |
| D.由第一次平衡到第二次平衡,采取的措施是从反应体系中移走C |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】目前工业上处理有机废水的一种方法是:在调节好pH和Mn2+浓度的废水中加入H2O2,使有机物氧化降解。现设计如下对比实验(实验条件见下表),实验测得有机物R浓度随时间变化的关系如下图所示。下列说法正确的是
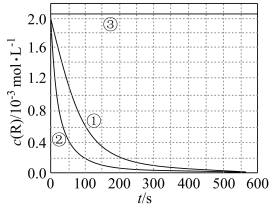

实验编号 | T/K | pH | c/10-3 mol/L | |
H2O2 | Mn2+ | |||
① | 298 | 3 | 6.0 | 0.30 |
② | 313 | 3 | 6.0 | 0.30 |
③ | 298 | 9 | 6.0 | 0.30 |
| A.313K时,在0~100s内有机物R降解的平均速率为:0.014 mol·L-1·s-1 |
| B.对比①②实验,可以得出温度越高越有利于有机物R的降解 |
| C.对比①②实验,可以发现在两次实验中有机物R的降解百分率不同 |
| D.通过以上三组实验,若想使反应停止,可以向反应体系中加入一定量的NaOH溶液 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】一定温度下,反应 的焓变为
的焓变为 、现将1mol
、现将1mol 充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是
充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是
 的焓变为
的焓变为 、现将1mol
、现将1mol 充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是
充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是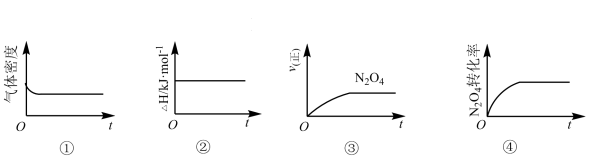
| A.①② | B.①④ | C.②④ | D.③④ |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在某一恒容容器中发生反应:
 。当反应达到平衡时,
。当反应达到平衡时, 、
、 、
、 、
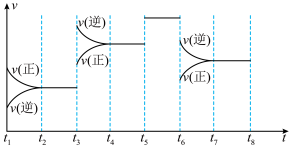
、 改变某一条件,反应速率与反应时间的曲线关系如图。下列说法错误的是
改变某一条件,反应速率与反应时间的曲线关系如图。下列说法错误的是

 。当反应达到平衡时,
。当反应达到平衡时, 、
、 、
、 、
、 改变某一条件,反应速率与反应时间的曲线关系如图。下列说法错误的是
改变某一条件,反应速率与反应时间的曲线关系如图。下列说法错误的是
A. 时刻,改变的条件可能是适当降低温度 时刻,改变的条件可能是适当降低温度 |
B. 时可能增大了反应物活化分子百分数 时可能增大了反应物活化分子百分数 |
C. 时刻,改变的条件一定是催化剂 时刻,改变的条件一定是催化剂 |
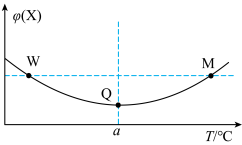
D.Q(g)的体积分数最高的时间段是 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】某恒温密闭容器发生可逆反应:Z(?)+W(?) X(g)+Y(?)△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件。下列有关说法中正确的是
X(g)+Y(?)△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件。下列有关说法中正确的是

 X(g)+Y(?)△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件。下列有关说法中正确的是
X(g)+Y(?)△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件。下列有关说法中正确的是
| A.t1~t2时间段与t3时刻后,两时间段反应体系中气体的平均摩尔质量可能相等也可能不等 |
| B.Z和W在该条件下至少有一个是为气态 |
| C.若在该温度下此反应平衡常数表达式为K=c(X),则t1~t2时间段与t3时刻后的X浓度不相等 |
| D.若该反应只在某温度T以上自发进行,则该反应的平衡常数K随温度升高而减小 |
您最近半年使用:0次


 3Z(g),反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是( )
3Z(g),反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是( )