解题方法
1 . 某小组同学查到一份研究过氧化氢溶液与氢碘酸( )反应的实验资料,具体如下。
)反应的实验资料,具体如下。
资料1:室温下,过氧化氢溶液可与氢碘酸反应: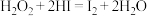
资料2:碘单质溶于水后,溶液为棕黄色。
资料3:实验数据如表所示。
(1)通过资料了中的数据,可以得出的结论是_______ 。
(2)资料3中编号为1的实验继续反应,20s后测得过氧化氢浓度为 ,则
,则
_______ 。
(3)该小组同学欲用碘化钾替代氢碘酸验证上述实验。在实验过程中,未观察到溶液变为棕黄色,却观察到有无色气体产生。于是,该小组同学提出假设: 可能是过氧化氢分解反应的催化剂。
可能是过氧化氢分解反应的催化剂。
①小组同学提出上述假设的依据是_______ 。
②请设计实验方案验证假设: 可能是过氧化氢分解反应的催化剂。(仪器和试剂可自选)
可能是过氧化氢分解反应的催化剂。(仪器和试剂可自选)
实验方案:_______ 。
(4)某研究人员通过研究得到以下两组数据( 为反应的活化能)。
为反应的活化能)。
第1组:
第2组:
结合第1组和第2组数据,你认为他所研究的问题是_______ 。
 )反应的实验资料,具体如下。
)反应的实验资料,具体如下。资料1:室温下,过氧化氢溶液可与氢碘酸反应:
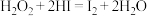
资料2:碘单质溶于水后,溶液为棕黄色。
资料3:实验数据如表所示。
| 实验编号 | 1 | 2 | 3 | 4 | 5 |
 | 0.1 | 0.1 | 0.1 | 0.2 | 0.3 |
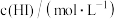 | 0.1 | 0.2 | 0.3 | 0.1 | 0.1 |
| 从混合到出现棕黄色时间/s | 13 | 6.5 | 4.3 | 6.6 | 4.4 |
(2)资料3中编号为1的实验继续反应,20s后测得过氧化氢浓度为
 ,则
,则
(3)该小组同学欲用碘化钾替代氢碘酸验证上述实验。在实验过程中,未观察到溶液变为棕黄色,却观察到有无色气体产生。于是,该小组同学提出假设:
 可能是过氧化氢分解反应的催化剂。
可能是过氧化氢分解反应的催化剂。①小组同学提出上述假设的依据是
②请设计实验方案验证假设:
 可能是过氧化氢分解反应的催化剂。(仪器和试剂可自选)
可能是过氧化氢分解反应的催化剂。(仪器和试剂可自选)实验方案:
(4)某研究人员通过研究得到以下两组数据(
 为反应的活化能)。
为反应的活化能)。第1组:
| 反应 | 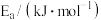 |  | 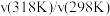 |
| A | 100 | 298→318 | 14.0 |
| 反应 | 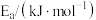 |  |
| A | 100 | 3205 |
| B | 120 |
您最近半年使用:0次
解题方法
2 . 动手实践。
请利用实验室提供的用品探究实验室制备氢气的最佳条件。
实验用品:
锌粒,铁钉,镁条,稀硫酸( ,
, ,
, );
);
大试管,秒表,导管,单孔塞,双孔塞,量筒,水槽,广口瓶,烧杯,玻璃棒,镊子,胶头滴管。
(1)请设计实验方案_______ 。
(2)请画出实验装置示意图_______ 。
(3)请设计实验记录单,包括实验现象、收集气体的体积、收集气体所用时间等_______ 。
(4)由此实验可得出什么结论_______ ?
请利用实验室提供的用品探究实验室制备氢气的最佳条件。
实验用品:
锌粒,铁钉,镁条,稀硫酸(
 ,
, ,
, );
);大试管,秒表,导管,单孔塞,双孔塞,量筒,水槽,广口瓶,烧杯,玻璃棒,镊子,胶头滴管。
(1)请设计实验方案
(2)请画出实验装置示意图
(3)请设计实验记录单,包括实验现象、收集气体的体积、收集气体所用时间等
(4)由此实验可得出什么结论
您最近半年使用:0次
21-22高一·全国·假期作业
解题方法
3 . 为了说明影响化学反应速率的因素,甲、乙、丙、丁四位同学分别设计了如下四个实验,你认为结论不正确的是
| A.在相同条件下,等质量的大理石块和大理石粉分别与相同浓度的盐酸反应时,大理石粉的反应快 |
| B.将相同大小、相同形状的镁条和铝条分别与相同浓度的盐酸反应时,二者的化学反应速率相等 |
| C.将相同浓度、相同体积的浓硝酸分别放在暗处和强光处,会发现光照可以加快浓硝酸的分解 |
| D.室温下,向两支试管中分别加入相同浓度、相同体积的双氧水,再向其中一支试管中加入少量二氧化锰粉末,二者产生氧气的快慢不同 |
您最近半年使用:0次
2022-11-26更新
|
225次组卷
|
3卷引用:第01讲 化学反应速率-【寒假自学课】2022年高一化学寒假精品课(苏教版2019必修第二册)
(已下线)第01讲 化学反应速率-【寒假自学课】2022年高一化学寒假精品课(苏教版2019必修第二册)2019版鲁科化学必修第二册第2章第3节 化学反应的快慢和限度课后习题6.1.2影响化学反应速率的因素(课中)-2019苏教版必修2课前课中课后
解题方法
4 . 等质量的铁与过量盐酸在不同的实验条件下进行反应(实验数据见下表),c为初始时盐酸的浓度( ),测定反应相同时间后产生氢气的体积V。则值最大的组是
),测定反应相同时间后产生氢气的体积V。则值最大的组是_______ (填组别序),其原因是_______ 。
 ),测定反应相同时间后产生氢气的体积V。则值最大的组是
),测定反应相同时间后产生氢气的体积V。则值最大的组是| 组别 | 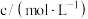 | 温度/℃ | 铁的状态 |
| 1 | 2.0 | 25 | 块状 |
| 2 | 2.5 | 30 | 粉末 |
| 3 | 2.5 | 50 | 块状 |
| 4 | 2.5 | 50 | 粉末 |
您最近半年使用:0次
名校
解题方法
5 . 某化学小组欲测定KClO3溶液与NaHSO3溶液反应的化学反应速率。所用试剂为10mL0.1mol/LKClO3溶液和10mL0.3mol/L NaHSO3溶液,所得数据如图所示。
已知:ClO +3HSO
+3HSO =Cl-+3SO
=Cl-+3SO +3H+。
+3H+。
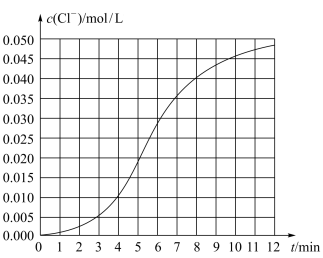
(1)根据实验数据可知,该反应在0~4min的平均反应速率:v(Cl-)=____ mol/(L·min)。
(2)某同学仔细分析实验数据后发现,在反应过程中,该反应的化学反应速率先增大,12min后逐渐变慢(12min后图略)。
i.小组同学针对这一现象进一步通过测定c(Cl-)随时间变化的曲线探究速率先增大的原因,具体如表所示。
①补全方案I中的实验操作:____ 。
②方案II中的假设为____ 。
③除I、II、III中的假设外,还可以提出的假设是____ 。
④在已知方案I的假设不成立的情况下,某同学从控制变量的角度思考,认为方案III中实验操作设计不严谨,请进行改进:____ 。
ii.12min后,化学反应速率变慢的原因是_____ 。
已知:ClO
 +3HSO
+3HSO =Cl-+3SO
=Cl-+3SO +3H+。
+3H+。
(1)根据实验数据可知,该反应在0~4min的平均反应速率:v(Cl-)=
(2)某同学仔细分析实验数据后发现,在反应过程中,该反应的化学反应速率先增大,12min后逐渐变慢(12min后图略)。
i.小组同学针对这一现象进一步通过测定c(Cl-)随时间变化的曲线探究速率先增大的原因,具体如表所示。
| 方案 | 假设 | 实验操作 |
| I | 该反应放热,使溶液温度升高,反应速率加快 | 向烧杯中加入10mL0.1mol/LKClO3溶液和10mL0.3mol/LNaHSO3溶液,_____ |
| II | ____ | 取10mL0.1mol/L KClO3溶液加入烧杯中,向其中加入少量NaCl固体,再加入10mL0.3mol/LNaHSO3溶液 |
| III | 溶液酸性增强加快了化学反应速率 | 分别向2只烧杯中加入10mL0.1mol/LKClO3溶液;向烧杯①中加入1mL水,向烧杯②中加入1mL0.2mol/L盐酸;再分别向2只烧杯中加入10mL0.3mol/LNaHSO3溶液 |
②方案II中的假设为
③除I、II、III中的假设外,还可以提出的假设是
④在已知方案I的假设不成立的情况下,某同学从控制变量的角度思考,认为方案III中实验操作设计不严谨,请进行改进:
ii.12min后,化学反应速率变慢的原因是
您最近半年使用:0次
2022-06-18更新
|
440次组卷
|
12卷引用:【全国百强校】浙江省余姚中学2018-2019学年高一下学期3月月考化学试题
【全国百强校】浙江省余姚中学2018-2019学年高一下学期3月月考化学试题课时1 化学反应的速率——A学习区 夯实基础(人教版必修2)课时1 化学反应的速率——A学习区 夯实基础(人教版(2019)第二册)必修第二册RJ第6章第二节 化学反应的速率与限度 课时1人教版(2019)高二化学选择性必修1第二章 化学反应速率与化学平衡 第一节 化学反应速率 课时2 影响化学反应速率的因素河南省洛阳市2020-2021学年高一下学期期中考试化学试题选择性必修1(SJ)专题2第一单元课时2 影响化学反应速率的因素河北省任丘一中2021-2022学年高二上学期阶段考试(一)化学试题贵州省“三新”改革联盟2021-2022学年高一下学期校联考等级考(四)化学试题北京海淀区八一学校2021-2022学年高一下学期6月月考化学试题2019版鲁科化学必修第二册第2章本章自我评价课后习题2.1.2影响化学反应速率的因素 课后
解题方法
6 . 实验室通常用大理石(或石灰石)与稀盐酸反应制取二氧化碳,不用纯碱与盐酸或硫酸反应制取二氧化碳的考虑是:(1)纯碱比大理石(或石灰石)成本高,不经济;(2)反应速率太快,难以控制和收集产物。反应速率可以通过改变反应条件来控制。作为研究,请你提出用纯碱与盐酸反应制取二氧化碳的适宜途径,并用实验来检验你的设计________________ 。
您最近半年使用:0次



