动手实践。
请利用实验室提供的用品探究实验室制备氢气的最佳条件。
实验用品:
锌粒,铁钉,镁条,稀硫酸( ,
, ,
, );
);
大试管,秒表,导管,单孔塞,双孔塞,量筒,水槽,广口瓶,烧杯,玻璃棒,镊子,胶头滴管。
(1)请设计实验方案_______ 。
(2)请画出实验装置示意图_______ 。
(3)请设计实验记录单,包括实验现象、收集气体的体积、收集气体所用时间等_______ 。
(4)由此实验可得出什么结论_______ ?
请利用实验室提供的用品探究实验室制备氢气的最佳条件。
实验用品:
锌粒,铁钉,镁条,稀硫酸(
 ,
, ,
, );
);大试管,秒表,导管,单孔塞,双孔塞,量筒,水槽,广口瓶,烧杯,玻璃棒,镊子,胶头滴管。
(1)请设计实验方案
(2)请画出实验装置示意图
(3)请设计实验记录单,包括实验现象、收集气体的体积、收集气体所用时间等
(4)由此实验可得出什么结论
更新时间:2022-11-26 10:52:48
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题。
(1)实验①的目的是________________________________________ ,实验中滴加 溶液的目的是
溶液的目的是______________________________________________ 。
(2)实验②中未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出对上述操作的改进意见是________________________________________________ (用实验中所提供的试剂和仪器)。
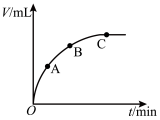
(3)某同学在50mL一定浓度的 溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的瞬时反应速率最慢的是
溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的瞬时反应速率最慢的是______________ 。
| 实验编号 | 实验操作 | 实验现象 |
| ① | 分别在试管A、B中加入5mL5% 溶液,各滴入2滴1mol/L 溶液,各滴入2滴1mol/L 溶液,待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡,将试管B放入盛有40℃左右热水的烧杯中浸泡 溶液,待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡,将试管B放入盛有40℃左右热水的烧杯中浸泡 | 试管A中不再产生气泡,试管B中产生气泡的量增大 |
| ② | 另取两支试管分别加入5mL5% 溶液和5mL10% 溶液和5mL10% 溶液 溶液 | 两试管中均未明显见到有气泡产生 |
 溶液的目的是
溶液的目的是(2)实验②中未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出对上述操作的改进意见是
(3)某同学在50mL一定浓度的
 溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的瞬时反应速率最慢的是
溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的瞬时反应速率最慢的是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究。他们利用Cu、Fe、Mg和不同浓度的硫酸溶液(0.5mol/L、2mol/L、18.4mol/L),设计实验方案来研究影响反应速率的因素。
甲同学研究的实验报告如表所示:
(1)甲同学的实验目的是_______ 。
乙同学为了更精确地研究浓度对反应速率的影响,利用如图所示装置进行定量实验。
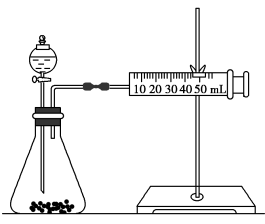
(2)乙同学在实验中应该测定的数据是_______ 。
(3)乙同学完成该实验应选用的实验药品是_______ 。
甲同学研究的实验报告如表所示:
| 实验步骤 | 现象 | 结论 |
| ①分别取等体积2mol/L硫酸溶液于三支试管中 ②向三支试管中分别投入大小、形状相同的Cu、Fe、Mg | 反应速率: ,Cu不反应 ,Cu不反应 | 金属的性质越活泼,反应速率越快 |
乙同学为了更精确地研究浓度对反应速率的影响,利用如图所示装置进行定量实验。

(2)乙同学在实验中应该测定的数据是
(3)乙同学完成该实验应选用的实验药品是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】某小组利用 溶液和硫酸酸化的
溶液和硫酸酸化的 溶液反应来探究“外界条件对化学反应速率的影响”。实验时通过测定酸性
溶液反应来探究“外界条件对化学反应速率的影响”。实验时通过测定酸性 溶液褪色所需时间来判断反应的快慢。该小组设计了如下方案。已知:
溶液褪色所需时间来判断反应的快慢。该小组设计了如下方案。已知:
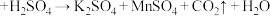
(1)配平下列化学方程式:___________ 。
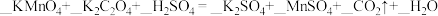
(2)表中
___________ mL,
___________ mL。
(3)探究温度对化学反应速率影响的实验编号是___________ (填编号,下同),可探究反应物浓度对化学反应速率影响的实验编号___________ 。
(4)除通过测定酸性 溶液褪色所需时间来比较反应速率外,本实验还可通过测定
溶液褪色所需时间来比较反应速率外,本实验还可通过测定___________ 来比较化学反应速率。
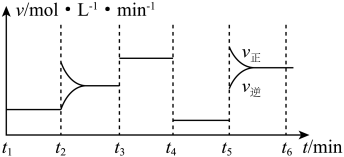
(5)小组同学发现反应速率总是如图所示,其中 时间内速率变快的主要原因可能是①产物
时间内速率变快的主要原因可能是①产物 是该反应的催化剂、②
是该反应的催化剂、②___________ 。
(6)实验①测得 溶液的褪色时间为2min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率
溶液的褪色时间为2min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率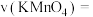
___________  。
。
 溶液和硫酸酸化的
溶液和硫酸酸化的 溶液反应来探究“外界条件对化学反应速率的影响”。实验时通过测定酸性
溶液反应来探究“外界条件对化学反应速率的影响”。实验时通过测定酸性 溶液褪色所需时间来判断反应的快慢。该小组设计了如下方案。已知:
溶液褪色所需时间来判断反应的快慢。该小组设计了如下方案。已知:
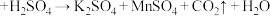
| 实验编号 | 实验温度/℃ |  酸性 酸性 溶液的体积/mL | 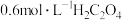 溶液的体积/mL |  的体 的体积/mL | 溶液褪色所 需时间/min |
| ① | 25 | 10 | 10 | 30 | |
| ② | 50 | 10 | 10 |  | |
| ③ | 25 | 10 |  | 35 |
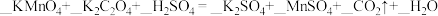
(2)表中


(3)探究温度对化学反应速率影响的实验编号是
(4)除通过测定酸性
 溶液褪色所需时间来比较反应速率外,本实验还可通过测定
溶液褪色所需时间来比较反应速率外,本实验还可通过测定(5)小组同学发现反应速率总是如图所示,其中
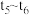 时间内速率变快的主要原因可能是①产物
时间内速率变快的主要原因可能是①产物 是该反应的催化剂、②
是该反应的催化剂、②
(6)实验①测得
 溶液的褪色时间为2min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率
溶液的褪色时间为2min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率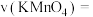
 。
。
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】某实验小组用 KI溶液、
KI溶液、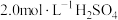 溶液、淀粉溶液等来探究外界条件对反应速率的影响,部分实验数据如表所示,查阅资料知:超过一定温度时,淀粉分子的热运动会使淀粉分子螺旋卷曲舒展开,此时淀粉与碘分子作用的显色现象消失,冷却后淀粉分子恢复螺旋卷曲的形状,淀粉与碘的显色现象会再次出现。
溶液、淀粉溶液等来探究外界条件对反应速率的影响,部分实验数据如表所示,查阅资料知:超过一定温度时,淀粉分子的热运动会使淀粉分子螺旋卷曲舒展开,此时淀粉与碘分子作用的显色现象消失,冷却后淀粉分子恢复螺旋卷曲的形状,淀粉与碘的显色现象会再次出现。
请回答下列问题:
(1)a=_______ ,b=_______ 。
(2)写出该反应的离子方程式:_______ 。
(3)Ⅰ、Ⅱ、Ⅲ、Ⅴ四组实验中,反应速率最快的是_______ (填标号)组、下列关于Ⅳ组实验没有出现蓝色可能的原因是_______ 。
(4)通过比较分析实验数据,总结外界条件对该反应的反应速率的影响。
①对比的实验:Ⅰ和Ⅱ,得出的结论是_______ 。
②对比的实验:_______ ,得出的结论是_______ 。
③对比的实验:_______ ,得出的结论是_______ 。(可不填满,也可增加)
 KI溶液、
KI溶液、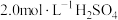 溶液、淀粉溶液等来探究外界条件对反应速率的影响,部分实验数据如表所示,查阅资料知:超过一定温度时,淀粉分子的热运动会使淀粉分子螺旋卷曲舒展开,此时淀粉与碘分子作用的显色现象消失,冷却后淀粉分子恢复螺旋卷曲的形状,淀粉与碘的显色现象会再次出现。
溶液、淀粉溶液等来探究外界条件对反应速率的影响,部分实验数据如表所示,查阅资料知:超过一定温度时,淀粉分子的热运动会使淀粉分子螺旋卷曲舒展开,此时淀粉与碘分子作用的显色现象消失,冷却后淀粉分子恢复螺旋卷曲的形状,淀粉与碘的显色现象会再次出现。| 编号 | 温度/℃ |  溶液体积/mL 溶液体积/mL | KI溶液体积/mL |  体积溶液/mL 体积溶液/mL | 淀粉溶液体积/mL | 出现蓝色所需时间/s |
| Ⅰ | 40 | 10 | 10 | 9 | 1 | 20 |
| Ⅱ | 20 | 10 | 10 | 9 | 1 | 80 |
| Ⅲ | 20 | 8 | 10 | a | 1 | 98 |
| Ⅳ | 80 | 10 | 10 | 9 | 1 | 没有出现蓝色 |
| Ⅴ | 20 | 8 | 8 | b | 1 | 120 |
(1)a=
(2)写出该反应的离子方程式:
(3)Ⅰ、Ⅱ、Ⅲ、Ⅴ四组实验中,反应速率最快的是
(4)通过比较分析实验数据,总结外界条件对该反应的反应速率的影响。
①对比的实验:Ⅰ和Ⅱ,得出的结论是
②对比的实验:
③对比的实验:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】 是一种常见试剂,在实验室、工业生产上有广泛用途。
是一种常见试剂,在实验室、工业生产上有广泛用途。
I. 不稳定、易分解,
不稳定、易分解, 等对其分解起催化作用,为比较
等对其分解起催化作用,为比较 和
和 对
对 分解的催化效果,某化学研究小组同学分别设计了如图甲、乙两种实验装置。
分解的催化效果,某化学研究小组同学分别设计了如图甲、乙两种实验装置。
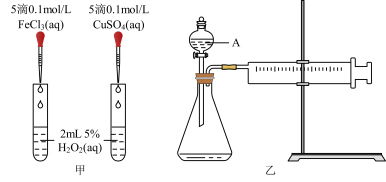
(1)若利用图甲装置,可通过观察___________ 现象,从而定性比较得出结论。
(2)有同学提出将 改为
改为___________  更为合理,其理由是
更为合理,其理由是___________ 。
(3)若利用乙实验可进行定量分析,实验时均以生成 气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是
气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是___________ 。
(4)如图为某小组研究的酸、碱对 分解的影响。该小组提出可以用
分解的影响。该小组提出可以用 固体与
固体与 溶液反应制
溶液反应制 ,反应的化学方程式为
,反应的化学方程式为___________ ,支持这一方案的理由是___________ 。
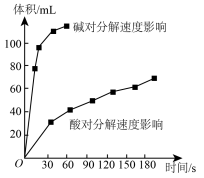
Ⅱ.实验室用 快速制氧气,其分解速率受多种因素影响。实验测得
快速制氧气,其分解速率受多种因素影响。实验测得 时不同条件下
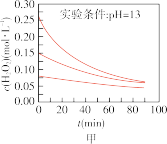
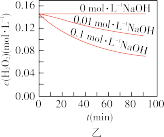
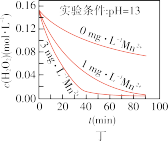
时不同条件下 浓度随时间的变化如甲、乙、丙、丁四图所示:
浓度随时间的变化如甲、乙、丙、丁四图所示:

(5)下列说法正确的是:___________(填字母序号)
(6)催化剂 在反应中,改变了
在反应中,改变了___________ (填字母序号)
A.反应速率 B.反应限度 C.反应焓变 D.反应路径 E.反应活化能 F.活化分子百分数
 是一种常见试剂,在实验室、工业生产上有广泛用途。
是一种常见试剂,在实验室、工业生产上有广泛用途。I.
 不稳定、易分解,
不稳定、易分解, 等对其分解起催化作用,为比较
等对其分解起催化作用,为比较 和
和 对
对 分解的催化效果,某化学研究小组同学分别设计了如图甲、乙两种实验装置。
分解的催化效果,某化学研究小组同学分别设计了如图甲、乙两种实验装置。
(1)若利用图甲装置,可通过观察
(2)有同学提出将
 改为
改为 更为合理,其理由是
更为合理,其理由是(3)若利用乙实验可进行定量分析,实验时均以生成
 气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是
气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是(4)如图为某小组研究的酸、碱对
 分解的影响。该小组提出可以用
分解的影响。该小组提出可以用 固体与
固体与 溶液反应制
溶液反应制 ,反应的化学方程式为
,反应的化学方程式为
Ⅱ.实验室用
 快速制氧气,其分解速率受多种因素影响。实验测得
快速制氧气,其分解速率受多种因素影响。实验测得 时不同条件下
时不同条件下 浓度随时间的变化如甲、乙、丙、丁四图所示:
浓度随时间的变化如甲、乙、丙、丁四图所示:



(5)下列说法正确的是:___________(填字母序号)
A.图甲表明,其他条件相同时, 浓度越小,其分解越慢 浓度越小,其分解越慢 |
B.图乙表明,其他条件相同时,溶液碱性越弱, 分解越快 分解越快 |
C.图丙表明,少量 存在时,溶液碱性越强, 存在时,溶液碱性越强, 分解越快 分解越快 |
D.图丁表明,碱性溶液中, 浓度越大,对 浓度越大,对 分解速率的影响越大 分解速率的影响越大 |
 在反应中,改变了
在反应中,改变了A.反应速率 B.反应限度 C.反应焓变 D.反应路径 E.反应活化能 F.活化分子百分数
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】3%的H2O2溶液是一种常用的外伤消毒剂,某校化学兴趣小组利用H2O2溶液探究影响化学反应速率的因素,实验设计如下表所示:
①实验的目的是探究 __________________ 、_____________ 对化学反应速率的影响。
②若 t2>t3,表明浓度越大,化学反应速率越______ (填“大”或“小”)。
③能表明温度对反应速率有影响的实验编号是①和______________ 。
④请你再提出一个影响H2O2分解速率的因素:_______________ 。
| 实验编号 | H2O2溶液的体积/mL | H2O2溶液的浓度 | 水浴温度/℃ | 收集50mLO2所需时间/s |
| ① | 25 | 5% | 30 | t1 |
| ② | 25 | 5% | 20 | t2 |
| ③ | 25 | 10% | 20 | t3 |
②若 t2>t3,表明浓度越大,化学反应速率越
③能表明温度对反应速率有影响的实验编号是①和
④请你再提出一个影响H2O2分解速率的因素:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】资料显示不同浓度的硫酸与锌反应时,硫酸可以被还原为SO2,也可被还原为氢气。为了验证这一事实,某同学拟用下图装置进行实验(实验时压强为10lkPa,温度为0℃)。
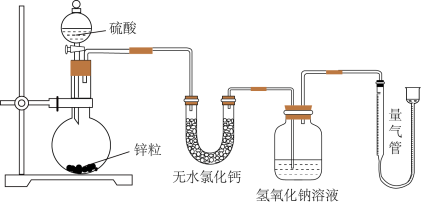
回答下列问题:
(1)将市售浓硫酸(98%)与水等体积混合,得到稀硫酸的浓度______ 49%(填“大于”“小于”或“等于”) ;
(2)在烧瓶放入1.30g锌片,与一定量某浓度的硫酸溶液反应,为保证实验结论的可靠,在洗气瓶中加入1mol/L NaOH溶液的体积最少是_____ mL,量气管的适宜规格是_______ (填:200 mL、400 mL或500 mL )。
(3)某次实验结果,测得量器管内气体的相对分子质量为2.62,推测其原因是:__________ ;
(4)1.30g 锌片完全溶解,若氢氧化钠洗气瓶增重0.64g ,则发生反应的化学方程式为:_________
(5)某次实验在烧瓶中投入少量铜粒,结果化学反应明显加快,其原因可能是:__________ 。
(6)待烧瓶中锌粒完全溶解后,从溶液中得到硫酸锌晶体的方法______ (填操作步骤)。

回答下列问题:
(1)将市售浓硫酸(98%)与水等体积混合,得到稀硫酸的浓度
(2)在烧瓶放入1.30g锌片,与一定量某浓度的硫酸溶液反应,为保证实验结论的可靠,在洗气瓶中加入1mol/L NaOH溶液的体积最少是
(3)某次实验结果,测得量器管内气体的相对分子质量为2.62,推测其原因是:
(4)1.30g 锌片完全溶解,若氢氧化钠洗气瓶增重0.64g ,则发生反应的化学方程式为:
(5)某次实验在烧瓶中投入少量铜粒,结果化学反应明显加快,其原因可能是:
(6)待烧瓶中锌粒完全溶解后,从溶液中得到硫酸锌晶体的方法
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】某化学课外小组用如图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
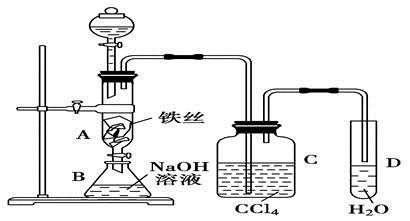
(1)写出A中反应的化学方程式:___________
(2)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是___________
(3)C中盛放CCl4的作用是___________
(4)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入___________ 溶液,现象是___________ 。

(1)写出A中反应的化学方程式:
(2)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是
(3)C中盛放CCl4的作用是
(4)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】用如图所示的装置做铝热反应实验,回答下列问题:
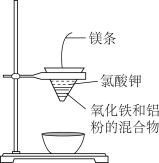
(1)写出该反应的化学方程式:___ ,在该反应中___ 是氧化剂,___ 是还原剂,该反应称为___ 反应。
(2)选出该实验的实验现象(把序号填写在横线上):___ 。
①镁条剧烈燃烧;②放出大量的热,并发出耀眼的光芒,火星四射;③纸漏斗的下部被烧穿;④有红热状态的液珠落入蒸发皿内的细沙上,液珠冷却后变为黑色固体。
(3)写出下列操作或物质的作用:内层纸漏斗底部剪一个孔:___ ;蒸发皿盛沙:___ ;镁条:___ ;氯酸钾:___ 。

(1)写出该反应的化学方程式:
(2)选出该实验的实验现象(把序号填写在横线上):
①镁条剧烈燃烧;②放出大量的热,并发出耀眼的光芒,火星四射;③纸漏斗的下部被烧穿;④有红热状态的液珠落入蒸发皿内的细沙上,液珠冷却后变为黑色固体。
(3)写出下列操作或物质的作用:内层纸漏斗底部剪一个孔:
您最近一年使用:0次



