为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题。
(1)实验①的目的是________________________________________ ,实验中滴加 溶液的目的是
溶液的目的是______________________________________________ 。
(2)实验②中未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出对上述操作的改进意见是________________________________________________ (用实验中所提供的试剂和仪器)。
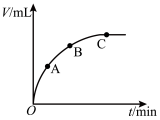
(3)某同学在50mL一定浓度的 溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的瞬时反应速率最慢的是
溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的瞬时反应速率最慢的是______________ 。
| 实验编号 | 实验操作 | 实验现象 |
| ① | 分别在试管A、B中加入5mL5% 溶液,各滴入2滴1mol/L 溶液,各滴入2滴1mol/L 溶液,待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡,将试管B放入盛有40℃左右热水的烧杯中浸泡 溶液,待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡,将试管B放入盛有40℃左右热水的烧杯中浸泡 | 试管A中不再产生气泡,试管B中产生气泡的量增大 |
| ② | 另取两支试管分别加入5mL5% 溶液和5mL10% 溶液和5mL10% 溶液 溶液 | 两试管中均未明显见到有气泡产生 |
 溶液的目的是
溶液的目的是(2)实验②中未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出对上述操作的改进意见是
(3)某同学在50mL一定浓度的
 溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的瞬时反应速率最慢的是
溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的瞬时反应速率最慢的是
19-20高二·全国·课时练习 查看更多[2]
人教版(2019)高二选择性必修第一册 第二章 化学反应速率与化学平衡 第一节 化学反应速率(已下线)第2章 化学反应速率与化学平衡(基础过关卷)-【高效检测】2021-2022学年高二化学章末测试卷(人教版2019选择性必修1)
更新时间:2020-10-05 10:42:26
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】I.分别取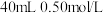 盐酸与
盐酸与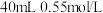 氢氧化钠溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热
氢氧化钠溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热 。请回答下列问题:
。请回答下列问题:
(1)本实验除烧杯、量筒、环形玻璃搅拌棒外还缺少的玻璃仪器名称为_______ ,大小烧杯间需要填满碎泡沫塑料的目的是_______ 。
(2)若某同学通过该实验测定出中和热 偏大,请分析可能的原因是
偏大,请分析可能的原因是_______ (填序号)。
A.用量筒量取盐酸时仰视读数
B.分多次将 溶液倒入盛有盐酸的小烧杯中
溶液倒入盛有盐酸的小烧杯中
C.将盐酸错取为等浓度的醋酸
Ⅱ.为探究化学反应速率的影响因素,设计的实验方案如下表:(已知 溶液、
溶液、 溶液、淀粉三种溶液混合,无明显现象,滴入溶液后溶液变蓝)
溶液、淀粉三种溶液混合,无明显现象,滴入溶液后溶液变蓝)
(3)写出混合溶液中滴入 溶液反应的离子方程式为
溶液反应的离子方程式为_______ 。
(4)表中的V=_______  ,
, 、
、 、
、 由小到大的顺序为
由小到大的顺序为_______ 。
(5)对比实验①②可推测实验结论为_______ 。
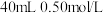 盐酸与
盐酸与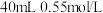 氢氧化钠溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热
氢氧化钠溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热 。请回答下列问题:
。请回答下列问题:(1)本实验除烧杯、量筒、环形玻璃搅拌棒外还缺少的玻璃仪器名称为
(2)若某同学通过该实验测定出中和热
 偏大,请分析可能的原因是
偏大,请分析可能的原因是A.用量筒量取盐酸时仰视读数
B.分多次将
 溶液倒入盛有盐酸的小烧杯中
溶液倒入盛有盐酸的小烧杯中C.将盐酸错取为等浓度的醋酸
Ⅱ.为探究化学反应速率的影响因素,设计的实验方案如下表:(已知
 溶液、
溶液、 溶液、淀粉三种溶液混合,无明显现象,滴入溶液后溶液变蓝)
溶液、淀粉三种溶液混合,无明显现象,滴入溶液后溶液变蓝)向烧杯中加入的试剂及用量/ | |||||||
0.1 溶液 溶液 | 0.1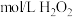 溶液 溶液 | 0.1 溶液 溶液 | 淀粉溶液 |  | 时间/s | ||
| ① | 25℃ | 20.0 | 10.0 | 5.0 | 1.0 | 0.0 |  |
| ② | 40℃ | 20.0 | 10.0 | 5.0 | 1.0 | 0.0 |  |
| ③ | 25℃ | 20.0 | 5.0 | 5.0 | 1.0 | V |  |
 溶液反应的离子方程式为
溶液反应的离子方程式为(4)表中的V=
 ,
, 、
、 、
、 由小到大的顺序为
由小到大的顺序为(5)对比实验①②可推测实验结论为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】某实验小组用 KI溶液、
KI溶液、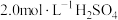 溶液、淀粉溶液等来探究外界条件对反应速率的影响,部分实验数据如表所示,查阅资料知:超过一定温度时,淀粉分子的热运动会使淀粉分子螺旋卷曲舒展开,此时淀粉与碘分子作用的显色现象消失,冷却后淀粉分子恢复螺旋卷曲的形状,淀粉与碘的显色现象会再次出现。
溶液、淀粉溶液等来探究外界条件对反应速率的影响,部分实验数据如表所示,查阅资料知:超过一定温度时,淀粉分子的热运动会使淀粉分子螺旋卷曲舒展开,此时淀粉与碘分子作用的显色现象消失,冷却后淀粉分子恢复螺旋卷曲的形状,淀粉与碘的显色现象会再次出现。
请回答下列问题:
(1)a=_______ ,b=_______ 。
(2)写出该反应的离子方程式:_______ 。
(3)Ⅰ、Ⅱ、Ⅲ、Ⅴ四组实验中,反应速率最快的是_______ (填标号)组、下列关于Ⅳ组实验没有出现蓝色可能的原因是_______ 。
(4)通过比较分析实验数据,总结外界条件对该反应的反应速率的影响。
①对比的实验:Ⅰ和Ⅱ,得出的结论是_______ 。
②对比的实验:_______ ,得出的结论是_______ 。
③对比的实验:_______ ,得出的结论是_______ 。(可不填满,也可增加)
 KI溶液、
KI溶液、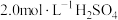 溶液、淀粉溶液等来探究外界条件对反应速率的影响,部分实验数据如表所示,查阅资料知:超过一定温度时,淀粉分子的热运动会使淀粉分子螺旋卷曲舒展开,此时淀粉与碘分子作用的显色现象消失,冷却后淀粉分子恢复螺旋卷曲的形状,淀粉与碘的显色现象会再次出现。
溶液、淀粉溶液等来探究外界条件对反应速率的影响,部分实验数据如表所示,查阅资料知:超过一定温度时,淀粉分子的热运动会使淀粉分子螺旋卷曲舒展开,此时淀粉与碘分子作用的显色现象消失,冷却后淀粉分子恢复螺旋卷曲的形状,淀粉与碘的显色现象会再次出现。| 编号 | 温度/℃ |  溶液体积/mL 溶液体积/mL | KI溶液体积/mL |  体积溶液/mL 体积溶液/mL | 淀粉溶液体积/mL | 出现蓝色所需时间/s |
| Ⅰ | 40 | 10 | 10 | 9 | 1 | 20 |
| Ⅱ | 20 | 10 | 10 | 9 | 1 | 80 |
| Ⅲ | 20 | 8 | 10 | a | 1 | 98 |
| Ⅳ | 80 | 10 | 10 | 9 | 1 | 没有出现蓝色 |
| Ⅴ | 20 | 8 | 8 | b | 1 | 120 |
(1)a=
(2)写出该反应的离子方程式:
(3)Ⅰ、Ⅱ、Ⅲ、Ⅴ四组实验中,反应速率最快的是
(4)通过比较分析实验数据,总结外界条件对该反应的反应速率的影响。
①对比的实验:Ⅰ和Ⅱ,得出的结论是
②对比的实验:
③对比的实验:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】某研究性学习小组利用H2C2O4溶液和酸性KMnO4溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,实验如下:
(1)通过实验A、B,可探究出H2C2O4溶液浓度的改变对反应速率的影响,其中V1=___________ ;通过实验___________ 可探究出温度变化对化学反应速率的影响。
(2)若t1<8,则由此实验可以得出的结论是___________ 。
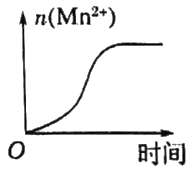
(3)该反应中有无色无味气体产生,且锰被还原为Mn2+,该小组的一位同学通过查阅资料发现,上述实验过程中n(Mn2+)随时间变化的趋势如图所示,并认为造成此种变化的原因是反应体系中的某种粒子对KMnO4与草酸之间的反应有某种特殊的作用,则该作用是___________ ,相应的粒子最可能是___________ 。
| 实验序号 | 实验温度/K | 参加反应的物质 | 溶液颜色褪至无色时所需时间s | ||||
| KMnO4溶液(含硫酸) | H2C2O4溶液 | H2O | |||||
| V/mL | c(mol/L) | V/mL | c(mol/L) | V/mL | |||
| A | 293 | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
| B | 293 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
| C | 313 | 2 | 0.02 | V2 | 0.1 | 1 | t1 |
(2)若t1<8,则由此实验可以得出的结论是
(3)该反应中有无色无味气体产生,且锰被还原为Mn2+,该小组的一位同学通过查阅资料发现,上述实验过程中n(Mn2+)随时间变化的趋势如图所示,并认为造成此种变化的原因是反应体系中的某种粒子对KMnO4与草酸之间的反应有某种特殊的作用,则该作用是

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】I.如图所示,800℃时A、B、C三种气体在密闭容器中反应时的浓度变化,分析图像回答问题:
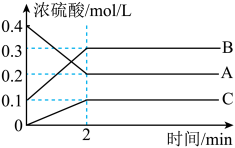
(1)2min内,用C表示的反应速率为______________ 。
(2)该反应的方程式为______________ 。
(3)在其他条件下,测得A的反应速率为0.05 mol/(L·s),此时的反应与800℃时相比,________ 。
A.比800℃ 时快 B.比800℃ 时慢 C.和800℃ 时速率一样
Ⅱ.学习小组甲利用H2C2O4溶液和酸性KMnO4溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如表实验:
(4)通过实验A、B,可探究出___________ (填外部因素)的改变对化学反应速率的影响,其中V1=_____ 、T1=_____ ;通过实验________ (填实验序号)可探究出温度变化对化学反应速率的影响,其中V2=_______ ,t2_______ 8 (填写“=”、“>”或“<”)。
(5)若t1<8,则由此实验可以得出的结论是_______ 。

(1)2min内,用C表示的反应速率为
(2)该反应的方程式为
(3)在其他条件下,测得A的反应速率为0.05 mol/(L·s),此时的反应与800℃时相比,
A.比800℃ 时快 B.比800℃ 时慢 C.和800℃ 时速率一样
Ⅱ.学习小组甲利用H2C2O4溶液和酸性KMnO4溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如表实验:
实验序号 | 实验温度/K | 有关物质 | 溶液颜色褪至无色所需时间/s | ||||
酸性KMnO4溶液 | H2C2O4溶液 | H2O | |||||
| V/mL | c/mol•L-1 | V/mL | c/mol•L-1 | V/mL | |||
A | 293 | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
C | 313 | 2 | 0.02 | V2 | 0.1 | 1 | t2 |
(5)若t1<8,则由此实验可以得出的结论是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究。他们利用Cu、Fe、Mg和不同浓度的硫酸溶液(0.5mol/L、2mol/L、18.4mol/L),设计实验方案来研究影响反应速率的因素。
甲同学研究的实验报告如表所示:
(1)甲同学的实验目的是_______ 。
乙同学为了更精确地研究浓度对反应速率的影响,利用如图所示装置进行定量实验。
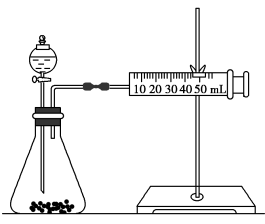
(2)乙同学在实验中应该测定的数据是_______ 。
(3)乙同学完成该实验应选用的实验药品是_______ 。
甲同学研究的实验报告如表所示:
| 实验步骤 | 现象 | 结论 |
| ①分别取等体积2mol/L硫酸溶液于三支试管中 ②向三支试管中分别投入大小、形状相同的Cu、Fe、Mg | 反应速率: ,Cu不反应 ,Cu不反应 | 金属的性质越活泼,反应速率越快 |
乙同学为了更精确地研究浓度对反应速率的影响,利用如图所示装置进行定量实验。

(2)乙同学在实验中应该测定的数据是
(3)乙同学完成该实验应选用的实验药品是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】某化学小组欲测定 与
与 反应的化学反应速率,并探究影响其化学反应速率的因素,请回答下列问题:
反应的化学反应速率,并探究影响其化学反应速率的因素,请回答下列问题:
Ⅰ.该小组同学设计了3组实验,探究影响化学反应速率的部分因素,具体情况如表所示.
(1)表中
__________ ,通过实验1和实验3可探究___________ 对化学反应速率的影响.
(2)写出 与
与 反应的离子方程式:
反应的离子方程式:___________
Ⅱ.该小组同学依据实验1的条件进行反应并测定其化学反应速率,所得数据如图所示. 的化学反应速率
的化学反应速率 为
为_______________ .
分析实验数据发现,反应过程中该反应的化学反应速率先增大后减小,探究化学反应速率先增大的原因,具体情况如表所示.
(4)补全方案1中的实验操作_________________ 。
(5)方案2中的假设为__________________ .
(6)除方案1、2中的假设外,还可提出的假设是____________________ .
(7)反应后期化学反应速率减小的原因是__________________ .
 与
与 反应的化学反应速率,并探究影响其化学反应速率的因素,请回答下列问题:
反应的化学反应速率,并探究影响其化学反应速率的因素,请回答下列问题:Ⅰ.该小组同学设计了3组实验,探究影响化学反应速率的部分因素,具体情况如表所示.
| 实验编号 | 加入 溶液的体积 溶液的体积 | 加入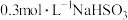 溶液的体积 溶液的体积 | 加入水的体积 | 反应温度 |
| 1 | 10 | 10 | 0 |  |
| 2 | 10 | 5 | a |  |
| 3 | 10 | 10 | 0 |  |
(1)表中

(2)写出
 与
与 反应的离子方程式:
反应的离子方程式:Ⅱ.该小组同学依据实验1的条件进行反应并测定其化学反应速率,所得数据如图所示.

 的化学反应速率
的化学反应速率 为
为分析实验数据发现,反应过程中该反应的化学反应速率先增大后减小,探究化学反应速率先增大的原因,具体情况如表所示.
| 方案 | 假设 | 实验操作 |
| 1 | 该反应放热,使溶液温度升高,化学反应速率加快 | 向烧杯中加入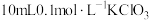 溶液和 溶液和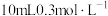 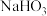 溶液,_________________ 溶液,_________________ |
| 2 | 取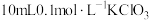 溶液加入烧杯中,向其中加入少量 溶液加入烧杯中,向其中加入少量 固体,再加入 固体,再加入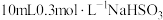 溶液. 溶液. |
(4)补全方案1中的实验操作
(5)方案2中的假设为
(6)除方案1、2中的假设外,还可提出的假设是
(7)反应后期化学反应速率减小的原因是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】H2O2作为氧化剂在反应时不产生污染物被称为绿色氧化剂,因而受到人们越来越多的关注。为比较Fe3+和Cu2+对H2O2(2%和5%两种浓度)分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答下列问题:
(1)定性分析:图甲可通过观察_______ 定性比较得出结论。有同学提出将FeCl3溶液改为Fe2(SO4)3溶液更合理,其理由是_______ 。

(2)定量分析:如图乙所示,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略。图中仪器A的名称为______ ,检查该装置气密性的方法是:关闭A的活塞,将注射器活塞向外拉出一段后松手,过一段时间后看______ ,实验中需要测量的数据是______ 。
(3)加入MnO2粉末于H2O2溶液中,在标准状况下放出气体的体积和时间的关系如丙图所示。由D到A过程中,随着反应的进行反应速率逐渐______ (填“加快”或“减慢”),其变化的原因是______ 。(选填字母编号)

A.改变了反应的活化能
B.改变活化分子百分比
C.改变了反应途径
D.改变单位体积内的分子总数
(4)另一小组同学为了研究浓度对反应速率的影响,设计了如下实验设计方案,请帮助完成(所有空均需填满)。
可得到的结论是浓度越大,H2O2分解速率越快。
(1)定性分析:图甲可通过观察

(2)定量分析:如图乙所示,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略。图中仪器A的名称为
(3)加入MnO2粉末于H2O2溶液中,在标准状况下放出气体的体积和时间的关系如丙图所示。由D到A过程中,随着反应的进行反应速率逐渐

A.改变了反应的活化能
B.改变活化分子百分比
C.改变了反应途径
D.改变单位体积内的分子总数
(4)另一小组同学为了研究浓度对反应速率的影响,设计了如下实验设计方案,请帮助完成(所有空均需填满)。
| 实验编号 | T/K | 催化剂 | 浓度 |
| 实验1 | 298 | 3滴FeCl3溶液 | 10mL2%H2O2 |
| 实验2 | 298 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】某研究性学习小组向一定量的NaHSO3溶液(加入少量淀粉)中加入稍过量的KIO3溶液,一段时间后,溶液突然变蓝色。为进一步研究有关因素对反应速率的影响,探究如下。
(1)查阅资料知NaHSO3与过量KIO3反应分为两步进行,且其反应速率主要由第一步反应决定。已知第一步反应的离子方程式为IO3-+3HSO3-=3SO42-+I-+3H+,则第二步反应的离子方程式为____ 。
(2)通过测定溶液变蓝所用时间来探究外界条件对该反应速率的影响,记录如下。
①实验①②是探究KIO3浓度对反应速率的影响,表中c=_____ mL;
②实验①③是探究温度对反应速率的影响,表中a=____ 。
(3)将NaHSO3溶液与KIO3溶液在恒温条件下混合,用速率检测仪检测出起始阶段反应速率逐渐增大。该小组对其原因提出如下假设,请你完成假设二。
假设一:生成的SO42-对反应起催化作用;
假设二:____ ;
(4)请你设计实验验证上述假设一,完成表中内容。
(1)查阅资料知NaHSO3与过量KIO3反应分为两步进行,且其反应速率主要由第一步反应决定。已知第一步反应的离子方程式为IO3-+3HSO3-=3SO42-+I-+3H+,则第二步反应的离子方程式为
(2)通过测定溶液变蓝所用时间来探究外界条件对该反应速率的影响,记录如下。
| 编号 | 0.01mol/LNaHSO3溶液/mL | 0.01mol/LKIO3溶液/mL | H2O/mL | 反应温度/℃ | 溶液变蓝所用时间t/s |
| ① | 6.0 | 10.0 | 4.0 | 15 | t1 |
| ② | 6.0 | 12.0 | c | 15 | t2 |
| ③ | 6.0 | a | b | 25 | t3 |
②实验①③是探究温度对反应速率的影响,表中a=
(3)将NaHSO3溶液与KIO3溶液在恒温条件下混合,用速率检测仪检测出起始阶段反应速率逐渐增大。该小组对其原因提出如下假设,请你完成假设二。
假设一:生成的SO42-对反应起催化作用;
假设二:
(4)请你设计实验验证上述假设一,完成表中内容。
| 实验步骤(不要求写出具体操作过程) | 预期实验现象和结论 |
| 在烧杯甲中将一定量的NaHSO3溶液与KIO3溶液混合,用速率检测仪测定起始时的反应速率v(甲)在烧杯乙中先加入少量① | ②若v(甲) ③若v(甲) |
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐3】天津地处环渤海湾,海水资源丰富。科研人员把铁的配合物 (L为配体)溶于弱碱性的海水中,制成吸收液,将气体
(L为配体)溶于弱碱性的海水中,制成吸收液,将气体 转化为单质硫,改进了湿法脱硫工艺。该工艺包含两个阶段:①
转化为单质硫,改进了湿法脱硫工艺。该工艺包含两个阶段:① 的吸收氧化;②
的吸收氧化;② 的再生。反应原理如下:
的再生。反应原理如下:
①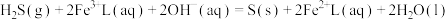
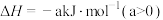
②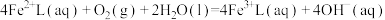
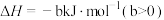
回答下列问题:
(1)该工艺的总反应方程式为___________ 。1mol 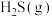 发生该反应的热量变化为
发生该反应的热量变化为___________ , 在总反应中的作用是
在总反应中的作用是___________ 。
(2)研究不同配体与 所形成的配合物(A、B、C)对
所形成的配合物(A、B、C)对 吸收转化率的影响。将配合物A、B、C分别溶于海水中,配成相同物质的量浓度的吸收液,在相同反应条件下,分别向三份吸收液持续通入
吸收转化率的影响。将配合物A、B、C分别溶于海水中,配成相同物质的量浓度的吸收液,在相同反应条件下,分别向三份吸收液持续通入 ,测得单位体积吸收液中
,测得单位体积吸收液中 吸收转化率
吸收转化率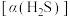 随时间变化的曲线如图1所示。以
随时间变化的曲线如图1所示。以 由100%降至80%所持续的时间来评价铁配合物的脱硫效率,结果最好的是
由100%降至80%所持续的时间来评价铁配合物的脱硫效率,结果最好的是___________ (填“A”、“B”或“C”)。 的电离方程式为
的电离方程式为___________ 。25℃时, 溶液中
溶液中 、
、 、
、 在含硫粒子总浓度中所占分数
在含硫粒子总浓度中所占分数 随溶液pH的变化关系如图2,由图2计算,
随溶液pH的变化关系如图2,由图2计算, 的
的
___________ ,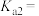
___________ 。再生反应在常温下进行,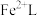 解离出的
解离出的 易与溶液中的
易与溶液中的 形成沉淀。若溶液中的
形成沉淀。若溶液中的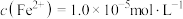 ,
,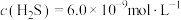 ,为避免有FeS沉淀生成,应控制溶液pH不大于
,为避免有FeS沉淀生成,应控制溶液pH不大于___________ (已知25℃时,FeS的 为
为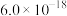 )。
)。
 (L为配体)溶于弱碱性的海水中,制成吸收液,将气体
(L为配体)溶于弱碱性的海水中,制成吸收液,将气体 转化为单质硫,改进了湿法脱硫工艺。该工艺包含两个阶段:①
转化为单质硫,改进了湿法脱硫工艺。该工艺包含两个阶段:① 的吸收氧化;②
的吸收氧化;② 的再生。反应原理如下:
的再生。反应原理如下:①
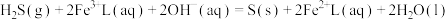
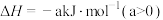
②
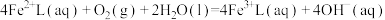
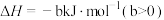
回答下列问题:
(1)该工艺的总反应方程式为
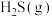 发生该反应的热量变化为
发生该反应的热量变化为 在总反应中的作用是
在总反应中的作用是(2)研究不同配体与
 所形成的配合物(A、B、C)对
所形成的配合物(A、B、C)对 吸收转化率的影响。将配合物A、B、C分别溶于海水中,配成相同物质的量浓度的吸收液,在相同反应条件下,分别向三份吸收液持续通入
吸收转化率的影响。将配合物A、B、C分别溶于海水中,配成相同物质的量浓度的吸收液,在相同反应条件下,分别向三份吸收液持续通入 ,测得单位体积吸收液中
,测得单位体积吸收液中 吸收转化率
吸收转化率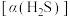 随时间变化的曲线如图1所示。以
随时间变化的曲线如图1所示。以 由100%降至80%所持续的时间来评价铁配合物的脱硫效率,结果最好的是
由100%降至80%所持续的时间来评价铁配合物的脱硫效率,结果最好的是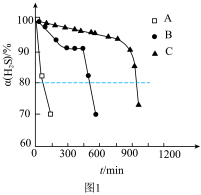
 的电离方程式为
的电离方程式为 溶液中
溶液中 、
、 、
、 在含硫粒子总浓度中所占分数
在含硫粒子总浓度中所占分数 随溶液pH的变化关系如图2,由图2计算,
随溶液pH的变化关系如图2,由图2计算, 的
的
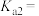
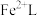 解离出的
解离出的 易与溶液中的
易与溶液中的 形成沉淀。若溶液中的
形成沉淀。若溶液中的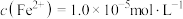 ,
,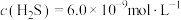 ,为避免有FeS沉淀生成,应控制溶液pH不大于
,为避免有FeS沉淀生成,应控制溶液pH不大于 为
为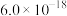 )。
)。
您最近一年使用:0次



