1 . 含氮污染物的有效去除和含碳资源的充分利用是重要研究课题。回答下列问题:
(1)利用尾气 与
与 反应制备新型硝化剂
反应制备新型硝化剂 ,过程见下表,其中
,过程见下表,其中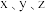 为常数。
为常数。
①反应Ⅱ的活化能
_______  (逆)(填“>”或“<”)。
(逆)(填“>”或“<”)。
② 的数值范围是
的数值范围是_______ 。
(2) 与
与 重整是
重整是 利用的研究热点之一。该重整反应体系有以下反应:
利用的研究热点之一。该重整反应体系有以下反应:
I.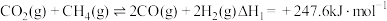
Ⅱ.
Ⅲ. (只在高温下自发进行)
(只在高温下自发进行)
在一定压强和催化剂的条件下,将等物质的的 和
和 通入重整反应器中,平衡时,
通入重整反应器中,平衡时, 的物质的量分数及转化率随温度变化的关系如图所示。平衡时
的物质的量分数及转化率随温度变化的关系如图所示。平衡时 的物质的量分数随温度变化的曲线是
的物质的量分数随温度变化的曲线是_______ (填标号)。温度高于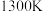 后,曲线d超过曲线c的可能原因为
后,曲线d超过曲线c的可能原因为_______ 。 和
和 转化为
转化为 和
和 是处理尾气的重要方式之一。相关反应如下:
是处理尾气的重要方式之一。相关反应如下:
I:
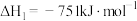
Ⅱ: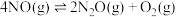
Ⅲ: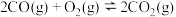
为探究温度对催化剂催化效果的影响,将固定比例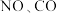 混合气体,以一定流速通过三元催化剂排气管,相同时间内测量尾气中
混合气体,以一定流速通过三元催化剂排气管,相同时间内测量尾气中 的含量,得到脱氮率随温度变化如图所示,已知图中
的含量,得到脱氮率随温度变化如图所示,已知图中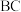 段为平衡状态,且平衡脱氮率为
段为平衡状态,且平衡脱氮率为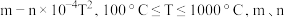 为常数。下列说法正确的是_______。
为常数。下列说法正确的是_______。
(4)一种焦炭催化 还原
还原 反应的历程如下,请补充完整相关基元反应(“*”表示吸附态):
反应的历程如下,请补充完整相关基元反应(“*”表示吸附态):
A.
B.
C._______ 。
D.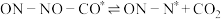
E._______ 。
(1)利用尾气
 与
与 反应制备新型硝化剂
反应制备新型硝化剂 ,过程见下表,其中
,过程见下表,其中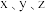 为常数。
为常数。| 过程 | 反应 | 焓变 | 平衡常数K与温度T关系 |
| Ⅰ |  |  |  |
| Ⅱ | 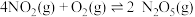 |  | 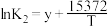 |
| Ⅲ | 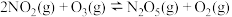 |  | 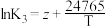 |

 (逆)(填“>”或“<”)。
(逆)(填“>”或“<”)。②
 的数值范围是
的数值范围是(2)
 与
与 重整是
重整是 利用的研究热点之一。该重整反应体系有以下反应:
利用的研究热点之一。该重整反应体系有以下反应:I.
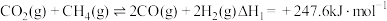
Ⅱ.

Ⅲ.
 (只在高温下自发进行)
(只在高温下自发进行)在一定压强和催化剂的条件下,将等物质的的
 和
和 通入重整反应器中,平衡时,
通入重整反应器中,平衡时, 的物质的量分数及转化率随温度变化的关系如图所示。平衡时
的物质的量分数及转化率随温度变化的关系如图所示。平衡时 的物质的量分数随温度变化的曲线是
的物质的量分数随温度变化的曲线是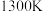 后,曲线d超过曲线c的可能原因为
后,曲线d超过曲线c的可能原因为
 和
和 转化为
转化为 和
和 是处理尾气的重要方式之一。相关反应如下:
是处理尾气的重要方式之一。相关反应如下:I:

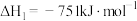
Ⅱ:
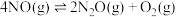
Ⅲ:
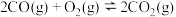
为探究温度对催化剂催化效果的影响,将固定比例
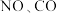 混合气体,以一定流速通过三元催化剂排气管,相同时间内测量尾气中
混合气体,以一定流速通过三元催化剂排气管,相同时间内测量尾气中 的含量,得到脱氮率随温度变化如图所示,已知图中
的含量,得到脱氮率随温度变化如图所示,已知图中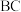 段为平衡状态,且平衡脱氮率为
段为平衡状态,且平衡脱氮率为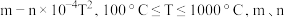 为常数。下列说法正确的是_______。
为常数。下列说法正确的是_______。
A.平衡脱氮率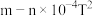 表达式中: 表达式中: |
B. 段因温度下降,催化剂活性降低,故平衡脱氮率下降 段因温度下降,催化剂活性降低,故平衡脱氮率下降 |
C.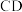 段处于平衡状态,因反应I正向放热,升温平衡逆向移动,故脱氮率降低 段处于平衡状态,因反应I正向放热,升温平衡逆向移动,故脱氮率降低 |
D.D点平衡脱氮率为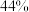 |
(4)一种焦炭催化
 还原
还原 反应的历程如下,请补充完整相关基元反应(“*”表示吸附态):
反应的历程如下,请补充完整相关基元反应(“*”表示吸附态): A.

B.

C.
D.
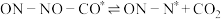
E.
您最近一年使用:0次
2 .  和
和 催化耦合脱氢制备丙烯是实现碳中和的有效途径之一,其微观过程示意如图1。
催化耦合脱氢制备丙烯是实现碳中和的有效途径之一,其微观过程示意如图1。 的量不变,向体积相同的恒容密闭容器中分别通入
的量不变,向体积相同的恒容密闭容器中分别通入 为0:1、1:1、2:1、3:1的
为0:1、1:1、2:1、3:1的 的混合气,测得
的混合气,测得 的平衡转化率随温度的变化曲线如图2。
的平衡转化率随温度的变化曲线如图2。
Ⅰ.
Ⅱ.
Ⅲ.
(1) =
=___________ 。
(2)① =1:1对应图中曲线
=1:1对应图中曲线___________ (填序号)。
②900K下,曲线b、c、d的平衡转化率显著大于a的原理为___________ 。
(3)900K,将 =3:1的混合气通入恒容密闭容器中进行反应。
=3:1的混合气通入恒容密闭容器中进行反应。
①下列说法正确的是___________ (填序号)。
A.通入氩气可提高 的平衡转化率
的平衡转化率
B.体系达到平衡时,若缩小容器容积,反应Ⅱ平衡不移动
C.当 和
和 的比值不变时,体系达到平衡
的比值不变时,体系达到平衡
D.改善催化剂的性能可提高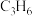 生产效率
生产效率
②若初始压强为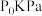 ,t min时达到平衡,此时
,t min时达到平衡,此时 分压是CO的5倍,0~t min内
分压是CO的5倍,0~t min内 =
=___________  ;反应Ⅰ的压强平衡常数
;反应Ⅰ的压强平衡常数 =
=___________ 。
(4)利用反应 可制备高纯Ni。
可制备高纯Ni。
① 晶体中不存在的作用力有
晶体中不存在的作用力有___________ 。
A.离子键 B.π键 C.范德华力 D.极性键 E.金属键
② 中Ni为
中Ni为 杂化,配位原子是
杂化,配位原子是___________ ,判断依据是___________ 。
 和
和 催化耦合脱氢制备丙烯是实现碳中和的有效途径之一,其微观过程示意如图1。
催化耦合脱氢制备丙烯是实现碳中和的有效途径之一,其微观过程示意如图1。
 的量不变,向体积相同的恒容密闭容器中分别通入
的量不变,向体积相同的恒容密闭容器中分别通入 为0:1、1:1、2:1、3:1的
为0:1、1:1、2:1、3:1的 的混合气,测得
的混合气,测得 的平衡转化率随温度的变化曲线如图2。
的平衡转化率随温度的变化曲线如图2。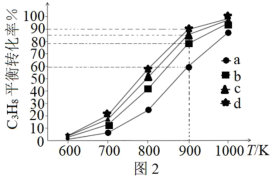
Ⅰ.

Ⅱ.

Ⅲ.

(1)
 =
=(2)①
 =1:1对应图中曲线
=1:1对应图中曲线②900K下,曲线b、c、d的平衡转化率显著大于a的原理为
(3)900K,将
 =3:1的混合气通入恒容密闭容器中进行反应。
=3:1的混合气通入恒容密闭容器中进行反应。①下列说法正确的是
A.通入氩气可提高
 的平衡转化率
的平衡转化率B.体系达到平衡时,若缩小容器容积,反应Ⅱ平衡不移动
C.当
 和
和 的比值不变时,体系达到平衡
的比值不变时,体系达到平衡D.改善催化剂的性能可提高
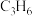 生产效率
生产效率②若初始压强为
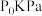 ,t min时达到平衡,此时
,t min时达到平衡,此时 分压是CO的5倍,0~t min内
分压是CO的5倍,0~t min内 =
= ;反应Ⅰ的压强平衡常数
;反应Ⅰ的压强平衡常数 =
=(4)利用反应
 可制备高纯Ni。
可制备高纯Ni。①
 晶体中不存在的作用力有
晶体中不存在的作用力有A.离子键 B.π键 C.范德华力 D.极性键 E.金属键
②
 中Ni为
中Ni为 杂化,配位原子是
杂化,配位原子是
您最近一年使用:0次
解题方法
3 . 含碳化合物的合成与转化具有重要的研究价值。
(1)热力学规定,在标准压强和指定温度下,由元素最稳定的单质生成 化合物时的反应热称为该化合物的标准摩尔生成焓。常温下,
化合物时的反应热称为该化合物的标准摩尔生成焓。常温下, 、
、 的标准摩尔生成焓分别为
的标准摩尔生成焓分别为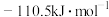 、
、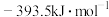 ,则表示
,则表示 标准摩尔生成焓的热化学反应方程式为
标准摩尔生成焓的热化学反应方程式为___________ 。
(2) 与
与 在某催化剂作用下的反应如图所示:
在某催化剂作用下的反应如图所示:
该反应的热化学反应方程式为___________ 。
(3)汽车尾气中的 和
和 在催化转化器中可反应生成两种无毒无害的气体(该反应为放热反应),若该反应在恒温、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到时刻达到平衡状态的是___________(填标号)。
在催化转化器中可反应生成两种无毒无害的气体(该反应为放热反应),若该反应在恒温、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到时刻达到平衡状态的是___________(填标号)。
(4) 与
与 可发生反应:
可发生反应: ,2L密闭容器中通入
,2L密闭容器中通入
 和
和
 ,在不同催化剂(A、B)作用下,进行相同时间后,
,在不同催化剂(A、B)作用下,进行相同时间后, 的产率随反应温度的变化如图所示:
的产率随反应温度的变化如图所示: 、
、 表示,则
表示,则
___________  (填“>”“<”或“=”,下同)。
(填“>”“<”或“=”,下同)。
②y点对应的v(逆)___________ z点对应的v(正)。
③若w点的时间为5min,则 的平均反应速率为
的平均反应速率为___________  。此温度下的化学平衡常数为
。此温度下的化学平衡常数为___________ 。
(1)热力学规定,在标准压强和指定温度下,由元素最稳定的单质生成
 化合物时的反应热称为该化合物的标准摩尔生成焓。常温下,
化合物时的反应热称为该化合物的标准摩尔生成焓。常温下, 、
、 的标准摩尔生成焓分别为
的标准摩尔生成焓分别为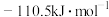 、
、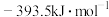 ,则表示
,则表示 标准摩尔生成焓的热化学反应方程式为
标准摩尔生成焓的热化学反应方程式为(2)
 与
与 在某催化剂作用下的反应如图所示:
在某催化剂作用下的反应如图所示: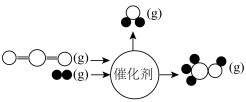
| 化学键 |
|
|
|
|
|
键能/( ) ) | 438 | 326 | 802 | 464 | 414 |
(3)汽车尾气中的
 和
和 在催化转化器中可反应生成两种无毒无害的气体(该反应为放热反应),若该反应在恒温、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到时刻达到平衡状态的是___________(填标号)。
在催化转化器中可反应生成两种无毒无害的气体(该反应为放热反应),若该反应在恒温、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到时刻达到平衡状态的是___________(填标号)。A.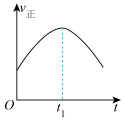 | B.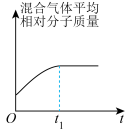 |
C.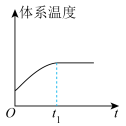 | D.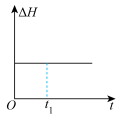 |
 与
与 可发生反应:
可发生反应: ,2L密闭容器中通入
,2L密闭容器中通入
 和
和
 ,在不同催化剂(A、B)作用下,进行相同时间后,
,在不同催化剂(A、B)作用下,进行相同时间后, 的产率随反应温度的变化如图所示:
的产率随反应温度的变化如图所示: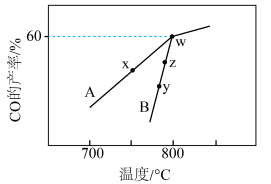
 、
、 表示,则
表示,则
 (填“>”“<”或“=”,下同)。
(填“>”“<”或“=”,下同)。②y点对应的v(逆)
③若w点的时间为5min,则
 的平均反应速率为
的平均反应速率为 。此温度下的化学平衡常数为
。此温度下的化学平衡常数为
您最近一年使用:0次
4 .  、CO、
、CO、 等都是重要的能源,也是重要的化工原料。
等都是重要的能源,也是重要的化工原料。
(1)25℃,101kPa时, 完全燃烧生成二氧化碳气体和液态水放出445.1kJ热量。写出该反应的热化学反应方程式:
完全燃烧生成二氧化碳气体和液态水放出445.1kJ热量。写出该反应的热化学反应方程式:___________ 。
(2)水煤气中的CO和 在高温下反应可生成甲烷。在体积为2L的恒容密闭容器中,充入1molCO和
在高温下反应可生成甲烷。在体积为2L的恒容密闭容器中,充入1molCO和 ,一定温度下发生反应:
,一定温度下发生反应: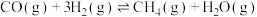 。测得CO和
。测得CO和 的转化率随时间变化如图所示:
的转化率随时间变化如图所示:___________ ,6min时, 的转化率为
的转化率为___________ 。
②下列叙述中能说明上述反应达到化学平衡状态的是___________ (填字母)。
a.容器中混合气体的密度保持不变 b.容器中混合气体的总压强保持不变
c.容器中 d.单位时间内每消耗1molCO,同时生成
d.单位时间内每消耗1molCO,同时生成
e.容器中混合气体的平均相对分子质量保持不变
(3)甲烷燃料电池装置如图,通入氧气的电极为电池的___________ (填“正极”或“负极”)。通入 一端电极反应方程式为:
一端电极反应方程式为:___________ 。
 、CO、
、CO、 等都是重要的能源,也是重要的化工原料。
等都是重要的能源,也是重要的化工原料。(1)25℃,101kPa时,
 完全燃烧生成二氧化碳气体和液态水放出445.1kJ热量。写出该反应的热化学反应方程式:
完全燃烧生成二氧化碳气体和液态水放出445.1kJ热量。写出该反应的热化学反应方程式:(2)水煤气中的CO和
 在高温下反应可生成甲烷。在体积为2L的恒容密闭容器中,充入1molCO和
在高温下反应可生成甲烷。在体积为2L的恒容密闭容器中,充入1molCO和 ,一定温度下发生反应:
,一定温度下发生反应: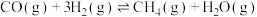 。测得CO和
。测得CO和 的转化率随时间变化如图所示:
的转化率随时间变化如图所示:
 的转化率为
的转化率为②下列叙述中能说明上述反应达到化学平衡状态的是
a.容器中混合气体的密度保持不变 b.容器中混合气体的总压强保持不变
c.容器中
 d.单位时间内每消耗1molCO,同时生成
d.单位时间内每消耗1molCO,同时生成
e.容器中混合气体的平均相对分子质量保持不变
(3)甲烷燃料电池装置如图,通入氧气的电极为电池的
 一端电极反应方程式为:
一端电极反应方程式为: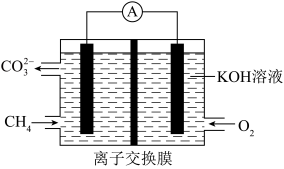
您最近一年使用:0次
名校
5 . 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:___________ ,Y的转化率为___________ 。
(2)该反应的化学方程式为___________ 。
(3)下列能表示该反应达平衡状态的是___________(填选项字母)。
(4)10s后保持其他条件不变,判断改变下列条件后反应速率的变化情况:
A.继续通入一定量的X:___________ (填“增大”、“减小”或“不变”,下同)。
B.继续通入一定量的He:___________ 。
(5)下列图像或实验属于放热反应的是___________ (填序号)。___________ (填物质名称),负极的电极反应式为___________ 。

(2)该反应的化学方程式为
(3)下列能表示该反应达平衡状态的是___________(填选项字母)。
| A.容器内气体质量不再发生变化 |
| B.容器内气体压强不再发生变化 |
| C.X的体积分数不再改变 |
| D.容器内混合气体的密度不再发生变化 |
(4)10s后保持其他条件不变,判断改变下列条件后反应速率的变化情况:
A.继续通入一定量的X:
B.继续通入一定量的He:
(5)下列图像或实验属于放热反应的是

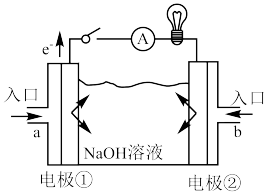
您最近一年使用:0次
6 . 杭州亚运会主火炬燃料是“零碳甲醇”,是一种利用焦炉气中的H2和工业废气捕获的CO2生产的绿色燃料,在适宜的过渡金属及其氧化物催化下发生反应:
(1)已知:Ⅰ.

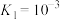
Ⅱ.

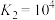
Ⅲ.


则
_________  ,
,
_________ (计算其数值)。
(2)甲醇气相脱水制甲醚(CH3OCH3)的反应可表示为: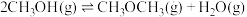
 。
。
①一定温度下,在恒容密闭容器中充入一定量的 发生上述反应,能判断反应达到化学平衡状态的是
发生上述反应,能判断反应达到化学平衡状态的是________
A.CH3OH(g)和CH3OCH3(g)的浓度比保持不变
B.
C.容器内压强不再变化
D.混合气体的平均相对分子质量不再变化
②200℃时向2 L恒容密闭容器中充入2 mol CH3OH(g)发生上述反应,测得CH3OH(g)的浓度随时间(t)的变化如下表:
达平衡时该反应放出的热量为________ kJ,若此时平衡压强为P0,则该温度条件下,压强平衡常数Kp=________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③200℃时,向该容器中投入三种成分的浓度如下:
此时,正、逆反应速率的大小关系为:
________ 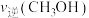 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
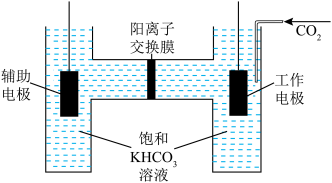
(3)我国科研团队在CO2电化学还原反应机理的研究上取得新突破,CO2电化学还原法中采用TiO2纳米管作电解池工作电极,惰性电极作辅助电极,以一定流速通入CO2,测得CO2生成CO的产率接近80%。
①工作电极上主要发生的电极反应为_____________ ;
②电解一段时间,交换膜左侧溶液的浓度_________ (填“增大”、“减小”或“不变”)。
(1)已知:Ⅰ.


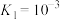
Ⅱ.



Ⅲ.



则

 ,
,
(2)甲醇气相脱水制甲醚(CH3OCH3)的反应可表示为:
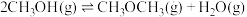
 。
。①一定温度下,在恒容密闭容器中充入一定量的
 发生上述反应,能判断反应达到化学平衡状态的是
发生上述反应,能判断反应达到化学平衡状态的是A.CH3OH(g)和CH3OCH3(g)的浓度比保持不变
B.

C.容器内压强不再变化
D.混合气体的平均相对分子质量不再变化
②200℃时向2 L恒容密闭容器中充入2 mol CH3OH(g)发生上述反应,测得CH3OH(g)的浓度随时间(t)的变化如下表:
t/min | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
c(CH3OH)/(mol·L-1) | 1.00 | 0.65 | 0.50 | 0.36 | 0.27 | 0.20 | 0.20 |
③200℃时,向该容器中投入三种成分的浓度如下:
物质 | CH3OH(g) | CH3OCH3(g) | H2O(g) |
c/(mol·L-1) | 0.64 | 0.68 | 0.68 |

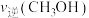 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(3)我国科研团队在CO2电化学还原反应机理的研究上取得新突破,CO2电化学还原法中采用TiO2纳米管作电解池工作电极,惰性电极作辅助电极,以一定流速通入CO2,测得CO2生成CO的产率接近80%。
①工作电极上主要发生的电极反应为
②电解一段时间,交换膜左侧溶液的浓度
您最近一年使用:0次
名校
7 . 工业上制备硫酸的反应之一为2SO2(g)+O2(g) 2SO3(g)。一定条件下,该反应在密闭容器中进行,下列说法错误的是
2SO3(g)。一定条件下,该反应在密闭容器中进行,下列说法错误的是
 2SO3(g)。一定条件下,该反应在密闭容器中进行,下列说法错误的是
2SO3(g)。一定条件下,该反应在密闭容器中进行,下列说法错误的是| A.使用合适的催化剂可以提高反应速率 |
| B.反应达到平衡后,SO2的物质的量不再变化 |
| C.反应达到平衡后,SO2和SO3的浓度一定相等 |
| D.反应达到平衡后,改变反应条件,不能改变平衡状态 |
您最近一年使用:0次
名校
8 . 由下列实验操作及现象推出的结论正确的是
选项 | 操作 | 现象 | 结论 |
A | 石蜡油加强热,将产生的气体通入 的 的 溶液 溶液 | 溶液由红棕色变为无色 | 气体中含有不饱和烃 |
B | 常温下将铁片分别插入稀硫酸和浓硫酸中 | 前者产生无色气体,后者无明显现象 | 稀硫酸的氧化性比浓硫酸强 |
C | 将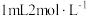 的 的 溶液与 溶液与  溶液混合充分反应后滴加 溶液混合充分反应后滴加 溶液 溶液 | 溶液颜色变红 |  与 与 的反应存在限度 的反应存在限度 |
D | 分别用 计测等物质的量浓度的 计测等物质的量浓度的 和 和 溶液的 溶液的 |  溶液 溶液 更大 更大 | 非金属性S>C |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 .  为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A. 中采取 中采取 杂化的原子数为 杂化的原子数为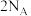 |
B.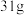 白磷所含孤电子对数为 白磷所含孤电子对数为 |
C.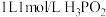 (一元弱酸)溶液中, (一元弱酸)溶液中, 与 与 的个数之和为 的个数之和为 |
D.标准状况下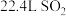 与 与 充分反应生成的 充分反应生成的 分子数为 分子数为 |
您最近一年使用:0次
10 . 减少氮氧化物的排放对保护环境有重要意义,因而研究氮及其化合物的转化成为重要课题。回答下列问题:
(1)已知:①

②

③

常温下 还原NO的热化学方程式为
还原NO的热化学方程式为________ 。
(2)降低汽车尾气中NO和CO含量的反应为 ,在容积为2L的恒容密闭容器中按照不同的投料比(m)进行反应,测得CO的平衡转化率与温度、投料比(m)的关系如图所示。
,在容积为2L的恒容密闭容器中按照不同的投料比(m)进行反应,测得CO的平衡转化率与温度、投料比(m)的关系如图所示。________ (填“吸热”或“放热”)反应,其熵变
________ (填“>”“<”或“=”)0。
② 下,下列叙述能说明反应已达到平衡状态的是
下,下列叙述能说明反应已达到平衡状态的是________ (填字母)。
A.容器内气体的密度保持不变 B.
C.容器内气体的压强不再变化 D.容器内 的体积分数保持不变
的体积分数保持不变
③随着温度的升高,不同投料比中CO的平衡转化率趋近,原因是________ 。
(3)科学家研究用活性炭对汽车尾气中的NO进行吸附,发生的反应为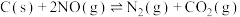
 。该反应的标准平衡常数
。该反应的标准平衡常数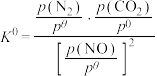 [
[ 为标准压强,
为标准压强,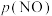 、
、 为各组分的平衡分压(分压=总压
为各组分的平衡分压(分压=总压 物质的量分数)]。温度为TK时,压强为
物质的量分数)]。温度为TK时,压强为 ,恒容密闭容器中加入足量活性炭和1molNO,tmin后达到平衡时,NO的转化率为a,则NO的平均反应速率
,恒容密闭容器中加入足量活性炭和1molNO,tmin后达到平衡时,NO的转化率为a,则NO的平均反应速率
________ 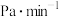 (用含
(用含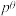 、t、a的代数式表示),
、t、a的代数式表示),
________ (用含a的代数式表示)。
(4)氨气中氢的含量高,是一种优良的小分子储氢载体。利用太阳能电池电解 得到高纯
得到高纯 ,装置如图所示。电解过程中
,装置如图所示。电解过程中 应向
应向________ (填“a极”或“b极”)区迁移,a极的电极反应为________ 。
(1)已知:①


②


③


常温下
 还原NO的热化学方程式为
还原NO的热化学方程式为(2)降低汽车尾气中NO和CO含量的反应为
 ,在容积为2L的恒容密闭容器中按照不同的投料比(m)进行反应,测得CO的平衡转化率与温度、投料比(m)的关系如图所示。
,在容积为2L的恒容密闭容器中按照不同的投料比(m)进行反应,测得CO的平衡转化率与温度、投料比(m)的关系如图所示。

②
 下,下列叙述能说明反应已达到平衡状态的是
下,下列叙述能说明反应已达到平衡状态的是A.容器内气体的密度保持不变 B.

C.容器内气体的压强不再变化 D.容器内
 的体积分数保持不变
的体积分数保持不变③随着温度的升高,不同投料比中CO的平衡转化率趋近,原因是
(3)科学家研究用活性炭对汽车尾气中的NO进行吸附,发生的反应为
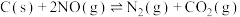
 。该反应的标准平衡常数
。该反应的标准平衡常数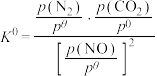 [
[ 为标准压强,
为标准压强,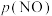 、
、 为各组分的平衡分压(分压=总压
为各组分的平衡分压(分压=总压 物质的量分数)]。温度为TK时,压强为
物质的量分数)]。温度为TK时,压强为 ,恒容密闭容器中加入足量活性炭和1molNO,tmin后达到平衡时,NO的转化率为a,则NO的平均反应速率
,恒容密闭容器中加入足量活性炭和1molNO,tmin后达到平衡时,NO的转化率为a,则NO的平均反应速率
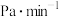 (用含
(用含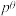 、t、a的代数式表示),
、t、a的代数式表示),
(4)氨气中氢的含量高,是一种优良的小分子储氢载体。利用太阳能电池电解
 得到高纯
得到高纯 ,装置如图所示。电解过程中
,装置如图所示。电解过程中 应向
应向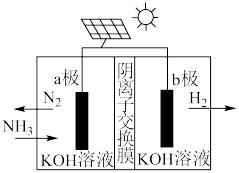
您最近一年使用:0次