名校
1 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.18ng  中含有的分子数为 中含有的分子数为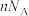 |
B.1mol  的结晶水合物中含有的H-O键数一定为 的结晶水合物中含有的H-O键数一定为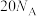 |
C.标准状况下,11.2L由HCl和 组成的混合气体中含有的质子数是 组成的混合气体中含有的质子数是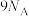 |
D.1mol  与1mol 与1mol  充分反应转移的电子数为 充分反应转移的电子数为 |
您最近一年使用:0次
2024-05-26更新
|
138次组卷
|
2卷引用:2024届重庆市渝西中学高三下学期模拟预测化学试题
名校
2 . T℃时,向体积不等的恒容密闭容器中加入足量活性炭和1mol ,发生反应
,发生反应 。反应相同时间,测得各容器中
。反应相同时间,测得各容器中 的转化率与容器体积的关系如图所示,下列说法正确的是
的转化率与容器体积的关系如图所示,下列说法正确的是
 ,发生反应
,发生反应 。反应相同时间,测得各容器中
。反应相同时间,测得各容器中 的转化率与容器体积的关系如图所示,下列说法正确的是
的转化率与容器体积的关系如图所示,下列说法正确的是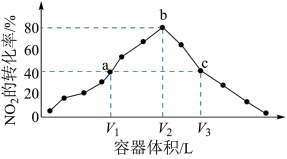
| A.a点对应容器中,反应未达到平衡状态 |
B.向b点对应容器中再充入一定量 ,达到新平衡时, ,达到新平衡时, 的转化率增大 的转化率增大 |
| C.缩小c点对应容器的体积增大压强,v(正)<v(逆) |
D.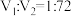 |
您最近一年使用:0次
名校
3 . 由下列实验操作及现象推出的结论正确的是
选项 | 操作 | 现象 | 结论 |
A | 石蜡油加强热,将产生的气体通入 的 的 溶液 溶液 | 溶液由红棕色变为无色 | 气体中含有不饱和烃 |
B | 常温下将铁片分别插入稀硫酸和浓硫酸中 | 前者产生无色气体,后者无明显现象 | 稀硫酸的氧化性比浓硫酸强 |
C | 将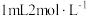 的 的 溶液与 溶液与  溶液混合充分反应后滴加 溶液混合充分反应后滴加 溶液 溶液 | 溶液颜色变红 |  与 与 的反应存在限度 的反应存在限度 |
D | 分别用 计测等物质的量浓度的 计测等物质的量浓度的 和 和 溶液的 溶液的 |  溶液 溶液 更大 更大 | 非金属性S>C |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
4 .  为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A. 中采取 中采取 杂化的原子数为 杂化的原子数为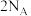 |
B.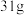 白磷所含孤电子对数为 白磷所含孤电子对数为 |
C.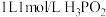 (一元弱酸)溶液中, (一元弱酸)溶液中, 与 与 的个数之和为 的个数之和为 |
D.标准状况下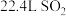 与 与 充分反应生成的 充分反应生成的 分子数为 分子数为 |
您最近一年使用:0次
5 . 下列实验操作、现象能得出相应结论的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向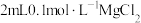 溶液中滴加2滴 溶液中滴加2滴 溶液,再滴加4滴 溶液,再滴加4滴 溶液 溶液 | 先出现白色沉淀,后出现红褐色沉淀 | 在相同温度下,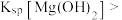  |
| B | 将等浓度的 溶液与 溶液与 溶液混合,充分反应后滴入 溶液混合,充分反应后滴入 溶液 溶液 | 溶液变红 |  与 与 的反应是可逆的 的反应是可逆的 |
| C | 向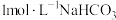 溶液中滴加少量盐酸,将产生的气体通入 溶液中滴加少量盐酸,将产生的气体通入 溶液中 溶液中 |  溶液中有沉淀生成 溶液中有沉淀生成 | 非金属性: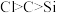 |
| D | 向某钠盐溶液中滴加浓盐酸 | 产生的气体能使品红溶液褪色 | 该钠盐为 或 或 或二者的混合物 或二者的混合物 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
6 . 一氧化碳和氮的氧化物都是大气污染物,如何有效处理它们是科学家长期研究的课题.
(1)CO还原 的反应为:
的反应为:
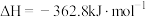 .
.
①研究者发现在气相中 催化CO与
催化CO与 反应的历程有两步:
反应的历程有两步:
第一步:
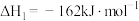
则第二步的热化学方程式为________________ ;
②在恒温恒容密闭容器中,反应一段时间后,以下能说明反应达到平衡状态的是________ (填字母);
A. B.混合气体的密度保持不变
B.混合气体的密度保持不变
C. 的体积分数保持不变 D.容器的压强保持不变
的体积分数保持不变 D.容器的压强保持不变
(2)在密闭容器中发生反应: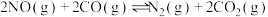
 .一段时间后达到平衡;
.一段时间后达到平衡;
①恒温恒压下,再向该容器中注入氩气,NO的平衡转化率煘小,其原因是________ ;
②一定温度下,在 恒容密闭容器中,加入
恒容密闭容器中,加入 和
和 各
各 ,反应过程中部分物质的体积分数(
,反应过程中部分物质的体积分数( )随时间(t)的变化如图1所示.曲线b代表的是
)随时间(t)的变化如图1所示.曲线b代表的是________ (填化学式)体积分数随时间的变化: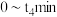 内,用
内,用 表示的平均反应速率为
表示的平均反应速率为________  ;该温度下的平衡常数为
;该温度下的平衡常数为________  ;
;
①a电极的电极反应式为________________ ;
②电池工作一段时间,反应消耗了标准状况下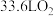 ,理论上负极区溶液增加的质量为
,理论上负极区溶液增加的质量为________ g。
(1)CO还原
 的反应为:
的反应为:
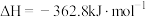 .
.①研究者发现在气相中
 催化CO与
催化CO与 反应的历程有两步:
反应的历程有两步:第一步:

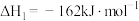
则第二步的热化学方程式为
②在恒温恒容密闭容器中,反应一段时间后,以下能说明反应达到平衡状态的是
A.
 B.混合气体的密度保持不变
B.混合气体的密度保持不变C.
 的体积分数保持不变 D.容器的压强保持不变
的体积分数保持不变 D.容器的压强保持不变(2)在密闭容器中发生反应:
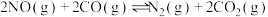
 .一段时间后达到平衡;
.一段时间后达到平衡;①恒温恒压下,再向该容器中注入氩气,NO的平衡转化率煘小,其原因是
②一定温度下,在
 恒容密闭容器中,加入
恒容密闭容器中,加入 和
和 各
各 ,反应过程中部分物质的体积分数(
,反应过程中部分物质的体积分数( )随时间(t)的变化如图1所示.曲线b代表的是
)随时间(t)的变化如图1所示.曲线b代表的是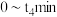 内,用
内,用 表示的平均反应速率为
表示的平均反应速率为 ;该温度下的平衡常数为
;该温度下的平衡常数为 ;
; 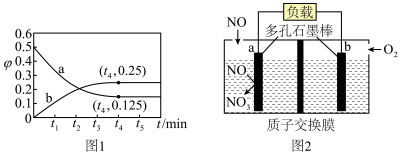
①a电极的电极反应式为
②电池工作一段时间,反应消耗了标准状况下
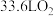 ,理论上负极区溶液增加的质量为
,理论上负极区溶液增加的质量为
您最近一年使用:0次
名校
7 . 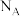 为阿伏伽德罗常数的值,下列说法正确的是
为阿伏伽德罗常数的值,下列说法正确的是
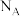 为阿伏伽德罗常数的值,下列说法正确的是
为阿伏伽德罗常数的值,下列说法正确的是A.16.25g 水解形成的 水解形成的 胶体粒子数为 胶体粒子数为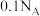 |
B.标准状况下,2.24L 与1.12L 与1.12L 充分反应,生成的 充分反应,生成的 分子数目为 分子数目为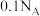 |
C.18g冰中氢键的数目与12g金刚石中C—C键的数目相同,均为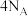 |
D.120g 和 和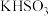 的固体混合物中含有的阳离子数为 的固体混合物中含有的阳离子数为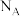 |
您最近一年使用:0次
8 . 回收、处理NO2是环境科学研究的重要课题,常用的处理方式有多孔材料吸附法和CH4还原法等。
(1)利用金属有机骨架多孔材料可将N2O4“固定”,能高效吸附NO2,经处理可得到HNO3,其原理如图所示。___________ (填序号)也能说明吸附反应已达到极限。
A.废气颜色不再发生变化
B.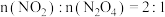
C.
D.混合气体的平均分子质量不再发生变化
②升温不利于NO2的吸附,原因是___________ 。
(2)CH4也可以用来除去NO2。一定条件下,CH4可与NO2反应生成无污染的气态物质与液态水。
已知:反应1: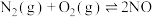

反应2:2NO(g)+O2(g) 2NO2(g) ∆H2=-115kJ/mol
2NO2(g) ∆H2=-115kJ/mol
①已知CH4的燃烧热为890.3kJ/mol,则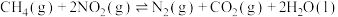 ∆H=
∆H=___________ kJ/mol。
②向恒容密闭容器中充入气体 发生反应
发生反应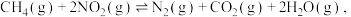 初始压强为192kPa,测得
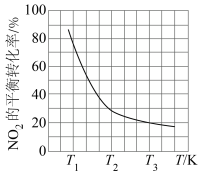
初始压强为192kPa,测得 的平衡转化率与温度(T)的关系如图所示。温度为
的平衡转化率与温度(T)的关系如图所示。温度为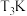 时,反应从开始到达平衡所用的时间为10min,则该段时间内的平均反应速率
时,反应从开始到达平衡所用的时间为10min,则该段时间内的平均反应速率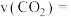
___________ 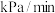 。该温度下,用平衡分压代替浓度计算的平衡常数,
。该温度下,用平衡分压代替浓度计算的平衡常数,
___________ 
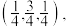 测定该原子坐标的方法为
测定该原子坐标的方法为___________ 。
②C、N原子的配位数之比为___________ 。
(4)下图是CH4燃料电池电解制备 的示意图,同时可以得到H2、Cl2、NaOH。
的示意图,同时可以得到H2、Cl2、NaOH。___________ 。
②理论上,相同时间内NaOH的产量是 的2倍,原因是
的2倍,原因是___________ 。
(1)利用金属有机骨架多孔材料可将N2O4“固定”,能高效吸附NO2,经处理可得到HNO3,其原理如图所示。

A.废气颜色不再发生变化
B.
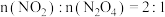
C.

D.混合气体的平均分子质量不再发生变化
②升温不利于NO2的吸附,原因是
(2)CH4也可以用来除去NO2。一定条件下,CH4可与NO2反应生成无污染的气态物质与液态水。
已知:反应1:
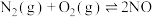

反应2:2NO(g)+O2(g)
 2NO2(g) ∆H2=-115kJ/mol
2NO2(g) ∆H2=-115kJ/mol①已知CH4的燃烧热为890.3kJ/mol,则
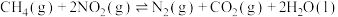 ∆H=
∆H=②向恒容密闭容器中充入气体
 发生反应
发生反应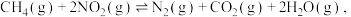 初始压强为192kPa,测得
初始压强为192kPa,测得 的平衡转化率与温度(T)的关系如图所示。温度为
的平衡转化率与温度(T)的关系如图所示。温度为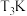 时,反应从开始到达平衡所用的时间为10min,则该段时间内的平均反应速率
时,反应从开始到达平衡所用的时间为10min,则该段时间内的平均反应速率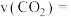
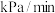 。该温度下,用平衡分压代替浓度计算的平衡常数,
。该温度下,用平衡分压代替浓度计算的平衡常数,

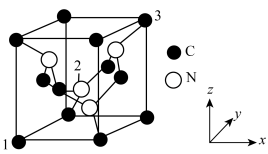
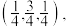 测定该原子坐标的方法为
测定该原子坐标的方法为②C、N原子的配位数之比为
(4)下图是CH4燃料电池电解制备
 的示意图,同时可以得到H2、Cl2、NaOH。
的示意图,同时可以得到H2、Cl2、NaOH。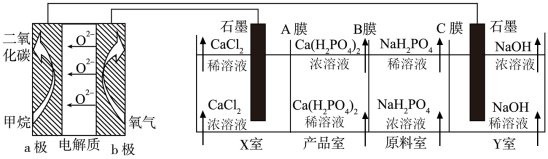
②理论上,相同时间内NaOH的产量是
 的2倍,原因是
的2倍,原因是
您最近一年使用:0次
名校
9 . 一定温度下,向四个不同的恒容密闭容器中分别通入3molNOCl(g),发生反应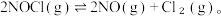 tmin时,NOCl的转化率与容器体积的关系如图所示。下列叙述正确的是
tmin时,NOCl的转化率与容器体积的关系如图所示。下列叙述正确的是
 tmin时,NOCl的转化率与容器体积的关系如图所示。下列叙述正确的是
tmin时,NOCl的转化率与容器体积的关系如图所示。下列叙述正确的是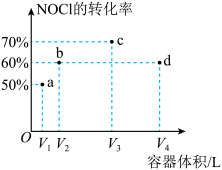
| A.图中只有c、d两点处于平衡状态 |
| B.b、d两点的压强相等 |
| C.tmin时a点v逆大于c点v正 |
| D.平衡常数:Ka<Kb<Kc<Kd |
您最近一年使用:0次
2024-04-28更新
|
301次组卷
|
2卷引用:重庆市康德2024年普通高中学业水平选择性考试高三下学期高考模拟调研卷(三)化学试题
10 . 向绝热恒容密闭容器中通入一定量SO2与NO2的混合气体,在一定条件下发生反应:SO2(g)+NO2(g) SO3(g)+NO(g)。其正反应速率
SO3(g)+NO(g)。其正反应速率 正随时间t变化的曲线如下,不考虑副反应的影响,下列说法正确的是
正随时间t变化的曲线如下,不考虑副反应的影响,下列说法正确的是
 SO3(g)+NO(g)。其正反应速率
SO3(g)+NO(g)。其正反应速率 正随时间t变化的曲线如下,不考虑副反应的影响,下列说法正确的是
正随时间t变化的曲线如下,不考虑副反应的影响,下列说法正确的是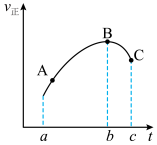
A. 逆随t变化的曲线在a~c时间段内与 逆随t变化的曲线在a~c时间段内与 正的趋势相同 正的趋势相同 |
| B.从A点到C点,NO的分压一直增大 |
| C.其他条件不变时,若在恒温条件下发生此反应,则SO2的平衡转化率减小 |
| D.A、B、C三点的Q值:QA>QB>Qc |
您最近一年使用:0次



