解题方法
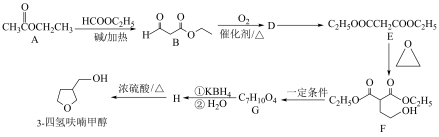
1 . 3-四氢呋喃甲醇是合成农药呋虫胺的中间体,其一种合成路线如下: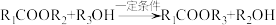
ⅱ.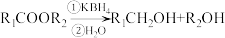
(1)B分子所含官能团的名称为___________ 。D→E反应所需试剂及条件为___________ 。
(2)H的结构简式为___________ 。
(3)由F生成G的过程中常伴有副反应发生,在一定条件下生成高分子聚合物的化学方程式为___________ 。
(4)3-四氢呋喃甲醇的同分异构体中,能发生水解反应有___________ 种(不含立体异构),其中核磁共振氢谱有两组峰的是___________ (写结构简式)。
(5)已知 具有极强还原性,除了还原酯基外(信息ⅱ),还可以还原醛基。请以
具有极强还原性,除了还原酯基外(信息ⅱ),还可以还原醛基。请以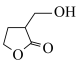 为原料,结合题中信息及所学知识,选用必要的无机试剂合成
为原料,结合题中信息及所学知识,选用必要的无机试剂合成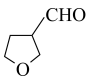 。设计的合成路线为
。设计的合成路线为___________ 。
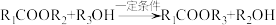
ⅱ.
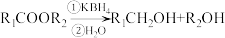
(1)B分子所含官能团的名称为
(2)H的结构简式为
(3)由F生成G的过程中常伴有副反应发生,在一定条件下生成高分子聚合物的化学方程式为
(4)3-四氢呋喃甲醇的同分异构体中,能发生水解反应有
(5)已知
 具有极强还原性,除了还原酯基外(信息ⅱ),还可以还原醛基。请以
具有极强还原性,除了还原酯基外(信息ⅱ),还可以还原醛基。请以 为原料,结合题中信息及所学知识,选用必要的无机试剂合成
为原料,结合题中信息及所学知识,选用必要的无机试剂合成 。设计的合成路线为
。设计的合成路线为
您最近一年使用:0次
2 . 镍、钴及其化合物在工业上有广泛的应用。以含镍废料(主要成分为NiO,含少量FeO、 、CoO、BaO和
、CoO、BaO和 )为原料制备
)为原料制备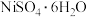 和
和 的工艺流程如下。
的工艺流程如下。
(1)基态Co原子的价层电子的轨道表示式为___________ 。
(2)“滤渣Ⅰ”主要成分是___________ (填化学式)。
(3)“调pH”过程中生成黄钠铁钒沉淀,该反应的离子方程式为___________ 。
(4)“萃取”时需充分振荡,目的是___________ 。“萃取”和“反萃取”可简单表示为: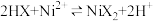 。在萃取过程中加入适量氨水,其作用是
。在萃取过程中加入适量氨水,其作用是___________ 。“反萃取”需要往有机层中加___________ (填试剂名称)。
(5)常温下,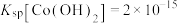 ,若起始时
,若起始时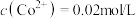 ,“沉钴”过程中应控制pH<
,“沉钴”过程中应控制pH<___________ 。
(6) 在空气中能受热分解,测得剩余固体的质量与起始
在空气中能受热分解,测得剩余固体的质量与起始 的质量的比值(剩余固体的质量分数)随温度变化曲线如图所示。
的质量的比值(剩余固体的质量分数)随温度变化曲线如图所示。 固体置于热解装置中,通入空气流,在
固体置于热解装置中,通入空气流,在___________ ℃(填范围)煅烧至恒重即可得到 。由
。由 制备
制备 总的反应方程式为
总的反应方程式为___________ 。
 、CoO、BaO和
、CoO、BaO和 )为原料制备
)为原料制备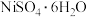 和
和 的工艺流程如下。
的工艺流程如下。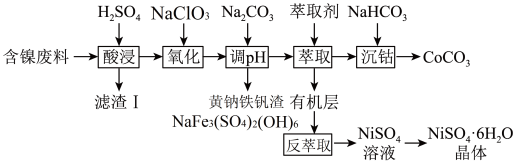
(1)基态Co原子的价层电子的轨道表示式为
(2)“滤渣Ⅰ”主要成分是
(3)“调pH”过程中生成黄钠铁钒沉淀,该反应的离子方程式为
(4)“萃取”时需充分振荡,目的是
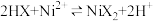 。在萃取过程中加入适量氨水,其作用是
。在萃取过程中加入适量氨水,其作用是(5)常温下,
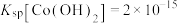 ,若起始时
,若起始时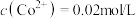 ,“沉钴”过程中应控制pH<
,“沉钴”过程中应控制pH<(6)
 在空气中能受热分解,测得剩余固体的质量与起始
在空气中能受热分解,测得剩余固体的质量与起始 的质量的比值(剩余固体的质量分数)随温度变化曲线如图所示。
的质量的比值(剩余固体的质量分数)随温度变化曲线如图所示。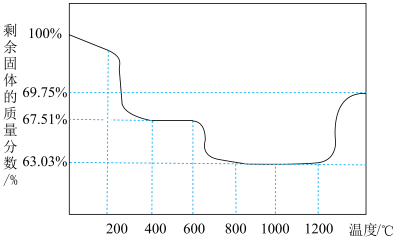
 固体置于热解装置中,通入空气流,在
固体置于热解装置中,通入空气流,在 。由
。由 制备
制备 总的反应方程式为
总的反应方程式为
您最近一年使用:0次
名校
3 . 三水合硝酸铜[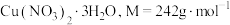 ]是一种重要的无机试剂,常用作搪瓷着色剂,也用于镀铜、制氧化铜及农药等。回答下列问题:
]是一种重要的无机试剂,常用作搪瓷着色剂,也用于镀铜、制氧化铜及农药等。回答下列问题:
Ⅰ.三水合硝酸铜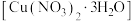 的制备。
的制备。
实验室常用废铜屑与稀硝酸反应制备硝酸铜溶液,过滤出剩余铜屑,再经蒸发浓缩、冷却结晶、过滤、乙醇洗涤后得到三水合硝酸铜晶体。
(1)制备硝酸铜时发生反应的离子方程式为___________ 。
(2)若废铜屑中含有杂质铁,则检验所得硝酸铜溶液中含有铁元素的最佳试剂为___________ (填化学式)。
Ⅱ. 溶液的配制。
溶液的配制。
(3)实验室里需要450mL0.1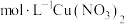 溶液。用三水合硝酸铜
溶液。用三水合硝酸铜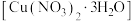 配制该溶液时,下列仪器不需要的是
配制该溶液时,下列仪器不需要的是___________ (填仪器名称)。___________ g。
Ⅲ.测定产品中 的含量
的含量
(5)准备称量ag产品,溶于水后加入过量KI溶液(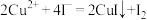 ):充分反应后,以淀粉溶液为指示剂,用c
):充分反应后,以淀粉溶液为指示剂,用c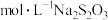 标准溶液滴定(
标准溶液滴定(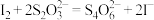 ),达到滴定终点时消耗标准液的体积为VmL。
),达到滴定终点时消耗标准液的体积为VmL。
①达到滴定终点的现象为___________ 。
②产品中 的质量分数为
的质量分数为___________ (用含a、c、V的代数式表示)。
③若所用KI溶液中部分KI被空气氧化,会导致所测结果___________ (填“偏高”“偏低”或“无影响”)。
Ⅳ.三水合硝酸铜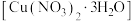 热分解实验。
热分解实验。
(6)将24.2g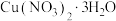 样品置于瓷坩埚中缓慢加热,其热重曲线(样品质量随温度变化的曲线)如图所示,则升温至
样品置于瓷坩埚中缓慢加热,其热重曲线(样品质量随温度变化的曲线)如图所示,则升温至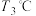 时生成的固体产物为
时生成的固体产物为___________ (填化学式)。
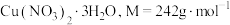 ]是一种重要的无机试剂,常用作搪瓷着色剂,也用于镀铜、制氧化铜及农药等。回答下列问题:
]是一种重要的无机试剂,常用作搪瓷着色剂,也用于镀铜、制氧化铜及农药等。回答下列问题:Ⅰ.三水合硝酸铜
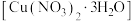 的制备。
的制备。实验室常用废铜屑与稀硝酸反应制备硝酸铜溶液,过滤出剩余铜屑,再经蒸发浓缩、冷却结晶、过滤、乙醇洗涤后得到三水合硝酸铜晶体。
(1)制备硝酸铜时发生反应的离子方程式为
(2)若废铜屑中含有杂质铁,则检验所得硝酸铜溶液中含有铁元素的最佳试剂为
Ⅱ.
 溶液的配制。
溶液的配制。(3)实验室里需要450mL0.1
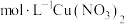 溶液。用三水合硝酸铜
溶液。用三水合硝酸铜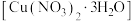 配制该溶液时,下列仪器不需要的是
配制该溶液时,下列仪器不需要的是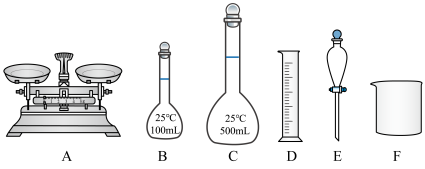
Ⅲ.测定产品中
 的含量
的含量(5)准备称量ag产品,溶于水后加入过量KI溶液(
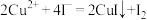 ):充分反应后,以淀粉溶液为指示剂,用c
):充分反应后,以淀粉溶液为指示剂,用c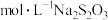 标准溶液滴定(
标准溶液滴定(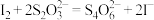 ),达到滴定终点时消耗标准液的体积为VmL。
),达到滴定终点时消耗标准液的体积为VmL。①达到滴定终点的现象为
②产品中
 的质量分数为
的质量分数为③若所用KI溶液中部分KI被空气氧化,会导致所测结果
Ⅳ.三水合硝酸铜
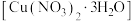 热分解实验。
热分解实验。(6)将24.2g
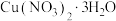 样品置于瓷坩埚中缓慢加热,其热重曲线(样品质量随温度变化的曲线)如图所示,则升温至
样品置于瓷坩埚中缓慢加热,其热重曲线(样品质量随温度变化的曲线)如图所示,则升温至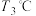 时生成的固体产物为
时生成的固体产物为
您最近一年使用:0次
名校
4 . T℃时,向体积不等的恒容密闭容器中加入足量活性炭和1mol ,发生反应
,发生反应 。反应相同时间,测得各容器中
。反应相同时间,测得各容器中 的转化率与容器体积的关系如图所示,下列说法正确的是
的转化率与容器体积的关系如图所示,下列说法正确的是
 ,发生反应
,发生反应 。反应相同时间,测得各容器中
。反应相同时间,测得各容器中 的转化率与容器体积的关系如图所示,下列说法正确的是
的转化率与容器体积的关系如图所示,下列说法正确的是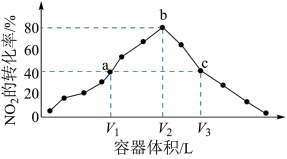
| A.a点对应容器中,反应未达到平衡状态 |
B.向b点对应容器中再充入一定量 ,达到新平衡时, ,达到新平衡时, 的转化率增大 的转化率增大 |
| C.缩小c点对应容器的体积增大压强,v(正)<v(逆) |
D.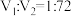 |
您最近一年使用:0次
名校
5 . 下列实验操作正确且能达到实验目的的是
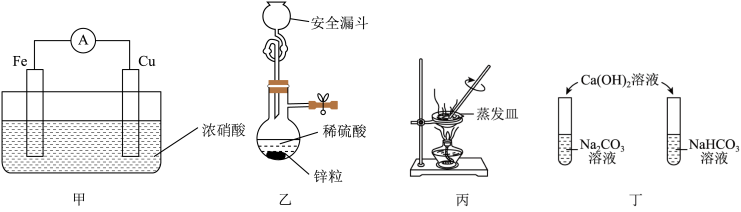
| A.用甲装置判断Fe和Cu金属的活泼性 |
B.用乙装置制取少量 |
C.用丙装置除去NaCl固体中的 |
D.用丁装置鉴别 溶液和 溶液和 溶液 溶液 |
您最近一年使用:0次
名校
6 . 下列说法正确的是
A.将 溶液和 溶液和 溶液分别加热、蒸干、灼烧,所得固体成分相同 溶液分别加热、蒸干、灼烧,所得固体成分相同 |
B.配制 溶液时,将 溶液时,将 固体溶于稀盐酸中,然后稀释至所需浓度 固体溶于稀盐酸中,然后稀释至所需浓度 |
C.用湿润的pH试纸测定 溶液的pH,会使测得结果偏大 溶液的pH,会使测得结果偏大 |
D.将 溶液稀释10倍,溶液中 溶液稀释10倍,溶液中 不变 不变 |
您最近一年使用:0次
名校
7 . 某种电解质由X、Y、Z、Q、W五元素短周期元素组成,原子序数依次增大,X原子中没有中子,Y元素形成的化合物种类最多,Z的单质在空气中含量最多,Q为地壳中含量最多的金属,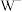 能与
能与 反应产生白色沉淀,下列说法正确的是
反应产生白色沉淀,下列说法正确的是
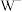 能与
能与 反应产生白色沉淀,下列说法正确的是
反应产生白色沉淀,下列说法正确的是A.第一电离能: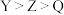 | B.Z的氢化物中各原子均满足8电子稳定结构 |
| C.W的含氧酸均为强酸 | D.半径: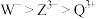 |
您最近一年使用:0次
8 . 下列方案设计、现象和结论均正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 鉴定某涂改液中是否存在含氯化合物 | 涂改液与KOH溶液混合加热,充分反应,取上层清液,加入足量稀硝酸,最后滴加硝酸银溶液 | 出现白色沉淀,说明涂改液中存在含氯化合物 |
| B | 证明非金属性 | 向装有FeS固体的试管中滴加稀盐酸 | 固体溶解,生成臭鸡蛋气味气体,证明非金属性 |
| C | 检验乙醇中是否混有乙醛 | 取待测液,滴加酸性高锰酸钾溶液 | 高锰酸钾溶液褪色,证明乙醇中混有乙醛 |
| D | 检验 样品是否变质 样品是否变质 | 将 样品溶于稀 样品溶于稀 ,滴加KSCN溶液 ,滴加KSCN溶液 | 观察到溶液变红,证明样品已氧化变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 . 肼( )是一种应用广泛的化工原料,可用作火箭和燃料电池的燃料。实验室制取肼的化学方程式为:
)是一种应用广泛的化工原料,可用作火箭和燃料电池的燃料。实验室制取肼的化学方程式为: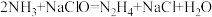 。已知
。已知 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 )是一种应用广泛的化工原料,可用作火箭和燃料电池的燃料。实验室制取肼的化学方程式为:
)是一种应用广泛的化工原料,可用作火箭和燃料电池的燃料。实验室制取肼的化学方程式为: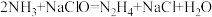 。已知
。已知 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A. 分子中含有的质子数为 分子中含有的质子数为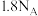 |
B.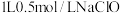 溶液中 溶液中 浓度为 浓度为 |
C.每消耗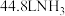 ,理论上转移电子数为 ,理论上转移电子数为 |
D.常温下, 的NaClO溶液中, 的NaClO溶液中, 的数目为 的数目为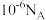 |
您最近一年使用:0次
名校
解题方法
10 . 科学家已获得极具理论研究意义的N4分子,其结构为正四面体(如下图所示),与白磷分子相似。已知断裂1 mol N-N键吸收193 kJ热量 ,形成1 mol N≡N叁键放出941 kJ热量,则
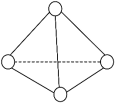
| A.N4分子中的N是sp2杂化 | B.N4是极性分子 |
| C.N4和N2互为同分异构体 | D.1 mol N4气体转化为N2时放出724 kJ 能量 |
您最近一年使用:0次



