名校
1 . 某液晶分子结构如图所示,X、Y、Z、W为原子序数依次增大的短周期非金属元素,基态X原子的电子只有一种自旋取向,基态W原子核外s能级上电子总数与p能级上电子总数相等,Y与W的质子数之和等于Z的质子数的2倍。下列说法正确的是
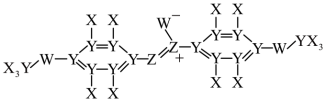
A.Y、Z、W的杂化方式均为 |
| B.第一电离能:Z>W>Y |
C.分子键能: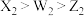 |
| D.氢化物沸点:W>Z>Y |
您最近一年使用:0次
2 . 近年来我国科技研究取得重大成就,科技创新离不开化学。下列相关叙述正确的是
| A.量子通信材料螺旋碳纳米管TEM与石墨烯互为同位素 |
| B.中国空间站太阳翼使用氮化镓(GaN)半导体材料,GaN属于新型金属材料 |
| C.可再生生物降解餐具的成分为聚乳酸(PLA),PLA属于有机高分子材料 |
| D.华为Mate60pro手机的CPU基础材料是SiO2 |
您最近一年使用:0次
名校
3 . 硅与储及其化合物在医药、生产、生活中有着重要的作用。回答下列问题:
(1)某铁的配合物结构如图所示,可由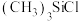 与
与 混合加热制得。
混合加热制得。_______ 区。C、O、H三种元素的电负性从大到小的顺序为_______ 。
②配位体CO分子中碳元素提供孤电子对的原因:_______ 。铁的配合物中碳元素的杂化方式共有_______ 种。
③在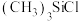 、
、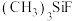 、
、 中,
中,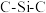 键角最大的是
键角最大的是_______ 。
(2)硅和卤素单质反应可以得到SiX4,SiX4的熔沸点如下表(已知:绝对零度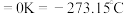 ):
):
0℃时,SiF4、SiCl4、SiBr4、SiI4呈液态的是_______ (填化学式),沸点依次升高的原因是_______ ,气态SiX4分子的空间结构是_______ 。
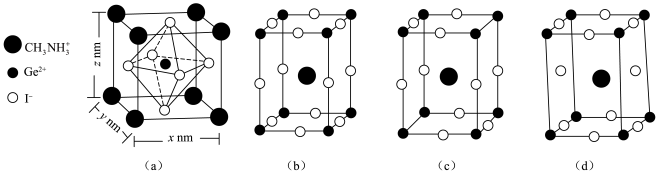
(3)一种含锗的化合物应用于太阳能电池,其晶胞为长方体,结构如图(a):_______ (填“b”“c”或“d”)图也能表示此化合物的晶胞。
②已知晶胞(a)密度为 ,则阿伏加德罗常数的值为
,则阿伏加德罗常数的值为_______ (用含x、y、z和ρ的式子表示)。
(1)某铁的配合物结构如图所示,可由
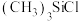 与
与 混合加热制得。
混合加热制得。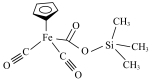
②配位体CO分子中碳元素提供孤电子对的原因:
③在
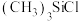 、
、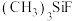 、
、 中,
中,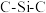 键角最大的是
键角最大的是(2)硅和卤素单质反应可以得到SiX4,SiX4的熔沸点如下表(已知:绝对零度
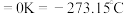 ):
):| SiF4 | SiCl4 | SiBr4 | SiI4 | |
| 熔点/K | 183.0 | 203.2 | 278.6 | 393.7 |
| 沸点/K | 187.2 | 330.8 | 427.2 | 560.7 |
(3)一种含锗的化合物应用于太阳能电池,其晶胞为长方体,结构如图(a):
②已知晶胞(a)密度为
 ,则阿伏加德罗常数的值为
,则阿伏加德罗常数的值为
您最近一年使用:0次
昨日更新
|
23次组卷
|
2卷引用:山西省运城市三晋卓越联盟2023-2024学年高二下学期期中考试化学试题
名校
解题方法
4 . 一定条件下,O2得电子转化为超氧自由基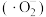 ,并实现如图所示的转化:
,并实现如图所示的转化:
(1)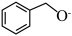 中有
中有___________ 种不同化学环境的氢原子。
(2)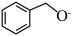 转化为
转化为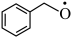 是
是___________ (填“氧化”或“还原”)反应。
(3)写出图示转化总反应的化学方程式:___________ 。
(4)用现代仪器区分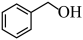 与
与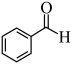 的方法是
的方法是___________ 。
(5)已知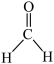 分子中所有原子都在同一平面内,则
分子中所有原子都在同一平面内,则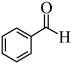 中至多有
中至多有___________ 个原子共平面。
(6)已知10.8g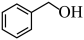 在足量O2中充分燃烧,混合气体依次通过足量的浓硫酸和碱石灰,分别增重
在足量O2中充分燃烧,混合气体依次通过足量的浓硫酸和碱石灰,分别增重___________ g和___________ g。
(7)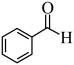 继续氧化产物(C7H6O2)与
继续氧化产物(C7H6O2)与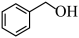 反应的化学方程式:
反应的化学方程式:___________ 。
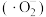 ,并实现如图所示的转化:
,并实现如图所示的转化: 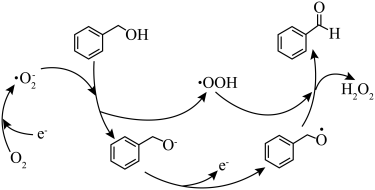
(1)
 中有
中有(2)
 转化为
转化为 是
是(3)写出图示转化总反应的化学方程式:
(4)用现代仪器区分
 与
与 的方法是
的方法是(5)已知
 分子中所有原子都在同一平面内,则
分子中所有原子都在同一平面内,则 中至多有
中至多有(6)已知10.8g
 在足量O2中充分燃烧,混合气体依次通过足量的浓硫酸和碱石灰,分别增重
在足量O2中充分燃烧,混合气体依次通过足量的浓硫酸和碱石灰,分别增重(7)
 继续氧化产物(C7H6O2)与
继续氧化产物(C7H6O2)与 反应的化学方程式:
反应的化学方程式:
您最近一年使用:0次
昨日更新
|
29次组卷
|
2卷引用:山西省运城市三晋卓越联盟2023-2024学年高二下学期期中考试化学试题
5 . 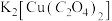 可用于功能材料的制备。下列说法正确的是
可用于功能材料的制备。下列说法正确的是
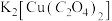 可用于功能材料的制备。下列说法正确的是
可用于功能材料的制备。下列说法正确的是| A.碳原子与氮原子形成的(CN)2属于极性分子 |
| B.钾晶体中1个K+只与1个价层电子存在强烈的相互作用 |
| C.第二周期中,第一电离能大于氧元素的有三种 |
| D.基态铜原子的4s电子能量较高,总是在比3s电子离核更远的地方运动 |
您最近一年使用:0次
昨日更新
|
19次组卷
|
2卷引用:山西省运城市三晋卓越联盟2023-2024学年高二下学期期中考试化学试题
名校
解题方法
6 . 已知有下列类物质(黑点表示碳原子,氢原子已省略)。下列说法错误的是
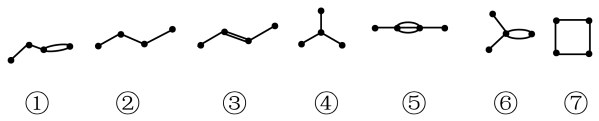
| A.①的名称为1-丁烯 | B.①③⑥互为同分异构体 |
| C.④与②互为同系物 | D.⑦的核磁共振氢谱只有一组峰 |
您最近一年使用:0次
昨日更新
|
51次组卷
|
2卷引用:山西省运城市三晋卓越联盟2023-2024学年高二下学期期中考试化学试题
名校
解题方法
7 . 有机物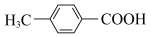 有多种同分异构体,其中属于酯类并含有苯环的同分异构体有(不考虑立体异构)
有多种同分异构体,其中属于酯类并含有苯环的同分异构体有(不考虑立体异构)
| A.5种 | B.6种 | C.7种 | D.8种 |
您最近一年使用:0次
昨日更新
|
62次组卷
|
2卷引用:山西省运城市三晋卓越联盟2023-2024学年高二下学期期中考试化学试题
名校
解题方法
8 . 设NA是阿伏加德罗常数的值。下列说法正确的是
| A.1molCH≡CH分子中所含的σ键数目为5NA |
| B.22.4LCH4分子中含有的C-H数目为4NA |
| C.标准状况下,28gCH2=CH2中含π键数目为NA |
| D.CH4和2.2.4LCl2恰好完全反应,生成的CH3Cl数目为0.1NA |
您最近一年使用:0次
昨日更新
|
64次组卷
|
2卷引用:山西省运城市三晋卓越联盟2023-2024学年高二下学期期中考试化学试题
9 . 某芳香烃A的质谱图如图所示。该烃为
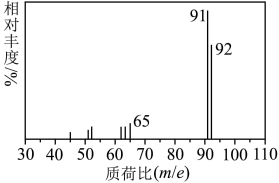
| A.甲苯 | B.乙苯 | C.二甲苯 | D.苯乙烯 |
您最近一年使用:0次
昨日更新
|
52次组卷
|
2卷引用:山西省运城市三晋卓越联盟2023-2024学年高二下学期期中考试化学试题
名校
解题方法
10 .  主要用作陶瓷、玻璃、搪瓷的着色颜料,也可用于镍粉的制造及磁性体的研究。以含镍矿渣(主要含
主要用作陶瓷、玻璃、搪瓷的着色颜料,也可用于镍粉的制造及磁性体的研究。以含镍矿渣(主要含 ,还有少量
,还有少量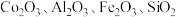 等)为原料制备
等)为原料制备 的工艺流程如图所示。
的工艺流程如图所示。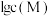 与溶液
与溶液 的关系如图所示。
的关系如图所示。 (水相)
(水相) (有机相)
(有机相) (有机相)
(有机相) (水相)。
(水相)。
回答下列问题:
(1) 元素位于周期表中第
元素位于周期表中第_______ 纵列,基态 原子的价层电子排布式为
原子的价层电子排布式为_______ 。
(2) 的晶体类型相同,则熔点由高到低的顺序为
的晶体类型相同,则熔点由高到低的顺序为_______ 。
(3)滤饼1、2的主要成分分别为_______ 、_______ (填化学式)。
(4) 在反应器1中发生反应的离子方程式为
在反应器1中发生反应的离子方程式为_______ 。
(5)加入有机萃取剂进行分液操作时,实验室使用的主要玻璃仪器为_______ ,水层为 溶液,经
溶液,经_______ 、过滤、洗涤、干燥可得到 晶体。
晶体。
(6)常温下,“调 ”时,若溶液中
”时,若溶液中 浓度为
浓度为 ,则需控制溶液的
,则需控制溶液的 范围是
范围是___ 。
(7)用电解法制取 时,先用
时,先用 调节溶液的
调节溶液的 至7.5,再加入适量
至7.5,再加入适量 用惰性电极进行电解。电解过程中所产生的
用惰性电极进行电解。电解过程中所产生的 大约有40%在弱碱性条件下生成
大约有40%在弱碱性条件下生成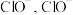 再把二价镍氧化为三价镍,则阴极的电极反应式为
再把二价镍氧化为三价镍,则阴极的电极反应式为_______ 。
 主要用作陶瓷、玻璃、搪瓷的着色颜料,也可用于镍粉的制造及磁性体的研究。以含镍矿渣(主要含
主要用作陶瓷、玻璃、搪瓷的着色颜料,也可用于镍粉的制造及磁性体的研究。以含镍矿渣(主要含 ,还有少量
,还有少量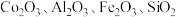 等)为原料制备
等)为原料制备 的工艺流程如图所示。
的工艺流程如图所示。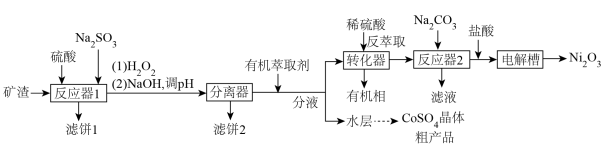
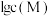 与溶液
与溶液 的关系如图所示。
的关系如图所示。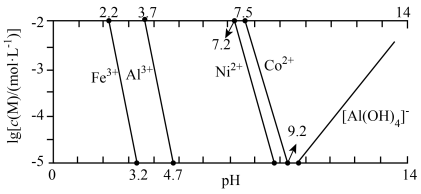
 (水相)
(水相) (有机相)
(有机相) (有机相)
(有机相) (水相)。
(水相)。回答下列问题:
(1)
 元素位于周期表中第
元素位于周期表中第 原子的价层电子排布式为
原子的价层电子排布式为(2)
 的晶体类型相同,则熔点由高到低的顺序为
的晶体类型相同,则熔点由高到低的顺序为(3)滤饼1、2的主要成分分别为
(4)
 在反应器1中发生反应的离子方程式为
在反应器1中发生反应的离子方程式为(5)加入有机萃取剂进行分液操作时,实验室使用的主要玻璃仪器为
 溶液,经
溶液,经 晶体。
晶体。(6)常温下,“调
 ”时,若溶液中
”时,若溶液中 浓度为
浓度为 ,则需控制溶液的
,则需控制溶液的 范围是
范围是(7)用电解法制取
 时,先用
时,先用 调节溶液的
调节溶液的 至7.5,再加入适量
至7.5,再加入适量 用惰性电极进行电解。电解过程中所产生的
用惰性电极进行电解。电解过程中所产生的 大约有40%在弱碱性条件下生成
大约有40%在弱碱性条件下生成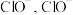 再把二价镍氧化为三价镍,则阴极的电极反应式为
再把二价镍氧化为三价镍,则阴极的电极反应式为
您最近一年使用:0次
7日内更新
|
93次组卷
|
2卷引用:2024届山西省名校高三下学期二模联考考试理综试题-高中化学



