解题方法
1 .  在Ni的活化下可放出
在Ni的活化下可放出 ,其反应历程如下图所示。下列关于该反应历程的说法正确的是
,其反应历程如下图所示。下列关于该反应历程的说法正确的是
 在Ni的活化下可放出
在Ni的活化下可放出 ,其反应历程如下图所示。下列关于该反应历程的说法正确的是
,其反应历程如下图所示。下列关于该反应历程的说法正确的是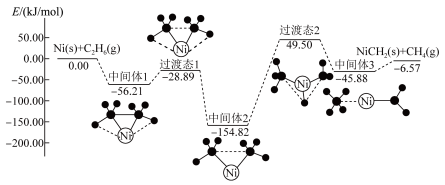
| A.该反应历程的决速步反应是中间体2→过渡态2 |
| B.此反应过程中有极性键和非极性键的断裂和生成 |
| C.整个过程中Ni是该反应的催化剂 |
| D.该反应过程中共包含4个基元反应 |
您最近一年使用:0次
解题方法
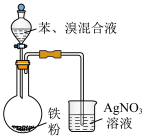
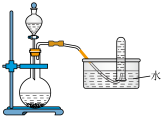
2 . 下列实验装置正确且能达到实验目的的是
选项 | A | B |
实验装置 |
|
|
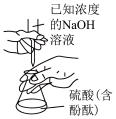
实验目的 | 制备溴苯并验证有HBr产生 | 滴定未知浓度的硫酸 |
选项 | C | D |
实验装置 |
|
|
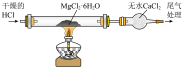
实验目的 | 制备无水 | 浓盐酸和 制备并收集 制备并收集 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . 根据下列实验操作和现象得出的结论错误的是
选项 | 实验操作和现象 | 实验结论 |
A | 向含有锌钡白( )粉末的浊液中滴加几滴 )粉末的浊液中滴加几滴 稀溶液,立即变黑 稀溶液,立即变黑 |
|
B | 向浓度均为0.1mol/L的苯酚钠和碳酸钠的混合溶液中逐渐滴加稀盐酸,开始无明显现象,后来变浑浊,最后有气泡产生 | 电离程度: |
C | 向盛有2mL 0.1mol/L  溶液的试管中,滴加几滴KSCN,再滴加过量抗氧化剂丁基羟基茴香醚,溶液由红色变为浅绿色 溶液的试管中,滴加几滴KSCN,再滴加过量抗氧化剂丁基羟基茴香醚,溶液由红色变为浅绿色 | 丁基羟基茴香醚具有还原性 |
D | 向淀粉溶液中加入稀硫酸,加热,待溶液冷却后向其中加入过量NaOH,再加碘水,不变蓝 | 淀粉已彻底水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 有一种离子液体结构如图: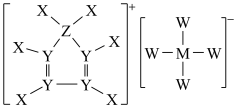 ,其中X、Y、Z、W、M为原子序数依次增大的短周期主族元素,核电荷数:M=Y+Z,下列说法中错误的是
,其中X、Y、Z、W、M为原子序数依次增大的短周期主族元素,核电荷数:M=Y+Z,下列说法中错误的是
| A.电负性:X<Y<Z |
| B.简单离子半径:M<W<Z |
| C.简单氢化物沸点:Z>W>Y |
| D.Y和Z简单氢化物VSEPR模型均为四面体形 |
您最近一年使用:0次
解题方法
5 . 一种储氢材料的结构如图所示,其由短周期主族元素 组成,这四种元素的原子序数依次增大,且只有
组成,这四种元素的原子序数依次增大,且只有 位于同周期;
位于同周期;
 组成,这四种元素的原子序数依次增大,且只有
组成,这四种元素的原子序数依次增大,且只有 位于同周期;
位于同周期;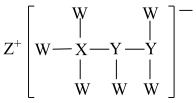
A.电负性: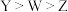 |
| B.阴离子中X和Y的杂化方式相同 |
C.与 同周期,且第一电离能介于二者之间的元素有三种 同周期,且第一电离能介于二者之间的元素有三种 |
D. 的单质分别与氧气反应,条件不同,均可得到不同的产物 的单质分别与氧气反应,条件不同,均可得到不同的产物 |
您最近一年使用:0次
6 . 磷酸铁 是合成锂离子电池正极材料磷酸铁锂的前驱体,工业上以硫铁矿(主要成分为
是合成锂离子电池正极材料磷酸铁锂的前驱体,工业上以硫铁矿(主要成分为 ,含少量
,含少量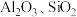 和
和 )为原料经过如下步骤可制备
)为原料经过如下步骤可制备 。
。 如下表(沉淀完全的
如下表(沉淀完全的 按金属离子浓度为
按金属离子浓度为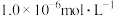 计算):
计算):
回答下列问题:
(1)“焙烧”时空气与矿料逆流而行,其目的是___________ 。
(2)“还原”的目的是___________ 。
(3)用平衡移动原理解释 能“沉铝”的原因:
能“沉铝”的原因:___________ (用必要的化学用语和文字说明);常温下,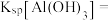
___________ (用科学计数法表示,已知 )。
)。
(4)虚线框内发生的氧化还原反应中氧化剂与还原剂的物质的量之比为___________ 。
(5)研究发现:不同 对
对 沉淀的影响如下表所示:
沉淀的影响如下表所示:
当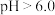 时,随
时,随 的增加,
的增加, 的沉淀率开始下降,而
的沉淀率开始下降,而 沉淀率反而上升,其原因可能为
沉淀率反而上升,其原因可能为___________ 。
(6) 的立方晶胞结构如图所示。已知:晶胞参数为
的立方晶胞结构如图所示。已知:晶胞参数为 ,用
,用 表示阿伏加德罗带数的值。
表示阿伏加德罗带数的值。 的价电子轨道表示式为
的价电子轨道表示式为___________ ; 晶体的摩尔体积=
晶体的摩尔体积=___________  (用含
(用含 的代数式表示)。
的代数式表示)。
 是合成锂离子电池正极材料磷酸铁锂的前驱体,工业上以硫铁矿(主要成分为
是合成锂离子电池正极材料磷酸铁锂的前驱体,工业上以硫铁矿(主要成分为 ,含少量
,含少量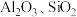 和
和 )为原料经过如下步骤可制备
)为原料经过如下步骤可制备 。
。
 如下表(沉淀完全的
如下表(沉淀完全的 按金属离子浓度为
按金属离子浓度为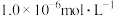 计算):
计算):| 金属离子 | 开始沉淀的 | 沉淀完全的 |
 | 1.2 | 3.3 |
 | 3.1 | 5.1 |
 | 5.8 | 8.8 |
(1)“焙烧”时空气与矿料逆流而行,其目的是
(2)“还原”的目的是
(3)用平衡移动原理解释
 能“沉铝”的原因:
能“沉铝”的原因: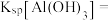
 )。
)。(4)虚线框内发生的氧化还原反应中氧化剂与还原剂的物质的量之比为
(5)研究发现:不同
 对
对 沉淀的影响如下表所示:
沉淀的影响如下表所示: | 5.0 | 5.5 | 6.0 | 6.5 | 7.0 | |
| 沉淀率/% |  | 90.0 | 94.6 | 97.9 | 96.2 | 95.3 |
 | 88.1 | 95.4 | 97.2 | 98.5 | 99.8 | |
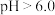 时,随
时,随 的增加,
的增加, 的沉淀率开始下降,而
的沉淀率开始下降,而 沉淀率反而上升,其原因可能为
沉淀率反而上升,其原因可能为(6)
 的立方晶胞结构如图所示。已知:晶胞参数为
的立方晶胞结构如图所示。已知:晶胞参数为 ,用
,用 表示阿伏加德罗带数的值。
表示阿伏加德罗带数的值。
 的价电子轨道表示式为
的价电子轨道表示式为 晶体的摩尔体积=
晶体的摩尔体积= (用含
(用含 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
7 . 硫代硫酸钠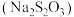 是一种常见的滴定剂和重要化工原料。工业上常用硫化碱法制备硫代硫酸钠(将
是一种常见的滴定剂和重要化工原料。工业上常用硫化碱法制备硫代硫酸钠(将 和
和 以
以 的物质的量之比配成溶液,再通入
的物质的量之比配成溶液,再通入 ),实验室模拟该制备原理设计的装置如图所示。
),实验室模拟该制备原理设计的装置如图所示。 固体的仪器的名称是
固体的仪器的名称是___________ ;装置B的作用是___________ 。
(2)配制混合溶液a的步骤:i.将 固体溶于“去氧水”中配成溶液(“去氧水”是指先煮沸一段时间,然后冷却至室温的蒸馏水);ⅱ.将
固体溶于“去氧水”中配成溶液(“去氧水”是指先煮沸一段时间,然后冷却至室温的蒸馏水);ⅱ.将 固体溶于
固体溶于 溶液中。第i步采用“去氧水”的目的是
溶液中。第i步采用“去氧水”的目的是___________ ,装置C中发生反应的化学方程式为___________ 。
(3)装置C中 不宜通入过多,其原因是
不宜通入过多,其原因是___________ 。
(4) 容易变质,可利用氧化还原反应测定其纯度(假设杂质不参加反应):称取
容易变质,可利用氧化还原反应测定其纯度(假设杂质不参加反应):称取 样品,配制成
样品,配制成 溶液。取
溶液。取 的
的 标准溶液
标准溶液 ,用硫酸酸化后加入过量
,用硫酸酸化后加入过量 ,摇匀后置于暗处,充分反应后加入少量淀粉溶液,然后用
,摇匀后置于暗处,充分反应后加入少量淀粉溶液,然后用 样品溶液滴定,恰好消耗
样品溶液滴定,恰好消耗 时达到滴定终点[已知:
时达到滴定终点[已知: (未配平)、
(未配平)、 ]。
]。
①达到滴定终点的标志为___________ 。
②样品中 的纯度为
的纯度为___________ %(用含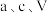 的代数式表示)。
的代数式表示)。
③诺样品中有未反应的 ,会导致测得的
,会导致测得的 的纯度
的纯度___________ (填“偏高”“偏低”或“无影响”)。
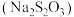 是一种常见的滴定剂和重要化工原料。工业上常用硫化碱法制备硫代硫酸钠(将
是一种常见的滴定剂和重要化工原料。工业上常用硫化碱法制备硫代硫酸钠(将 和
和 以
以 的物质的量之比配成溶液,再通入
的物质的量之比配成溶液,再通入 ),实验室模拟该制备原理设计的装置如图所示。
),实验室模拟该制备原理设计的装置如图所示。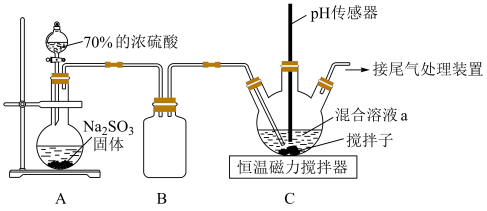
 固体的仪器的名称是
固体的仪器的名称是(2)配制混合溶液a的步骤:i.将
 固体溶于“去氧水”中配成溶液(“去氧水”是指先煮沸一段时间,然后冷却至室温的蒸馏水);ⅱ.将
固体溶于“去氧水”中配成溶液(“去氧水”是指先煮沸一段时间,然后冷却至室温的蒸馏水);ⅱ.将 固体溶于
固体溶于 溶液中。第i步采用“去氧水”的目的是
溶液中。第i步采用“去氧水”的目的是(3)装置C中
 不宜通入过多,其原因是
不宜通入过多,其原因是(4)
 容易变质,可利用氧化还原反应测定其纯度(假设杂质不参加反应):称取
容易变质,可利用氧化还原反应测定其纯度(假设杂质不参加反应):称取 样品,配制成
样品,配制成 溶液。取
溶液。取 的
的 标准溶液
标准溶液 ,用硫酸酸化后加入过量
,用硫酸酸化后加入过量 ,摇匀后置于暗处,充分反应后加入少量淀粉溶液,然后用
,摇匀后置于暗处,充分反应后加入少量淀粉溶液,然后用 样品溶液滴定,恰好消耗
样品溶液滴定,恰好消耗 时达到滴定终点[已知:
时达到滴定终点[已知: (未配平)、
(未配平)、 ]。
]。①达到滴定终点的标志为
②样品中
 的纯度为
的纯度为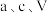 的代数式表示)。
的代数式表示)。③诺样品中有未反应的
 ,会导致测得的
,会导致测得的 的纯度
的纯度
您最近一年使用:0次
名校
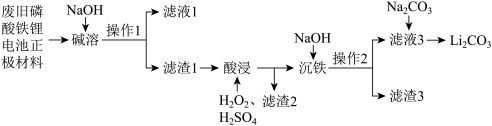
8 . 利用废旧磷酸铁锂电池正极材料(主要成分为LiFePO4、FePO4、石墨粉和铝箔)制备Li2CO3的一种流程如图所示,请回答下列问题:
(1)为了提高“碱溶”速率,可以采取的措施有___________ ;“碱溶”时铝箔发生反应的离子方程式为___________ 。
(2)“操作1”和“操作2”需要使用的主要成分为无机非金属材料的仪器有烧杯、___________ 、___________ ;滤渣2和滤渣3的主要成分分别为___________ 、___________ 。
(3)磷酸铁锂电池放电时的反应为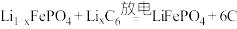 ,放电时,正极的电极反应式为
,放电时,正极的电极反应式为___________ ;若放电时电路中转移1mol电子,则电池负极质量减少___________ g。
(4)Li2CO3粗品可以用___________ (填标号)洗涤;检验Li2CO3是否洗涤干净的操作及现象为___________ 。
A.热水 B.冷水 C.稀硫酸 D.氯化锂溶液
(1)为了提高“碱溶”速率,可以采取的措施有
(2)“操作1”和“操作2”需要使用的主要成分为无机非金属材料的仪器有烧杯、
(3)磷酸铁锂电池放电时的反应为
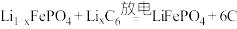 ,放电时,正极的电极反应式为
,放电时,正极的电极反应式为(4)Li2CO3粗品可以用
A.热水 B.冷水 C.稀硫酸 D.氯化锂溶液
您最近一年使用:0次
2024-06-02更新
|
201次组卷
|
4卷引用:山西省忻州市2023-2024学年高一下学期5月月考化学试题
9 . 习总书记强调:积极培育和发展新质生产力。下列与科技成就相关的描述正确的是
A.实施 海底液化封存时破坏了共价键 海底液化封存时破坏了共价键 |
| B.以废旧纺织品为原料生产再生纤维,再生纤维属于化学纤维 |
C.“北斗三号”导航卫星搭载铷原子钟,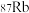 与 与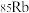 的化学性质差异很大 的化学性质差异很大 |
| D.挑战马里亚纳海沟的自供电软体机器人所用的硅树脂是新型无机非金属材料 |
您最近一年使用:0次
2024-06-02更新
|
278次组卷
|
3卷引用:2024届山西省太原市高三下学期模拟考试(二) 理科综合试卷-高中化学
名校
10 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.16.9g过氧化钡( )固体中阴、阳离子总数为0.2 )固体中阴、阳离子总数为0.2 |
B. 个氢氧化铁胶体粒子的质量是107g 个氢氧化铁胶体粒子的质量是107g |
C.70g 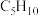 的烃分子中含有C—C 的烃分子中含有C—C  键的数目一定为4 键的数目一定为4 |
D.常温下,pH=1的醋酸溶液中含有的氢离子数为0.1 |
您最近一年使用:0次


 :ZnS>CuS
:ZnS>CuS >
> >
>


