1 . 利用下列装置(夹持装置略)进行实验,能达到实验目的的是
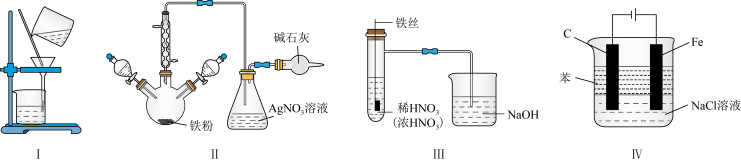
| A.用装置Ⅰ除去苯中的三溴苯酚 |
| B.用装置Ⅱ证明苯与溴发生取代反应 |
| C.用装置Ⅲ证明不同浓度硝酸还原产物可为NO、NO2 |
| D.用装置Ⅳ制备并较长时间观察到Fe(OH)2 |
您最近一年使用:0次
今日更新
|
104次组卷
|
2卷引用:2024届山东省日照市五莲县第一中学高三下学期模拟预测化学试题
名校
2 . Ⅰ.有机化合物A(相对分子质量为28)是重要的有机化工基础原料,其产量被用作衡量一个国家石油化工产业发展水平的标志。A与其他化合物之间的转化关系如图所示,回答下列问题。________________ 。
(2)上图中的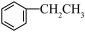 也可由B与
也可由B与 在
在 作催化剂的条件下合成,反应的化学方程式是
作催化剂的条件下合成,反应的化学方程式是_______________ ,反应类型是_______________ 。
Ⅱ.回答下列问题
(3)CO与 反应还可制备
反应还可制备 ,
, 可作为燃料使用,用
可作为燃料使用,用 和
和 组合形成的质子交换膜燃料电池的结构示意图如下:
组合形成的质子交换膜燃料电池的结构示意图如下:__________________ 。若线路中转移2mol电子,则上述 燃料电池,消耗的
燃料电池,消耗的 在标准状况下的体积为
在标准状况下的体积为__________ L。
(4)2023年12月丰城顺利通过了创文明城的验收,文明驾驶就是其中的一条。一种基于碱性燃料电池原理设计的酒精检测仪,负极上的反应为______________________ 。
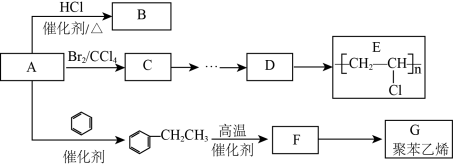
(2)上图中的
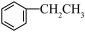 也可由B与
也可由B与 在
在 作催化剂的条件下合成,反应的化学方程式是
作催化剂的条件下合成,反应的化学方程式是Ⅱ.回答下列问题
(3)CO与
 反应还可制备
反应还可制备 ,
, 可作为燃料使用,用
可作为燃料使用,用 和
和 组合形成的质子交换膜燃料电池的结构示意图如下:
组合形成的质子交换膜燃料电池的结构示意图如下:
 燃料电池,消耗的
燃料电池,消耗的 在标准状况下的体积为
在标准状况下的体积为(4)2023年12月丰城顺利通过了创文明城的验收,文明驾驶就是其中的一条。一种基于碱性燃料电池原理设计的酒精检测仪,负极上的反应为
您最近一年使用:0次
名校
解题方法
3 . 利用CO2与H2电化学催化还原制备HCOOH的反应机理(M为催化剂)和不同催化剂(Bi、BiIn或In)下的相对能量变化如图所示(*表示吸附态)。下列说法错误的是

| A.存在2个副反应 | B.电化学还原时,HCOOH是阴极产物 |
| C.使用BiIn作催化剂更优 | D.降低温度有利于提高CO2制甲酸的平衡转化率 |
您最近一年使用:0次
今日更新
|
72次组卷
|
2卷引用:2024届山东省日照市五莲县第一中学高三下学期模拟预测化学试题
名校
4 . 实验室制取溴苯的装置如图所示。
有关数据如下:
回答下列问题:
(1)仪器a的作用是___________ 。
(2)二颈烧瓶中生成有机物发生反应的化学方程式为___________ 。
(3)A装置盛装___________ (填试剂)用于检验诱导期已过,反应开始。当出现 ___________ (填现象)时,证明反应已结束。
(4)取反应后的混合物,经过一系列操作得到纯净的溴苯:
①水洗除去___________ ,分液;
②用NaOH稀溶液洗涤,除去___________ ,分液;
③水洗,分液;
④用干燥剂干燥,过滤;
⑤___________ ,分离溴苯和苯。
(5)经过一系列操作得到纯净的溴苯5ml,产率为___________ (保留三位有效数字)。
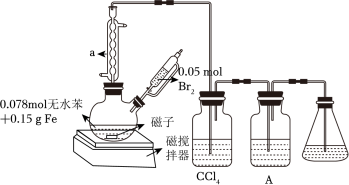
有关数据如下:
| 物质 | 苯 | 溴 | 溴苯 |
| 密度(g•cm﹣3) | 0.88 | 3.12 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 在水中的溶解性 | 不溶 | 微溶 | 不溶 |
(1)仪器a的作用是
(2)二颈烧瓶中生成有机物发生反应的化学方程式为
(3)A装置盛装
(4)取反应后的混合物,经过一系列操作得到纯净的溴苯:
①水洗除去
②用NaOH稀溶液洗涤,除去
③水洗,分液;
④用干燥剂干燥,过滤;
⑤
(5)经过一系列操作得到纯净的溴苯5ml,产率为
您最近一年使用:0次
5 . 某有机物的结构简式如图所示,其性质有下列说法不正确的是

| A.含酚羟基,遇FeCl3溶液显紫色 |
| B.1mol该有机物最多能与3molNaOH 反应 |
| C.1mol该有机物最多能与2mol Na2CO3反应 |
| D.能与羧酸发生酯化反应,也能与醇发生酯化反应,也可以进行分子内酯化反应 |
您最近一年使用:0次
名校
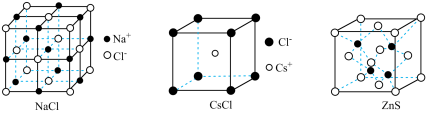
6 . 下列说法错误的是
| A.乙烯分子中,碳原子的sp2杂化轨道形成σ键,未杂化的2p轨道形成π键 |
| B.苯酚具有弱酸性的原因是苯环使羟基中的O-H极性变强 |
| C.冰晶体中每个水分子与另外四个水分子形成氢键,且四个水分子形成四面体结构 |
D.上述三种晶胞中,其阳离子的配位数大小关系为 |
您最近一年使用:0次
名校
解题方法
7 . 下列实验操作或对实验事实的描述正确的有
①除去苯中的己烯:向溶液中加入浓溴水,分液
②鉴别己烯和甲苯:向己烯和甲苯中分别滴入酸性KMnO4溶液,振荡观察是否褪色
③除去乙烷中少量乙烯:通入氢气在一定条件下反应,使乙烯转化为乙烷
④用浓溴水可将C2H5OH.AgNO3溶液、C2H5Br、苯区分开
①除去苯中的己烯:向溶液中加入浓溴水,分液
②鉴别己烯和甲苯:向己烯和甲苯中分别滴入酸性KMnO4溶液,振荡观察是否褪色
③除去乙烷中少量乙烯:通入氢气在一定条件下反应,使乙烯转化为乙烷
④用浓溴水可将C2H5OH.AgNO3溶液、C2H5Br、苯区分开
⑤CH3Cl、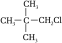 、
、 中加入NaOH的醇溶液共热,然后加入稀硝酸呈酸性,再滴入AgNO3溶液,均有沉淀生成
中加入NaOH的醇溶液共热,然后加入稀硝酸呈酸性,再滴入AgNO3溶液,均有沉淀生成
| A.①⑤ | B.④ | C.①③ | D.②⑤ |
您最近一年使用:0次
解题方法
8 . 面向“碳中和”的绿色化学是当前研究的重要方向。回答下列问题:
(1)一定条件下由丙烷制备丙烯有以下两种方式:
反应i:
 ;
;
反应ii: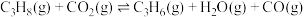
 。
。
已知上述反应中相关的键能数据如表所示。
则
___________  。
。
(2)在 温度下,将
温度下,将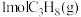 和
和 充入恒容密闭容器中,在一定条件下发生反应i、ii。测得
充入恒容密闭容器中,在一定条件下发生反应i、ii。测得 转化率及体系内压强随时间的变化关系如图所示(忽略温度对催化剂活性的影响)。
转化率及体系内压强随时间的变化关系如图所示(忽略温度对催化剂活性的影响)。 时,
时, 的平衡转化率是
的平衡转化率是___________ 。
② 时,从反应开始到反应达到平衡,用
时,从反应开始到反应达到平衡,用 的分压变化表示的化学反应速率为
的分压变化表示的化学反应速率为___________  。
。
③ 时,反应i的
时,反应i的
___________  。
。
(3)在一定条件下, 与
与 合成甲醇的反应为
合成甲醇的反应为
 ,已知速率方程
,已知速率方程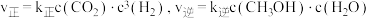 ,
, 、
、 是速率常数,只受温度影响。图甲、图乙分别表示平衡常数、速率常数的对数
是速率常数,只受温度影响。图甲、图乙分别表示平衡常数、速率常数的对数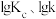 与温度的倒数
与温度的倒数 之间的关系。降低温度,
之间的关系。降低温度,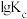 的变化曲线为
的变化曲线为___________ (填字母,下同),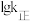 的变化曲线为
的变化曲线为___________ 。 在催化剂表面发生以下反应:
在催化剂表面发生以下反应:
反应iii.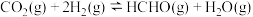
 ;
;
反应iv.
 。
。
在密闭容器中,保持投料比不变,将 与
与 按一定流速通过反应器,
按一定流速通过反应器, 转化率和甲烷选择性
转化率和甲烷选择性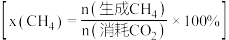 随温度变化关系如图所示。若
随温度变化关系如图所示。若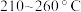 时,催化剂的活性受温度影响不大,则
时,催化剂的活性受温度影响不大,则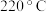 后图中曲线下降的原因是
后图中曲线下降的原因是___________ ;若气体流速过大, 的转化率会降低,原因是
的转化率会降低,原因是___________ 。
(1)一定条件下由丙烷制备丙烯有以下两种方式:
反应i:

 ;
;反应ii:
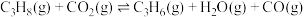
 。
。已知上述反应中相关的键能数据如表所示。
| 化学键 |  |  |  |  |
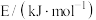 | 436 | 413 | 348 | 615 |

 。
。(2)在
 温度下,将
温度下,将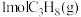 和
和 充入恒容密闭容器中,在一定条件下发生反应i、ii。测得
充入恒容密闭容器中,在一定条件下发生反应i、ii。测得 转化率及体系内压强随时间的变化关系如图所示(忽略温度对催化剂活性的影响)。
转化率及体系内压强随时间的变化关系如图所示(忽略温度对催化剂活性的影响)。
 时,
时, 的平衡转化率是
的平衡转化率是②
 时,从反应开始到反应达到平衡,用
时,从反应开始到反应达到平衡,用 的分压变化表示的化学反应速率为
的分压变化表示的化学反应速率为 。
。③
 时,反应i的
时,反应i的
 。
。(3)在一定条件下,
 与
与 合成甲醇的反应为
合成甲醇的反应为
 ,已知速率方程
,已知速率方程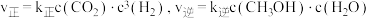 ,
, 、
、 是速率常数,只受温度影响。图甲、图乙分别表示平衡常数、速率常数的对数
是速率常数,只受温度影响。图甲、图乙分别表示平衡常数、速率常数的对数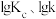 与温度的倒数
与温度的倒数 之间的关系。降低温度,
之间的关系。降低温度,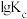 的变化曲线为
的变化曲线为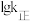 的变化曲线为
的变化曲线为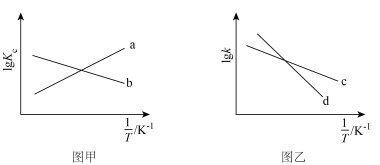
 在催化剂表面发生以下反应:
在催化剂表面发生以下反应:反应iii.
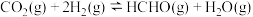
 ;
;反应iv.

 。
。在密闭容器中,保持投料比不变,将
 与
与 按一定流速通过反应器,
按一定流速通过反应器, 转化率和甲烷选择性
转化率和甲烷选择性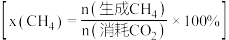 随温度变化关系如图所示。若
随温度变化关系如图所示。若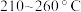 时,催化剂的活性受温度影响不大,则
时,催化剂的活性受温度影响不大,则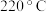 后图中曲线下降的原因是
后图中曲线下降的原因是 的转化率会降低,原因是
的转化率会降低,原因是
您最近一年使用:0次
解题方法
9 . 从硝酸铜和硝酸银的混合溶液中回收铜和银的流程如图所示。

| A.试剂Ⅰ可以是稀盐酸或稀硫酸 |
| B.流程中涉及的反应均是氧化还原反应 |
C.生成银氨溶液的离子方程式为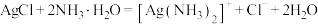 |
D.若试剂Ⅱ是甲醛, 甲醛参加反应最多生成 甲醛参加反应最多生成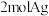 |
您最近一年使用:0次
解题方法
10 . 乙烯的产量可用来衡量一个国家石油化学工业的发展水平,通过电解可实现乙烯的高效利用,电解装置如图所示( 电极均为惰性电极)。下列说法正确的是
电极均为惰性电极)。下列说法正确的是
 电极均为惰性电极)。下列说法正确的是
电极均为惰性电极)。下列说法正确的是
| A.N是电源负极 |
| B.离子交换膜是阴离子交换膜 |
C.a电极反应式为 |
D.消耗 (标准状况下),阴极区溶液质量减少 (标准状况下),阴极区溶液质量减少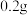 |
您最近一年使用:0次



