从硝酸铜和硝酸银的混合溶液中回收铜和银的流程如图所示。

| A.试剂Ⅰ可以是稀盐酸或稀硫酸 |
| B.流程中涉及的反应均是氧化还原反应 |
C.生成银氨溶液的离子方程式为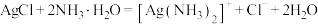 |
D.若试剂Ⅱ是甲醛, 甲醛参加反应最多生成 甲醛参加反应最多生成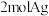 |
更新时间:2024-06-01 14:08:57
|
相似题推荐
多选题
|
适中
(0.65)
【推荐1】由硫铁矿烧渣(主要成分为Fe3O4、Fe2O3、FeO和SiO2)制备绿矾(FeSO4·7H2O)的流程如下,已知:FeS2难溶于水。
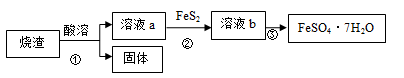
下列说法错误的是

下列说法错误的是
| A.步骤①酸溶烧渣最好选用硫酸 |
B.步骤②涉及的离子反应为FeS2+16Fe3++8H2O=17Fe2++2SO +16H+ +16H+ |
| C.步骤③须控制条件防止氧化 |
| D.将溶液b加热到有较多固体析出,再用余热将液体蒸干得纯净绿矾 |
您最近一年使用:0次
【推荐2】高锰酸钾溶液在酸性条件下可以与硫酸亚铁反应,化学方程式如下(未配平):KMnO4+FeSO4+H2SO4―→K2SO4+MnSO4+Fe2(SO4)3+H2O。下列说法正确的是
| A.Fe2+的还原性强于Mn2+ |
| B.MnO4-是氧化剂,Fe3+是还原产物 |
| C.生成1 mol水时,转移1.25 mol电子 |
| D.取反应后的溶液加KSCN溶液,可观察到有血红色沉淀生成 |
您最近一年使用:0次
【推荐1】探究甲醛与新制Cu(OH)2的反应:①向6mL6mol/LNaOH溶液中滴加8滴2%CuSO4溶液,振荡,加入0.5mL15%甲醛溶液,混合均匀,水浴加热,迅速产生红色沉淀,产生无色气体;②反应停止后分离出沉淀,将所得沉淀洗净后加入浓盐酸,不溶解;③相同条件下,甲酸钠溶液与新制Cu(OH)2共热,未观察到明显现象:已知: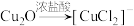 ,甲醛是具有强还原性的气体,下列说法正确的是
,甲醛是具有强还原性的气体,下列说法正确的是
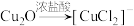 ,甲醛是具有强还原性的气体,下列说法正确的是
,甲醛是具有强还原性的气体,下列说法正确的是| A.红色沉淀的主要成分不是Cu2O,可能是Cu |
| B.将产生的无色气体通过灼热的CuO后得到红色固体,气体中一定含有CO |
C.从甲醛的结构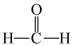 推测,其氧化产物可能为碳酸( 推测,其氧化产物可能为碳酸(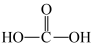 ) ) |
| D.实验中会得到大量含有CO2的无色气体 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】下列离子方程式正确的是
| A.甲酸与碳酸钠溶液反应:2H++CO32-=CO2↑+H2O |
| B.醋酸溶液与Cu(OH)2:2CH3COOH+Cu(OH)2=Cu2++2CH3COO-+2H2O |
| C.苯酚钠溶液通少量CO2 :2C6H5O-+CO2+H2O→2C6H5OH+CO32- |
D.甲醛溶液与足量的银氨溶液共热:HCHO +4Ag(NH3)2++4OH- CO32-+2NH4++4Ag↓ +6NH3+2H2O CO32-+2NH4++4Ag↓ +6NH3+2H2O |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】向 溶液中分别加入少量的NaOH溶液和
溶液中分别加入少量的NaOH溶液和 溶液,前者没有明显现象,后者有少量黑色沉淀,说明
溶液,前者没有明显现象,后者有少量黑色沉淀,说明 可以微弱地解离出极少量的
可以微弱地解离出极少量的 和
和 ,已知
,已知 溶液中存在如下平衡:
溶液中存在如下平衡: ,该配离子在溶液中的解离平衡与弱电解质的电离平衡相似,下列说法错误的是
,该配离子在溶液中的解离平衡与弱电解质的电离平衡相似,下列说法错误的是
 溶液中分别加入少量的NaOH溶液和
溶液中分别加入少量的NaOH溶液和 溶液,前者没有明显现象,后者有少量黑色沉淀,说明
溶液,前者没有明显现象,后者有少量黑色沉淀,说明 可以微弱地解离出极少量的
可以微弱地解离出极少量的 和
和 ,已知
,已知 溶液中存在如下平衡:
溶液中存在如下平衡: ,该配离子在溶液中的解离平衡与弱电解质的电离平衡相似,下列说法错误的是
,该配离子在溶液中的解离平衡与弱电解质的电离平衡相似,下列说法错误的是A.向该溶液中加入少量 固体,有助于 固体,有助于 的解离 的解离 |
B.向该体系中通入 ,可以使 ,可以使 的产率增大 的产率增大 |
C.已知 、 、 和 和 的解离平衡常数分别为 的解离平衡常数分别为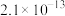 、 、 、 、 ,说明 ,说明 最不稳定, 最不稳定, 最稳定 最稳定 |
D.已知C选项中解离平衡常数,在一定条件下, 可以转化为 可以转化为 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】向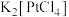 的稀盐酸溶液中通入乙烯气体可得到金黄色沉淀
的稀盐酸溶液中通入乙烯气体可得到金黄色沉淀 ,该沉淀的阴离子结构如图所示.下列有关该沉淀的阴离子说法正确的是
,该沉淀的阴离子结构如图所示.下列有关该沉淀的阴离子说法正确的是

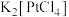 的稀盐酸溶液中通入乙烯气体可得到金黄色沉淀
的稀盐酸溶液中通入乙烯气体可得到金黄色沉淀 ,该沉淀的阴离子结构如图所示.下列有关该沉淀的阴离子说法正确的是
,该沉淀的阴离子结构如图所示.下列有关该沉淀的阴离子说法正确的是
| A.该沉淀的阴离子所有原子共平面 |
B.乙烯分子中碳原子的杂化方式为 杂化 杂化 |
| C.配位键的形成均为电子给予体提供孤电子对 |
| D.由其组成的物质可以燃烧 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】从海带中提取碘流程如下:

下列说法正确的是

下列说法正确的是
| A.海带灼烧成灰用到的实验仪器有烧杯、玻璃棒、酒精灯等 |
| B.操作1是分液、操作2是蒸馏、操作3是过滤 |
| C.操作2得到的有机层可循环使用 |
D.分散系2中加入硫酸的反应为5I-+IO +6H+=3I2+3H2O +6H+=3I2+3H2O |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】绿水青山是习近平总书记构建美丽中国的伟大构想,碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体工艺流程如图,下列说法不正确 的是


| A.分离器中的物质分离操作为过滤 |
| B.该工艺中I2和HI的相互转化体现了“碘循环” |
| C.膜反应器中,增大压强有利于提高化学反应速率 |
D.碘循环工艺的总反应为2SO2+I2+4H2O 2H2SO4+2HI+H2 2H2SO4+2HI+H2 |
您最近一年使用:0次

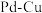 为催化剂去除水体中
为催化剂去除水体中 的机理如图a所示;其他条件相同,
的机理如图a所示;其他条件相同, 不同时,
不同时, )的关系如图b所示。
)的关系如图b所示。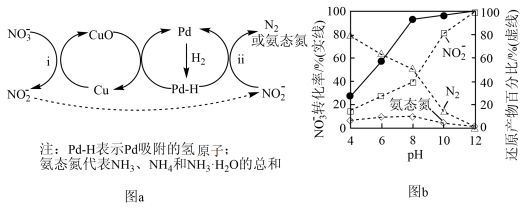
 对
对 的吸附,不影响对H的吸附。
的吸附,不影响对H的吸附。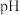 变小时
变小时 的离子方程式为
的离子方程式为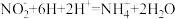
 ,理论上转移电子
,理论上转移电子
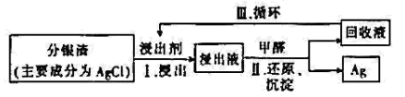
 ,“浸出”时发生的主要反应为
,“浸出”时发生的主要反应为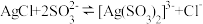 。
。 也能浸取分银渣中的Ag
也能浸取分银渣中的Ag 三种不同大小的球代表三种相对大小不同的短周期元素原子,则有关该物质的说法不正确的
三种不同大小的球代表三种相对大小不同的短周期元素原子,则有关该物质的说法不正确的


