解题方法
1 . 银及其化合物在催化与电化学等领域中具有重要应用。已知:①在银催化下,乙烯与氧气反应生成乙醛(CH3-CHO)和环氧乙烷(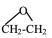 )。下图所示是两反应分步进行的历程图:
)。下图所示是两反应分步进行的历程图:
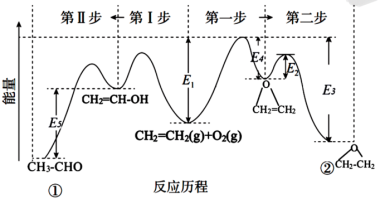
i:2CH2=CH2(g)+O2(g)⇌2CH2=CH-OH(g) ΔH1
ii:CH2=CH-OH(g) ⇌CH3-CHO(g) ΔH2
③乙烯与氧气反应生成环氧乙烷的分步反应方程式为:
iii:2CH2=CH2(g)+O2(g) 2
2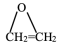 (g) ΔH3
(g) ΔH3
iv: (g)
(g)
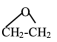 (g) ΔH4
(g) ΔH4
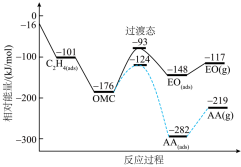
(2)根据已知条件③,乙烯与氧气反应生成环氧乙烷的热化学方程式为:
(3)根据已知条件④,中间体OMC生成吸附态AA(ads)的活化能为
 。
。(4)某温度下,在一体积为1L的恒容密闭容器中,充入1.8molCH2=CH2(g)和0.8molO2(g)发生反应:2CH2=CH2(g)+O2(g)⇌2CH3-CHO(g) ΔH,反应进行10min后到达平衡,体系中各气体的体积分数随反应温度的变化如下图所示
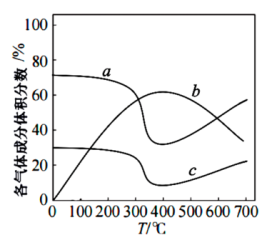
②温度为400℃,达到平衡时,化学反应速率v(O2)=
③温度为600℃,该反应的平衡常数Kc=
(5)乙醛燃料电池有广泛的应用前景,其工作原理如图所示
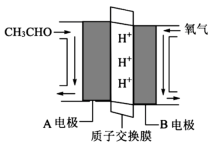
②A电极上的电极方程式为:
您最近一年使用:0次
解题方法
2 . 煤的化学活性是评价煤气化或燃烧性能的一项重要指标,可用与焦炭(由煤样制得)反应的CO2的转化率 来表示。研究小组设计模拟实验探究煤燃烧产物的转化率装置如下:
来表示。研究小组设计模拟实验探究煤燃烧产物的转化率装置如下:___________ 。
(2)装置Ⅰ中,仪器a的名称是___________ ;b的作用是___________ 。
(3)装置Ⅱ中,CO2从下口通入的原因是___________ 。气体X的成分有:___________ 。
(4)装置Ⅲ中,d中的现象是___________ 。e中生成的固体为Ag,则反应的离子方程式为___________ 。
 来表示。研究小组设计模拟实验探究煤燃烧产物的转化率装置如下:
来表示。研究小组设计模拟实验探究煤燃烧产物的转化率装置如下:
(2)装置Ⅰ中,仪器a的名称是
(3)装置Ⅱ中,CO2从下口通入的原因是
(4)装置Ⅲ中,d中的现象是
您最近一年使用:0次
解题方法
3 . 下列实验操作和现象,得出的相应结论正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向盛有Fe(OH)3和NiO(OH)的试管中分别滴加浓盐酸 | 盛NiO(OH)的试管中产生黄绿色气体 | 氧化性:NiO(OH)>Fe(OH)3>Cl2 |
| B | 向CuSO4溶液中通入H2S气体 | 出现黑色沉淀(CuS) | Cu2+能使H2S的电离平衡正向移动 |
| C | 乙醇和浓硫酸共热至170℃,将产生的气体通入溴水中 | 溴水褪色 | 产生的气体中只有乙烯和SO2 |
| D | 向Na2HPO4溶液中滴加AgNO3溶液 | 出现黄色沉淀(Ag3PO4) | Na2HPO4的水解程度大于其电离程度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . “嫦娥石”是中国首次在月球上发现的新矿物,其主要由Ca、Fe、P、O和Y(钇,原子序数比Fe大13)组成,下列说法正确的是
| A.基态Ca原子含20个运动状态不同的电子 |
| B.Y元素原子价层电子排布式为:5s24d1 |
| C.5种元素中,第一电离能最小的是Fe |
| D.5种元素中,电负性最大的是P |
您最近一年使用:0次
解题方法
5 . 已知反应: ,NA为阿伏加德罗常数的值,若消耗2.24L(标准状况)F2,下列叙述
,NA为阿伏加德罗常数的值,若消耗2.24L(标准状况)F2,下列叙述错误 的是
 ,NA为阿伏加德罗常数的值,若消耗2.24L(标准状况)F2,下列叙述
,NA为阿伏加德罗常数的值,若消耗2.24L(标准状况)F2,下列叙述| A.转移的电子数为0.2NA | B.生成的氧化产物分子数为0.2NA |
| C.生成的NaF质量为4.2g | D.消耗的F2中含有的共价键数为0.1NA |
您最近一年使用:0次
6 . 下列叙述正确的是
| A.Mg在空气中燃烧,生成的固体产物只有Mg3N2和MgO |
B. 与 与 反应属于复分解反应 反应属于复分解反应 |
C. 与 与 反应,生成的O2与电子数之比为1:1 反应,生成的O2与电子数之比为1:1 |
D.浓 与 与 反应,生成CO2、SO2两种酸性气体 反应,生成CO2、SO2两种酸性气体 |
您最近一年使用:0次
解题方法
7 . 下列离子方程式中,错误 的是
A.NO2通入水中: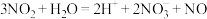 |
| B.Al投入少量NaOH溶液中:Al+OH-+2H2O=Al(OH)3↓+2H+ |
| C.Cl2通入石灰乳中:Cl2+Ca(OH)2=Ca2++Cl-+ClO-+H2O |
D.Pb放入Fe2(SO4)3溶液中: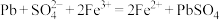 |
您最近一年使用:0次
解题方法
8 . NCl3和SiCl4均可发生水解反应,其中NCl3的水解机理示意图如下:
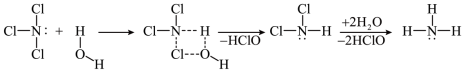
A.HClO的电子式: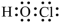 |
B.基态N原子的价层电子排布图: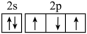 |
C.H2O分子的球棍模型: |
D.NH3的VSEPR模型: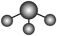 |
您最近一年使用:0次
9 . 二氧化碳催化加氢制甲醇是一种重要的碳中和方式。回答下列问题:
(1)二氧化碳加氢制甲醇的热化学方程式为
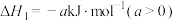 。
。
①此反应在___________ (填“高温”“常温”或“低温”)条件下容易自发进行。
②有利于提高 平衡转化率的是
平衡转化率的是___________ (填序号)。
A.降低温度 B.继续通入 C.及时将
C.及时将 分离 D.使用合适催化剂
分离 D.使用合适催化剂
③根据下表中的键能数据计算 的键能
的键能___________ 。
(2)398K时,在某刚性容器中,投入2mol 和6mol
和6mol  发生上述反应,初始压强为8MPa,反应经过5min达到平衡时
发生上述反应,初始压强为8MPa,反应经过5min达到平衡时 的物质的量等于其余三种物质的物质的量之和,用
的物质的量等于其余三种物质的物质的量之和,用 表示此反应的速率为
表示此反应的速率为___________  ,计算该温度下的
,计算该温度下的
___________  。
。
(3)①研究表明,在酸性电解质中, 气体可被电化学还原为
气体可被电化学还原为 和CO等产品。请写出
和CO等产品。请写出 被电化学还原为
被电化学还原为 的电极反应式:
的电极反应式:___________ 。
②实验证明,此电解过程中阴极产物只有 和CO,且电化学还原44g
和CO,且电化学还原44g  时转移电子的物质的量为5mol,则产物中
时转移电子的物质的量为5mol,则产物中 和CO的物质的量之比为
和CO的物质的量之比为___________ 。
(1)二氧化碳加氢制甲醇的热化学方程式为

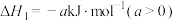 。
。①此反应在
②有利于提高
 平衡转化率的是
平衡转化率的是A.降低温度 B.继续通入
 C.及时将
C.及时将 分离 D.使用合适催化剂
分离 D.使用合适催化剂③根据下表中的键能数据计算
 的键能
的键能| 化学键 |  |  |  |  |
键能 | b | c | d | e |
(2)398K时,在某刚性容器中,投入2mol
 和6mol
和6mol  发生上述反应,初始压强为8MPa,反应经过5min达到平衡时
发生上述反应,初始压强为8MPa,反应经过5min达到平衡时 的物质的量等于其余三种物质的物质的量之和,用
的物质的量等于其余三种物质的物质的量之和,用 表示此反应的速率为
表示此反应的速率为 ,计算该温度下的
,计算该温度下的
 。
。(3)①研究表明,在酸性电解质中,
 气体可被电化学还原为
气体可被电化学还原为 和CO等产品。请写出
和CO等产品。请写出 被电化学还原为
被电化学还原为 的电极反应式:
的电极反应式:②实验证明,此电解过程中阴极产物只有
 和CO,且电化学还原44g
和CO,且电化学还原44g  时转移电子的物质的量为5mol,则产物中
时转移电子的物质的量为5mol,则产物中 和CO的物质的量之比为
和CO的物质的量之比为
您最近一年使用:0次
10 . 下列陈述 、陈述
、陈述 说法不正确或不存在关联的是
说法不正确或不存在关联的是
 、陈述
、陈述 说法不正确或不存在关联的是
说法不正确或不存在关联的是| 选项 | 陈述 | 陈述 |
| A | 盛放纯碱溶液的试剂瓶不能用磨口玻璃塞 | 碳酸钠水解产生的氢氧根离子与磨口玻璃塞中的 反应生成硅酸钠,具有较强粘合性 反应生成硅酸钠,具有较强粘合性 |
| B | 浓硝酸应保存在棕色瓶并置于阴暗处 |  光照或受热会分解 光照或受热会分解 |
| C | 向硫酸钡沉淀中加入浓碳酸钠溶液,充分搅拌后,取洗净后的沉淀放入盐酸中,有气泡产生 |  |
| D | 酸性大小: | 极性大小: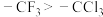 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



