解题方法
1 .  资源化是实现“双碳”目标的重要途径。
资源化是实现“双碳”目标的重要途径。
方法1:化学还原 制备
制备 、
、 、
、 等。
等。
(1)以 和
和 为原料合成乙烯,其反应的过程分两步进行:
为原料合成乙烯,其反应的过程分两步进行:
①
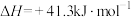
②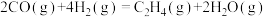
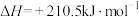
写出 加氢合成乙烯的热化学方程式:
加氢合成乙烯的热化学方程式:________ 。
(2)利用二氧化碳合成淀粉,首先是利用二氧化碳制备甲醇。已知 和
和 在某种催化剂作用下可同时发生以下两个反应:
在某种催化剂作用下可同时发生以下两个反应:
Ⅰ.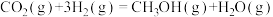
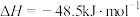
Ⅱ.
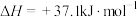
在压强为P, 、
、 的起始投料为1:3的条件下,发生反应Ⅰ、Ⅱ。实验测得
的起始投料为1:3的条件下,发生反应Ⅰ、Ⅱ。实验测得 的平衡转化率和平衡时
的平衡转化率和平衡时 的选择性随温度的变化如图所示。
的选择性随温度的变化如图所示。 的选择性
的选择性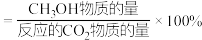
①有利于提高 的选择性的措施有
的选择性的措施有________ (填序号)。
A.适当降温 B.适当升温 C.选择合适的催化剂
②温度高于350℃时,体系中发生的反应以________ (填“Ⅰ”或“Ⅱ”)为主,说明理由:________ 。
③其中表示平衡时 的选择性的曲线是
的选择性的曲线是________ (填“a”或“b”)。
(3) 合成乙醇。在一定温度下,向容积为1L的恒容密闭容器中,充入1mol
合成乙醇。在一定温度下,向容积为1L的恒容密闭容器中,充入1mol 、xmol
、xmol ,发生反应
,发生反应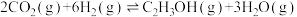 ,测得平衡体系中,
,测得平衡体系中, 的体积分数
的体积分数 与x的关系如图所示。
与x的关系如图所示。 的转化率最大的是
的转化率最大的是________ (填字母)点。该温度下,平衡常数K=________ (列出算式即可得分)。
方法2:用电解法可将 转化为多种原料。
转化为多种原料。
(4)用如图装置电解二氧化碳制取甲烷,温度控制在10℃左右,持续通入二氧化碳,电解过程中 ,物质的量基本不变。写出阴极的电极反应式
,物质的量基本不变。写出阴极的电极反应式________ ;阳极产生的气体是________ (写化学式)。
 资源化是实现“双碳”目标的重要途径。
资源化是实现“双碳”目标的重要途径。方法1:化学还原
 制备
制备 、
、 、
、 等。
等。(1)以
 和
和 为原料合成乙烯,其反应的过程分两步进行:
为原料合成乙烯,其反应的过程分两步进行:①

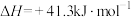
②
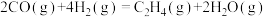
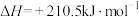
写出
 加氢合成乙烯的热化学方程式:
加氢合成乙烯的热化学方程式:(2)利用二氧化碳合成淀粉,首先是利用二氧化碳制备甲醇。已知
 和
和 在某种催化剂作用下可同时发生以下两个反应:
在某种催化剂作用下可同时发生以下两个反应:Ⅰ.
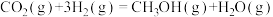
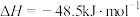
Ⅱ.

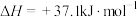
在压强为P,
 、
、 的起始投料为1:3的条件下,发生反应Ⅰ、Ⅱ。实验测得
的起始投料为1:3的条件下,发生反应Ⅰ、Ⅱ。实验测得 的平衡转化率和平衡时
的平衡转化率和平衡时 的选择性随温度的变化如图所示。
的选择性随温度的变化如图所示。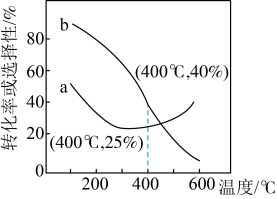
 的选择性
的选择性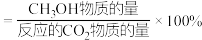
①有利于提高
 的选择性的措施有
的选择性的措施有A.适当降温 B.适当升温 C.选择合适的催化剂
②温度高于350℃时,体系中发生的反应以
③其中表示平衡时
 的选择性的曲线是
的选择性的曲线是(3)
 合成乙醇。在一定温度下,向容积为1L的恒容密闭容器中,充入1mol
合成乙醇。在一定温度下,向容积为1L的恒容密闭容器中,充入1mol 、xmol
、xmol ,发生反应
,发生反应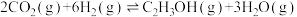 ,测得平衡体系中,
,测得平衡体系中, 的体积分数
的体积分数 与x的关系如图所示。
与x的关系如图所示。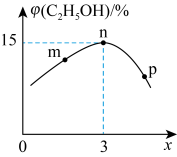
 的转化率最大的是
的转化率最大的是方法2:用电解法可将
 转化为多种原料。
转化为多种原料。(4)用如图装置电解二氧化碳制取甲烷,温度控制在10℃左右,持续通入二氧化碳,电解过程中
 ,物质的量基本不变。写出阴极的电极反应式
,物质的量基本不变。写出阴极的电极反应式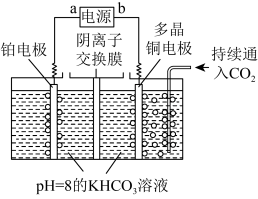
您最近一年使用:0次
2 . 硫及其化合物在生产、生活中有广泛应用。回答下列问题:
Ⅰ.已知:①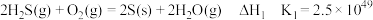
②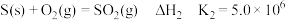
(1)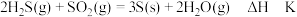 ,根据上述信息推知,
,根据上述信息推知,
___________ ,
___________ (填具体数值)。
Ⅱ.羰基硫 是一种粮食熏蒸剂,能防治某些害虫和真菌的危害。以
是一种粮食熏蒸剂,能防治某些害虫和真菌的危害。以 固体为催化剂,
固体为催化剂, 分别与
分别与 反应制备
反应制备 的反应如下:
的反应如下:
 ;
;
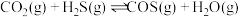 。
。
(2)一定温度下,向恒容密闭容器中充入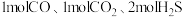 气体,加入适量的
气体,加入适量的 固体(作催化剂,且参与反应),发生上述两个反应。下列叙述正确的是___________(填标号)。
固体(作催化剂,且参与反应),发生上述两个反应。下列叙述正确的是___________(填标号)。
Ⅲ.利用 和
和 反应制备
反应制备 。
。
已知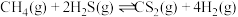 分以下两步进行:
分以下两步进行:
(a)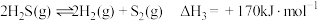
(b)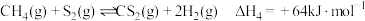
(3) 温度下,保持总压强为
温度下,保持总压强为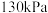 ,向反应器中充入
,向反应器中充入 和
和 ,只发生反应a,测得
,只发生反应a,测得 平衡转化率与投料比
平衡转化率与投料比 的关系如图所示。
的关系如图所示。 增大,
增大, 平衡转化率增大的原因是
平衡转化率增大的原因是___________ ; 温度下,该反应的平衡常数
温度下,该反应的平衡常数
___________  。(提示:用分压计算的平衡常数叫压强平衡常数
。(提示:用分压计算的平衡常数叫压强平衡常数 ,分压等于总压×物质的量分数。)
,分压等于总压×物质的量分数。)
(4)向一密闭容器中通入 和
和 ,同时通入一定量的
,同时通入一定量的 稀释。常压下,不同温度下反应相同时间后,测得
稀释。常压下,不同温度下反应相同时间后,测得 和
和 的体积分数如图所示。
的体积分数如图所示。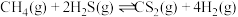 能自发进行的条件是
能自发进行的条件是___________ (填标号)。
a.较低温度 b.较高温度 c.任何温度
②其他条件不变,在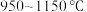 范围内,
范围内, 的体积分数随温度的变化趋势与图
的体积分数随温度的变化趋势与图___________ (填标号)相符。
Ⅰ.已知:①
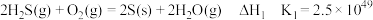
②
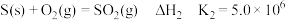
(1)
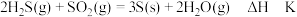 ,根据上述信息推知,
,根据上述信息推知,

Ⅱ.羰基硫
 是一种粮食熏蒸剂,能防治某些害虫和真菌的危害。以
是一种粮食熏蒸剂,能防治某些害虫和真菌的危害。以 固体为催化剂,
固体为催化剂, 分别与
分别与 反应制备
反应制备 的反应如下:
的反应如下: ;
;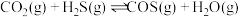 。
。(2)一定温度下,向恒容密闭容器中充入
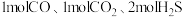 气体,加入适量的
气体,加入适量的 固体(作催化剂,且参与反应),发生上述两个反应。下列叙述正确的是___________(填标号)。
固体(作催化剂,且参与反应),发生上述两个反应。下列叙述正确的是___________(填标号)。| A.气体总压强不变时反应达到平衡状态 |
B.平衡时混合气体中 体积分数的最大值为50% 体积分数的最大值为50% |
C.达到平衡时再充入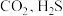 的平衡转化率增大 的平衡转化率增大 |
D.其他条件相同,使用纳米 比使用颗粒 比使用颗粒 的反应速率大 的反应速率大 |
Ⅲ.利用
 和
和 反应制备
反应制备 。
。已知
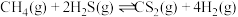 分以下两步进行:
分以下两步进行:(a)
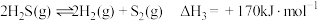
(b)
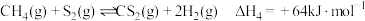
(3)
 温度下,保持总压强为
温度下,保持总压强为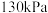 ,向反应器中充入
,向反应器中充入 和
和 ,只发生反应a,测得
,只发生反应a,测得 平衡转化率与投料比
平衡转化率与投料比 的关系如图所示。
的关系如图所示。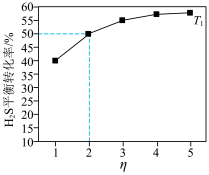
 增大,
增大, 平衡转化率增大的原因是
平衡转化率增大的原因是 温度下,该反应的平衡常数
温度下,该反应的平衡常数
 。(提示:用分压计算的平衡常数叫压强平衡常数
。(提示:用分压计算的平衡常数叫压强平衡常数 ,分压等于总压×物质的量分数。)
,分压等于总压×物质的量分数。)(4)向一密闭容器中通入
 和
和 ,同时通入一定量的
,同时通入一定量的 稀释。常压下,不同温度下反应相同时间后,测得
稀释。常压下,不同温度下反应相同时间后,测得 和
和 的体积分数如图所示。
的体积分数如图所示。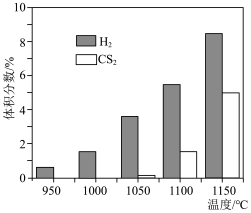
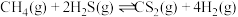 能自发进行的条件是
能自发进行的条件是a.较低温度 b.较高温度 c.任何温度
②其他条件不变,在
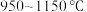 范围内,
范围内, 的体积分数随温度的变化趋势与图
的体积分数随温度的变化趋势与图A.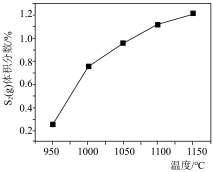 B.
B.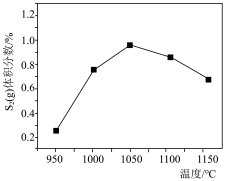
C.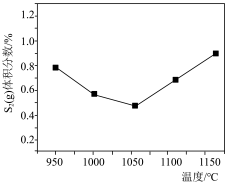 D.
D.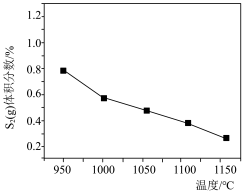
您最近一年使用:0次
3 . 中医药振兴发展意义重大,从中药三七中提取的一种具有生理活性的化学物质槲皮素的结构如图所示。下列关于该化合物的说法错误的是
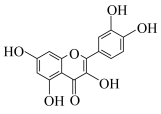
| A.分子中含有3种含氧官能团 |
| B.分子中所有碳原子可能共平面 |
C.不能与 反应产生氢气 反应产生氢气 |
| D.能与氢气发生加成反应 |
您最近一年使用:0次
4 . 下列实验目的对应的实验操作正确的是
| 选项 | 实验目的 | 实验操作 |
| A | 证明酸性: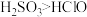 | 将 通入漂白粉溶液,观察是否变浑浊 通入漂白粉溶液,观察是否变浑浊 |
| B | 证明 溶液与 溶液与 反应后 反应后 完全沉淀 完全沉淀 | 反应后静置,取上层清液,向其中再加1滴 溶液,观察是否产生沉淀 溶液,观察是否产生沉淀 |
| C | 证明 具有氧化性 具有氧化性 | 将少量稀硫酸滴入 溶液,观察是否产生刺激性气味的气体 溶液,观察是否产生刺激性气味的气体 |
| D | 证明 和 和 溶度积的大小 溶度积的大小 | 向氢氧化钠溶液中先加入少量 溶液,充分反应后再加入少量 溶液,充分反应后再加入少量 溶液,观察沉淀颜色变化 溶液,观察沉淀颜色变化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
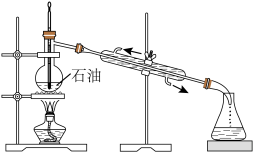
5 . 化学实验操作是进行科学实验的基础。下列操作合理的是
|
|
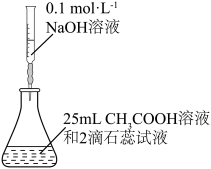
| A.石油分馏 | B.用NaOH标准溶液滴定未知浓度的 溶液 溶液 |
|
|
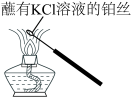
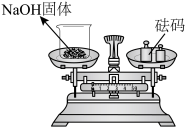
| C.观察K元素的焰色 | D.称量NaOH固体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7日内更新
|
89次组卷
|
6卷引用:2024届青海省西宁市大通县高三下学期高考四模理科综合试卷-高中化学
6 . 氢能是一种重要的绿色能源,在实现“碳中和”与“碳达峰”目标中起到重要作用。
Ⅰ.甲醇―水催化重整可获得氢气。
(1)表中数据是该反应中相关物质的标准摩尔生成焓(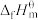 )数据(标准摩尔生成焓是指在298.15K、100kPa下由稳定态单质生成1mol化合物时的焓变)。
)数据(标准摩尔生成焓是指在298.15K、100kPa下由稳定态单质生成1mol化合物时的焓变)。
则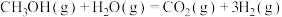 △H=
△H=___________ kJ∙mol-1,该反应在___________ (填“高温”“低温”或“任意温度”)下能自发进行。
Ⅱ.乙醇―水催化重整亦可获得,主要反应如下:
反应①:
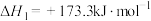
反应②:

(2)向恒容密闭容器中充入1mol 和3mol
和3mol 发生上述反应①和②,初始时体系压强为100kPa.平衡时
发生上述反应①和②,初始时体系压强为100kPa.平衡时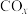 的分布分数
的分布分数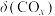 、
、 的产率随温度的变化曲线如图所示。
的产率随温度的变化曲线如图所示。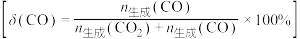
___________ (写出2条)。
②200℃以后,解释曲线a随温度变化趋势的原因:___________ 。
③温度为500℃时,反应经10min达到平衡,此时乙醇的转化率为60%,则0~10min内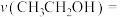
___________ kPa∙min-1,该温度下,反应②的Kp=___________ (保留小数点后两位)。
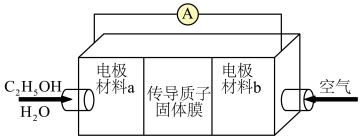
(3)乙醇燃料电池(电极材料a和b均为惰性电极)广泛应用于微型电源、能源汽车、家用电源、国防等领域,工作原理如图所示,写出负极的电极反应式:___________ ,当转移1.2mol电子时,正极消耗的氧气的体积为___________ L(标准状况下)。
Ⅰ.甲醇―水催化重整可获得氢气。
(1)表中数据是该反应中相关物质的标准摩尔生成焓(
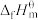 )数据(标准摩尔生成焓是指在298.15K、100kPa下由稳定态单质生成1mol化合物时的焓变)。
)数据(标准摩尔生成焓是指在298.15K、100kPa下由稳定态单质生成1mol化合物时的焓变)。| 物质 |  |  |  |  |
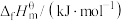 | 0 | ―393.5 | ―241.8 | ―200.7 |
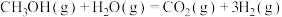 △H=
△H=Ⅱ.乙醇―水催化重整亦可获得,主要反应如下:
反应①:

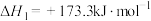
反应②:


(2)向恒容密闭容器中充入1mol
 和3mol
和3mol 发生上述反应①和②,初始时体系压强为100kPa.平衡时
发生上述反应①和②,初始时体系压强为100kPa.平衡时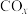 的分布分数
的分布分数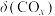 、
、 的产率随温度的变化曲线如图所示。
的产率随温度的变化曲线如图所示。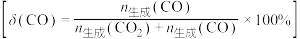
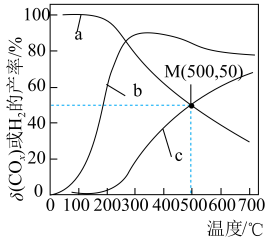
②200℃以后,解释曲线a随温度变化趋势的原因:
③温度为500℃时,反应经10min达到平衡,此时乙醇的转化率为60%,则0~10min内
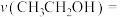
(3)乙醇燃料电池(电极材料a和b均为惰性电极)广泛应用于微型电源、能源汽车、家用电源、国防等领域,工作原理如图所示,写出负极的电极反应式:
您最近一年使用:0次
2024-05-19更新
|
92次组卷
|
3卷引用:2024届青海省部分学校高三下学期模拟考试理综试题-高中化学
名校
解题方法
7 . 物质M转化为物质N的反应如图,下列叙述正确的是

| A.物质M与物质N互为同系物 | B.M中所有的原子可能在同一平面上 |
C.1mol N与碳酸钠反应得44g | D.M、N均能发生加成反应和取代反应 |
您最近一年使用:0次
2024-05-19更新
|
90次组卷
|
2卷引用:2024届青海省部分学校高三下学期模拟考试理综试题-高中化学
名校
解题方法
8 . 一种新型的葡萄糖辅助Cu(Ⅰ)/Cu(Ⅱ)氧化还原耦合制氢系统工作原理如图所示。下列说法错误的是
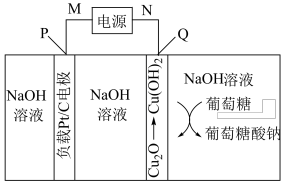
| A.M极为电源负极 | B.P极的电极反应式为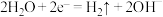 |
| C.电解过程中Q极发生氧化反应 | D.理论上消耗18g葡萄糖,可制得0.2mol |
您最近一年使用:0次
2024-05-19更新
|
88次组卷
|
2卷引用:2024届青海省部分学校高三下学期模拟考试理综试题-高中化学
9 . 铬酸铅(PbCrO4)又称铬黄,是一种重要的黄色颜料,常用作橡胶、水彩、色纸的着色剂。以含铅废渣(主要成分是PbSO4和ZnO,还含Fe3O4、SiO2等)为原料制备铬酸铅的流程如下:
②常温下,几种难溶电解质的溶度积如下:
回答下列问题:
(1)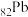 位于周期表第
位于周期表第___________ 周期___________ 族,PbCrO4中Cr的化合价为___________ 。
(2)“碱浸”中PbSO4转化反应的离子方程式为___________ 。
(3)已知:“酸浸”中6.3gHNO3作氧化剂时转移0.3mol电子。气体R在空气中的颜色变化为___________ 。
(4)“酸浸”中铅元素浸出率与温度、硝酸浓度的关系如图所示。“酸浸”最佳条件为___________ 。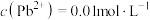 ,“除铁”中控制pH范围为
,“除铁”中控制pH范围为___________ 。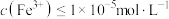 ,则表明Fe3+已完全沉淀。
,则表明Fe3+已完全沉淀。
(6)“沉铬”中生成PbCrO4反应的离子方程式为___________ 。
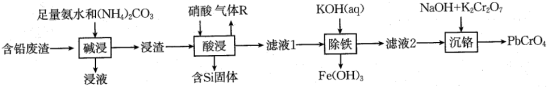
②常温下,几种难溶电解质的溶度积如下:
| 电解质 | PbCO3 | PbSO4 | PbCrO4 | Pb(OH)2 | Fe(OH)3 |
 | 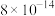 |  | 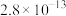 | 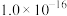 | 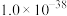 |
(1)
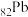 位于周期表第
位于周期表第(2)“碱浸”中PbSO4转化反应的离子方程式为
(3)已知:“酸浸”中6.3gHNO3作氧化剂时转移0.3mol电子。气体R在空气中的颜色变化为
(4)“酸浸”中铅元素浸出率与温度、硝酸浓度的关系如图所示。“酸浸”最佳条件为
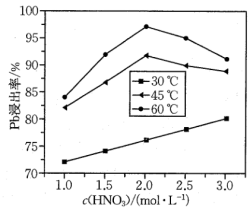
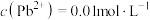 ,“除铁”中控制pH范围为
,“除铁”中控制pH范围为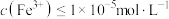 ,则表明Fe3+已完全沉淀。
,则表明Fe3+已完全沉淀。(6)“沉铬”中生成PbCrO4反应的离子方程式为
您最近一年使用:0次
2024-05-18更新
|
56次组卷
|
2卷引用:2024届青海省部分学校高三下学期模拟考试理综试题-高中化学
名校
10 . X、Y、Z、W为原子序数依次增大且互不相邻的四种短周期主族元素,X为元素周期表中原子半径最小的元素,X与W同主族,Y、Z的最外层电子数之和与W的核外电子总数相等。下列说法错误的是
| A.简单离子半径:Z>W | B.仅由X、Y形成的化合物不止一种 |
| C.Y、Z的最高价氧化物对应的水化物均为弱酸 | D.化合物WZ为离子化合物 |
您最近一年使用:0次
2024-05-18更新
|
71次组卷
|
2卷引用:2024届青海省部分学校高三下学期模拟考试理综试题-高中化学