名校
解题方法
1 . 图为铜锌原电池示意图,下列说法中不正确的是

| A.锌片逐渐溶解,铜片上红色固体生成 |
| B.该装置是把电能转变成化学能的装置 |
| C.电子由锌片通过导线流向铜片 |
| D.Cu2+移向铜电极,发生还原反应 |
您最近一年使用:0次
名校
2 . 部分含N及S物质的分类与相应化合价之间的关系如图所示。 下列说法正确的是
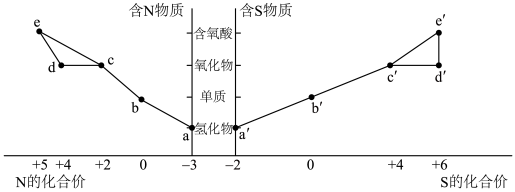
| A.氮元素由游离态转化为化合态,氮元素一定被还原 |
| B.人为活动中排放的c和 d大部分来自于汽车尾气 |
| C.工业上制取 1mol d‘, 只需要投料 64g c’, 和足量的氧气即可 |
| D.e和 e’的浓溶液久置于空气中,溶质质量分数前者减小,后者增大 |
您最近一年使用:0次
3 . 当前,多种因素叠加引发全球性能源供应紧张,能源安全面临复杂挑战。我国已建成世界规模最大的清洁能源体系,逐步完成能源结构的深度转型,最终必将实现“碳中和”目标。如图所示是一种生产和利用氢能的途径,下列说法错误的是

| A.氢能是21世纪最具发展潜力的清洁能源 | B.图中能量转化的方式至少有6种 |
| C.太阳能、风能、氢能都属于新能源 | D.太阳能电池的供电原理与燃料电池相同 |
您最近一年使用:0次
名校
4 . 用如图所示的装置进行实验,将稀硫酸全部加入装置 I的试管中,关闭活塞。 下列说法错误的是
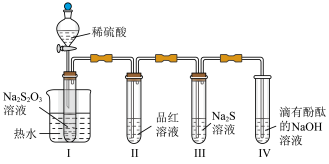
| A.Ⅳ的作用是吸收尾气 SO2,防止污染空气 |
| B.降低稀硫酸浓度,装置 I中试管内出现浑浊所需的时间会变长 |
| C.装置 Ⅱ中品红溶液褪色,与氯水使品红溶液褪色原理相同 |
| D.装置 Ⅲ试管中出现浑浊,说明 SO2 具有氧化性 |
您最近一年使用:0次
名校
解题方法
5 . 下列装置难以达到预期目的的是
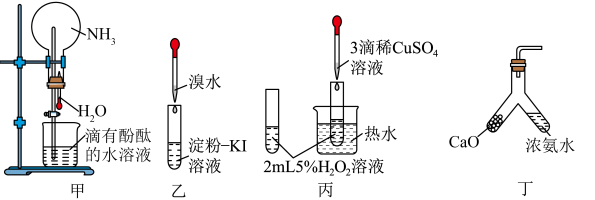
| A.甲:用 NH3 做红色喷泉实验 |
| B.乙:验证溴的得电子能力强于碘 |
| C.丙:证明 CuSO4 溶液对 H2O 分解的催化作用 |
| D.丁:用 CaO和浓氨水制备少量 NH3 |
您最近一年使用:0次
7日内更新
|
65次组卷
|
2卷引用:青海省西宁市第十四中学2023-2024学年高一下学期期中考试化学试卷
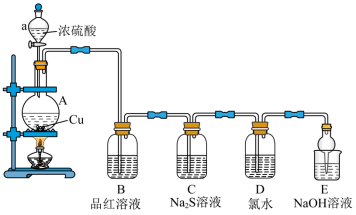
6 . 不同价态硫元素之间有如图所示的转化关系:_______ ,A装置中发生反应的化学方程式为_______ 。
(2)装置B中的现象_______ ,检验SO2具有_______ 性,装置C的现象_______ ,检验SO2具有_______ 性。
(3)写出D装置中发生反应的离子方程式为_______ 。
(4)装置E作用是_______ 。
(5)下列有关硫及其化合物的叙述正确的是_______。
(2)装置B中的现象
(3)写出D装置中发生反应的离子方程式为
(4)装置E作用是
(5)下列有关硫及其化合物的叙述正确的是_______。
| A.硫在足量氧气中燃烧生成SO3 |
| B.向SO2水溶液中滴加Ba(NO3)2溶液,会生成BaSO4白色沉淀 |
| C.浓硫酸与蔗糖反应的实验仅体现了浓硫酸的脱水性 |
| D.除去SO2中含有的少量HCl气体,可以使气体通过饱和NaHSO3溶液 |
您最近一年使用:0次
名校
解题方法
7 . 研究化学能与热能、电能的转化具有重要价值。回答下列问题:
电能是现代社会中应用最广泛的二次能源。
(1)下列装置中能够实现化学能转化为电能的是_______(填字母)。
(2)(1)中的原电池装置中,正极反应方程是_______ 。
(3)若装置中转移了0.2mol电子,负极减少的质量是_______ 。
(4)有甲、乙两位同学均想利用原电池反应检测金属的活动性强弱,两人均使用镁片与铝片作电极,但甲同学将电极放入6mol•L-1的H2SO4溶液中,乙同学将电极放入6mol•L-1的NaOH溶液中,如图所示:_______ 。
②乙中作负极材料是_______ ,总反应的离子方程式:_______ 。
③如果甲同学与乙同学均认为“构成原电池的电极材料都是金属时,则构成负极材料的金属应比构成正极材料的金属活泼”,由此他们会得出不同的实验结论,依据该实验得出的结论中,正确的是_______ (填标号)。
A.镁的金属性不一定比铝的金属性强
B.该实验说明金属活动性顺序表已过时,没有实用价值了
C.利用原电池反应判断金属活动性顺序时应注意选择合适的电解质溶液
D.该实验说明化学研究对象复杂、反应受条件影响较大,因此具体问题应具体分析
(5)下列化学反应过程中的能量变化符合图示的是_______ (填序号)。
③金属钠与水反应 ④酒精燃烧
⑤灼热的碳与二氧化碳反应 ⑥ 与
与 反应
反应
(6)已知键能是表征化学键强度的物理量,可以用键断裂时所需的能量大小来衡量,键能越大,化学键越牢固,含有该键的分子越稳定。某些化学键的键能如下表所示( ):
):
① 在
在 中燃烧,
中燃烧,_______ (填吸收或放出)的热量为_______  。
。
②表中所列化学键形成的单质分子中,最稳定的是_______ (填化学式)。
电能是现代社会中应用最广泛的二次能源。
(1)下列装置中能够实现化学能转化为电能的是_______(填字母)。
A.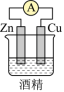 | B. | C.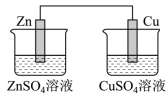 | D.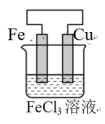 |
(3)若装置中转移了0.2mol电子,负极减少的质量是
(4)有甲、乙两位同学均想利用原电池反应检测金属的活动性强弱,两人均使用镁片与铝片作电极,但甲同学将电极放入6mol•L-1的H2SO4溶液中,乙同学将电极放入6mol•L-1的NaOH溶液中,如图所示:
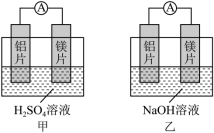
②乙中作负极材料是
③如果甲同学与乙同学均认为“构成原电池的电极材料都是金属时,则构成负极材料的金属应比构成正极材料的金属活泼”,由此他们会得出不同的实验结论,依据该实验得出的结论中,正确的是
A.镁的金属性不一定比铝的金属性强
B.该实验说明金属活动性顺序表已过时,没有实用价值了
C.利用原电池反应判断金属活动性顺序时应注意选择合适的电解质溶液
D.该实验说明化学研究对象复杂、反应受条件影响较大,因此具体问题应具体分析
(5)下列化学反应过程中的能量变化符合图示的是
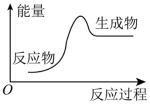
③金属钠与水反应 ④酒精燃烧
⑤灼热的碳与二氧化碳反应 ⑥
 与
与 反应
反应(6)已知键能是表征化学键强度的物理量,可以用键断裂时所需的能量大小来衡量,键能越大,化学键越牢固,含有该键的分子越稳定。某些化学键的键能如下表所示(
 ):
):| 共价键 |  |  |  |
| 键能 | 247 | 431 | 436 |
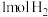 在
在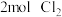 中燃烧,
中燃烧, 。
。②表中所列化学键形成的单质分子中,最稳定的是
您最近一年使用:0次
名校
解题方法
8 . 下列化学反应对应的离子方程式表示正确的是
A.氢氟酸与 反应: 反应: |
B.向氯化铝溶液中滴入过量的氨水: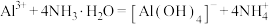 |
C.向 溶液中通入过量 溶液中通入过量 : :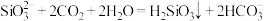 |
D.铁丝插入CuSO4溶液中: |
您最近一年使用:0次
名校
解题方法
9 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.常温常压下,18g重水( )中所含的中子数为 )中所含的中子数为 |
B.标准状况下,14g氮气含有的核外电子数为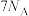 |
C.标准状况下,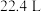 的 的 和 和 组成的混合气体中,含氧原子数为 组成的混合气体中,含氧原子数为 |
D.1mol 与足量 与足量 充分反应,生成的 充分反应,生成的 分子数为 分子数为 |
您最近一年使用:0次
名校
解题方法
10 . 正确掌握化学用语是学好化学的基础,下列有关化学用语表述正确的是
A.质子数为18、中子数为22的氩原子: | B.次氯酸的电子式: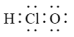 |
C. 的结构示意图: 的结构示意图: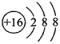 | D.58.5g NaCl晶体含有 个NaCl分子 个NaCl分子 |
您最近一年使用:0次



